
【题目】有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装 置 |
|
|
|
|
部分实验现象 | a极质量减小;b极质量增加 | b极有气体产生;c极无变化 | d极溶解;c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】关于如图装置说法正确的是

A. 装置中电子移动的途径是:负极→Fe→M溶液→石墨→正极
B. 若M为NaCl溶液,通电一段时间后,溶液中可能有NaClO
C. 若M为FeCl2溶液,可以实现石墨上镀铁
D. 若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4CuO![]() 2Cu2O+O2↑,其中Cu2O和CuO中氧元素的化合价均为-2价。关于该反应的叙述正确的是
2Cu2O+O2↑,其中Cu2O和CuO中氧元素的化合价均为-2价。关于该反应的叙述正确的是
A. O2是还原产物
B. 铜元素被还原,氧元素部分被氧化
C. Cu2O是氧化剂
D. 该反应中每生成1个O2,则转移2个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可利用NaCl溶液和AgNO3溶液制备胶体,也可以反应生成沉淀,图中圆的大小代表分散质粒子的相对大小。下列说法正确的是

A. 分散系Ⅰ为溶液
B. 制备分散系I的离子方程式为Ag++Cl-=AgCl(胶体)
C. 分散系Ⅱ为胶体
D. 两分散系的本质区别是是否有丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】营养平衡、科学使用食品添加剂有助于健康和提高免疫力。

(1)维生素C又称抗坏血酸,在氯化铁溶液中加入维生素C后,溶液由黄色转变为浅绿色,说明维生素C具有较强的________性(填“氧化”或“还原”)。
(2)某种食品的配料标签如图所示。该配料中,属于防腐剂的是________,蛋白质在人体内水解的最终产物是氨基酸,氨基酸结构中含有的官能团有氨基和____________(填结构简式)。
(3)“阿司匹林”是一种解热镇痛药,遇潮湿空气或水能缓慢水解生成水杨酸(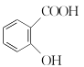 )和醋酸,写出该反应的化学方程式:__________________________。
)和醋酸,写出该反应的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mol·L-1的NaOH溶液分别滴定20mL0.1mol·L-1的HA和HB溶液,溶液pH随加入NaOH溶液的体积变化曲线如图所示,下列判断错误的是
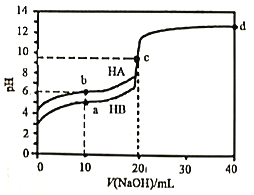
A. 水的电离度:c点溶液>纯水>b点溶液
B. 电离常数:Ka(HA)<Ka(HB)
C. d点溶液:2c(Na+)=c(A-)+(HA)
D. a点溶液:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的基本化工原料,以乙烷为原料生产乙烯有多种方法。
I.乙烷裂解脱氢法。该方法的反应为:C2H6(g)=C2H4(g)+H2(g) △H= a kJ·mol-1
(1)已知101kPa,298K时,C(s)和H2(g)生成lmoC2H6(g)、1molC2H4(g)的△H分别为-84.7 kJ·mol-1、+52.3 kJ·mol-1。则a=___________。
II.乙烧氧化脱氢法,在原料气中加入氧气,乙烷氧化脱氢的反应如下:
2C2H6(g)+O2(g)![]() 2C2H4(g)+2H2O(g) △H<0,副反应都为放热反应,副产物有CH4(g)、CO(g)、CO2(g)。原料气(70.1%空气、29.9%C2H6)在反应器中停留15s,获得相关数据如下表:
2C2H4(g)+2H2O(g) △H<0,副反应都为放热反应,副产物有CH4(g)、CO(g)、CO2(g)。原料气(70.1%空气、29.9%C2H6)在反应器中停留15s,获得相关数据如下表:
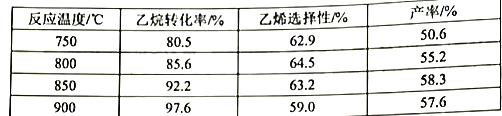
(2)①反应的平衡常数表达式为K=___________,K(750℃)___________K(900℃)(填“>”、“<”、“=”)
②当温度超过800℃时,乙烯的选择性降低,其主要原因可能是___________。根据表中数据选择适宜的反应温度为___________。
III.催化氧化脱氢法。以Mo-V-Nb-Sb的氧化物为催化剂,在常压、380℃下,反应速率与氧气分压[P(O2)]、乙烷分压[P(C2H6)的关系如下图所示。
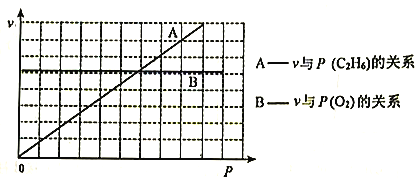
(3)已知该反应的速率方程为v=kPm(O2)·Pn(C2H6),则m=___________,n=___________。
IV质子膜燃料电池法。
(4)乙烷氧化制乙烯会产生CO2的大量排放,近年研究人员开发了乙烷氧化制乙烯的质子膜燃料电池(SOFC),该燃料电池的负极反应式为______________________,这种电池工作过程中没有CO2排放,原因是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的催化氧化是制硝酸的主要反应之一,其微观示意图如下。下列说法正确的是( )

A.甲的化学式为NH3 , 其水溶液呈碱性B.该反应中元素的化合价都发生改变
C.该反应中甲、乙的质量比为17 :32D.生成物丙、丁的分子个数比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是( )
A. 将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B. 必需的定量仪器有100 mL量筒、250 mL容量瓶和托盘天平
C. 量取浓硫酸的体积为25.0 mL
D. 先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com