
SO2是常见的大气污染物,燃煤是产生SO2的主要原因。工业上有多种方法可以减少SO2的排放。
(1)往煤中添加一些石灰石,可使燃煤过程中产生的SO2转化成硫酸钙。该反应的总化学方程式是___________________________________。
(2)可用多种溶液做燃煤烟气中SO2的吸收液。
①分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHS03时,两种吸收液体积比V(Na2SO3): V(NaOH)= 。
②NaOH溶液吸收了足量的:SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式是 。
(3)甲同学认为BaCl2溶液可以做SO2的吸收液。为此甲同学设计如下实验(夹持装置和加热装置略,气密性已检验)。反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B中有白色沉淀。甲同学认为B中白色沉淀是SO2与BaCl2溶液反应生成的BaSO3,所以BaCl2溶液可做SO2 吸收液。
吸收液。
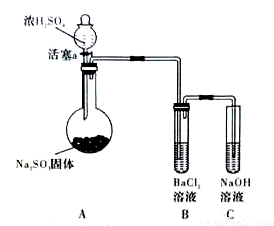
乙同学认为B中的白色沉淀是BaSO4,产生BaSO4的原因是:
①A中产生的白雾是浓硫酸的酸雾,进入B中与BaCI2溶液反应生成BaSO4沉淀。
② 。
为证明 SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略,气密性已检验):
SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略,气密性已检验):
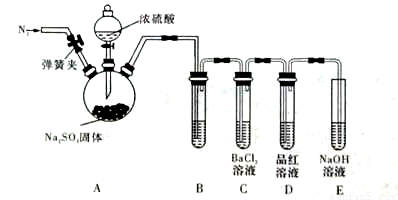
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其它现 象;D中红色褪去。
象;D中红色褪去。
③试管B中试剂是 溶液;滴加浓硫酸之前的操作是 。
④通过甲、乙两位同学的实验,得出的结论是 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届山东省高三上学期期中测试化学试卷(解析版) 题型:选择题
在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g) 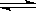 nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是
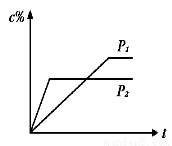
A.P1>P2,n<3 B.P1<P2,n>3
C.P1>P2,n>3 D.P1<P2,n<3
查看答案和解析>>
科目:高中化学 来源:2015-2016河北石家庄第一中学高二上期中考试化学试卷(解析版) 题型:选择题
具有解热镇痛及抗生素作用的药物芬必得主要成分的结构简式为
 ,它属于
,它属于
①芳香族化合物 ②脂肪族化合物 ③有机羧酸 ④有机高分子化合物 ⑤芳香烃
A.③⑤ B.②③ C.①③ D.①④
查看答案和解析>>
科目:高中化学 来源:2016届山西康杰中学等四校高三上第二次联考理化学试卷(解析版) 题型:选择题
某芳香族化合物甲的分子式为C10H11ClO2,已知苯环上只有两个取代基,其中一个取代基为—Cl,甲能与饱和碳酸氢钠溶液反应放出二氧化碳,则满足上述条件的有机物甲的同分异构体数目有多少种
A.5种 B.9种 C.12种 D.15种
查看答案和解析>>
科目:高中化学 来源:2016届江苏常州一中、江阴南菁高中高三两校联考化学卷(解析版) 题型:填空题
NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Fe、Cr等杂质)为原料获得。工艺流程如下图:
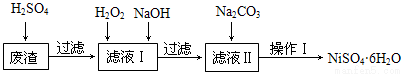
已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示。
Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
Ksp | 8.0×10—16 | 4.0×10—38 | 6.0×10—31 | 6.5×10—18 |
完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
注:NiCO3是一种不溶于水易溶于强酸的沉淀。
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有 。
A.升高反应温度 B.增大压强 C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2,其作用是 (用离子方程式表示);
加入NaOH调节pH的范围是 ,为了除去溶液中的 离子。
(3)滤液Ⅱ的主要成分是 。
(4)检验Ni2+已完全沉淀的实验方法是 。
(5)操作Ⅰ的实验步骤依次为:
① ;
② ;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体;
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省株洲市高三上学期期中化学试卷(解析版) 题型:实验题
酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下:
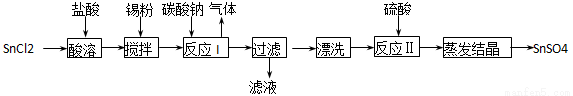
回答下列问题:
(1) SnCl2用盐酸而不用水直接溶解的原因是:_______________;加入锡粉的作用是:_______________;
(2) 反应I生成的沉淀为SnO,写出该反应的化学方程式:_______________;
(3) 检验沉淀已经“洗涤”干净的操作是:______________________________;
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH。若溶液中c(Sn2+)=1.0mol·L-1,则室温下应控制溶液pH _______________。(已知:Ksp[Sn (OH)2]=1.0×10-26)
(5)酸性条件下,SnSO4还可用作双氧水的去除剂,试写出所发生反应的离子方程式:_______________。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三第三次月考理综化学试卷(解析版) 题型:选择题
下列各组物质中,能一步实现右图所示①~⑤转化关系的是

X | Y | Z | W | |
A | C | CO | CO2 | Na2CO3 |
B | Fe3O4 | Fe | FeCl2 | FeCl3 |
C | H2SO4 | SO2 | S | SO3 |
D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源:2016届湖南长沙市三上学期第四次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的数值,下列叙述正确的是
A.在标况下,22.4LSO3和22.4LC2H4原子个数比为2:3
B.将78gNa2O2与过量CO2反应CO2转移的电子数为2NA
C.含0.2molH2SO4的浓硫酸与足量铜充分反应,生成SO2分子的数目少于0.1NA
D.电解精炼铜时,若阳极质量减少32g,则阴极转移的电子的数目为NA
查看答案和解析>>
科目:高中化学 来源:2016届江西南昌第二中学高三上第三次考试理综化学试卷(解析版) 题型:实验题
氯离子插层镁铝水滑石[Mg2Al(OH)6Cl•xH2O]是一种新型离子交换材料。某课外活动小组同学利用如图甲装置(固定装置略去)测定[Mg2Al(OH)6Cl•xH2O]的化学式,[Mg2Al(OH)6Cl•XH2O]高温下分解为MgO、Al2O3、HCl和水蒸气。

(1)装置连接后首先进行的操作是______________________________。
(2)将一定质量的[Mg2Al(OH)6Cl•xH2O]放在加热装置中充分加热,冷却后称量剩余固体的质量是131g,则其中MgO的质量是_______g。
(3)若只通过测定装置C、D的增重来确定x,加热前先通过N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2 。
①装置的连接顺序为a→ (用接口处的小写字母表示)。
②实验过程中装置C吸收HCl气体,没有用如图乙所示防倒吸装置的理由是_______________。
③完全分解后测得C增重3.65g、D增重9.90g,则x=______。
(4)下列实验方案也能测定x值的是 ,并且对不选方案说明不合理的理由:__________(若两个方案都选,此问就不作答)。
方案1:测定加热装置剩余固体的质量和装置D增重的质量
方案2:测定加热装置剩余固体的质量和装置C增重的质量
(5)上述水滑石在空气中放置时易发生反应生成[Mg2Al(OH)6Cl1-2x(CO3)y • zH2O],该生成物能发生类似的热分解反应。现以此物质为样品,用(2)中连接的装置和试剂进行实验测定z,除测定D的增重外,至少还需测定下列数据中的 (填a、b、c等字母) 。
a.样品质量 b.样品分解后残余物质量 c.装置C的增重
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com