
����Ŀ���±����й����ʵ�Ksp��
���� | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
Ksp(��λʡ��) | 2.8��10-9 | 6.8��10-6 | 4.7��10-6 | 5.6��10-12 |
�ش��������⣺
��1��___(������������������)ֱ�Ӱѱ�����ĥ�ɷ�ĩ���뺣ˮ�У�ʹMg2+ת��ΪMgCO3������ԭ����_______��
��2��ʵ���������ǰ�Mg2+ת��ΪMg(OH)2������������ת��ΪMgCO3������ԭ����______�������Ʋ�Ӧ�����ǽ��������ļӹ�����_____��
��3��ijͬѧ��ʵ����������ģ����������̣��ڼ��Լ�ʱ��������Һ���뺣ˮ�У���˼����һ�£����ڵõ��Ļ����ϵ�м���������ռ���Һ���������_____(������������������)��Mg2+ת��ΪMg(OH)2������������__________��
��4��Ҫ�Ƶ���ˮMgCl2�����˳�Mg(OH)2���������Լ�_____(�ѧʽ)�����ܽ⣬ѡ����Լ���������__________��
��5�����õ����Ȼ�þ��Һ��Ũ�������Ƶ�MgCl2��6H2O��Ȼ��MgCl2��6H2Oת�Ƶ��������У��ڸ����HCl�����м���MgCl2��6H2O�����ܵõ���ˮMgCl2��ԭ����_______��
���𰸡����� MgCO3���ܽ�ȱ�CaCO3���ܽ�ȴ�ֱ�Ӽӱ��Ƿ�ĩ�ò���MgCO3���� ΪʹMg2+������ȫ��Ӧ��Mg2+ת��Ϊ�ܽ�ȸ�С��Mg(OH)2 ��ĥ�����ա���ˮ�Ƴ�ʯ���� �� �ռ���Һ���������OH-�ܽ��MgCO3�ܽ������Mg2+�����ܽ�ȸ�С��Mg(OH)2������ʹMgCO3�ij����ܽ�ƽ�ⲻ�������ƶ� HCl �����ܽ�Mg(OH)2��������MgCl2��H2O���������µ����� MgCl2��6H2O����ʱ��ˮ�⣬Ҫ�ڸ����HCl�����м���������ˮ��
��������
(1)���ݱ�����Ҫ�ɷ���CaCO3������ܽ��Է�����
(2)�����ܶȻ�������̼��þ���ܽ�ȴ���������þ�������Ҫ��̼���ת��Ϊ�������ƣ��ݴ˷������
(3)�ռ�Ҳ���Գ���þ���ӣ���������Ǵ���̼���ƣ�������̼��þ����������������Һ������������ƶ�̼��þ���ܽ�ƽ���Ӱ��������
(4)�Ӳ����������ʽǶȷ����жϣ�
(5)�Ȼ�þ�е�þ������ˮ�⣬�����Ի����¿�������ˮ�⡣
(1)���ǵ���Ҫ�ɷ���CaCO3��������ˮ�������ܶȻ�������̼��Ʊ�MgCO3��Ҫ���ܣ����Խ�CaCO3��ֱ��Ͷ�뺣ˮ�в��ܲ���MgCO3�������ʴ�Ϊ�����ܣ�������ĥ�ɷ�ĩ����CaCO3������CaCO3��MgCO3��Ҫ���ܣ����Խ���ֱ��Ͷ�뺣ˮ�в��ܲ���MgCO3��
(2)�����ܶȻ�������̼��þ���ܽ�ȴ���������þ��ΪʹMg2+������ȫ��Ӧ��Mg2+ת��Ϊ�ܽ�ȸ�С��Mg(OH)2�����Խ���CaCO3ת��ΪCaO���䷴Ӧ����ʽΪ��CaCO3 ![]() CaO+CO2����CaO����ˮ��Ӧ���ɼ����þ���ӷ�Ӧ����������þ�������ʴ�Ϊ��ΪʹMg2+������ȫ��Ӧ��Mg2+ת��Ϊ�ܽ�ȸ�С��Mg(OH)2����ĥ�����ա���ˮ�Ƴ�ʯ���飻
CaO+CO2����CaO����ˮ��Ӧ���ɼ����þ���ӷ�Ӧ����������þ�������ʴ�Ϊ��ΪʹMg2+������ȫ��Ӧ��Mg2+ת��Ϊ�ܽ�ȸ�С��Mg(OH)2����ĥ�����ա���ˮ�Ƴ�ʯ���飻
(3)�����þ���ӷ�Ӧ�ܹ���������ˮ��̼��þ�������ռ���Һ���������OH-�ܽ��MgCO3�ܽ������Mg2+�����ܽ�ȸ�С��Mg(OH)2������ʹMgCO3�ij����ܽ�ƽ�ⲻ�������ƶ���ʹ̼��þת��Ϊ������þ�����������з�Ӧ�����ӷ���ʽΪ��Mg2++CO32-=MgCO3��MgCO3+2OH-=Mg(OH)2+CO32-���ʴ�Ϊ���ܣ��ռ���Һ���������OH-�ܽ��MgCO3�ܽ������Mg2+�����ܽ�ȸ�С��Mg(OH)2������ʹMgCO3�ij����ܽ�ƽ�ⲻ�������ƶ���
(4)Ҫ�Ƶ���ˮMgCl2�����˳�Mg(OH)2������Ϊ�˲����������ʣ����������Ὣ���ܽ⣬�ʴ�Ϊ��HCl�������ܽ�Mg(OH)2��������MgCl2��H2O���������µ����ʣ�
(5)�Ȼ�þ�е�þ������ˮ�⣬�ڸ����HCl�����У���������MgCl2ˮ�⣬�Ҵ���MgCl26H2O���Ȳ�����ˮ�������ܵõ���ˮMgCl2���ʴ�Ϊ��MgCl2��6H2O����ʱ��ˮ�⣬Ҫ�ڸ����HCl�����м���������ˮ�⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ⶨ![]() ��Һ�������ٽ��¹����е�pH���������¡�ʵ������У�ȡ�٢�ʱ�̵���Һ�����������ữ��BaCl2��Һ���Ա�ʵ�顣�ܲ�����ɫ�����ࡣ����˵������ȷ����
��Һ�������ٽ��¹����е�pH���������¡�ʵ������У�ȡ�٢�ʱ�̵���Һ�����������ữ��BaCl2��Һ���Ա�ʵ�顣�ܲ�����ɫ�����ࡣ����˵������ȷ����![]()
![]()
ʱ�� | �� | �� | �� | �� |
�¶� | 25 | 30 | 40 | 25 |
pH |
|
|
| 9.25 |
A.![]() ��Һ�д���ˮ��ƽ�⣺
��Һ�д���ˮ��ƽ�⣺![]()
B.�ܵ�pH��ٲ�ͬ��������![]() Ũ�ȼ�С��ɵ�
Ũ�ȼ�С��ɵ�
C.�١��۵Ĺ����У��¶Ⱥ�Ũ�ȶ�ˮ��ƽ���ƶ������Ӱ��һ��
D.����ܵ�![]() ֵ���
ֵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�л���ṹ��ͼ������˵������ȷ����![]()

A. �����ʵĻ�ѧʽΪC15H8O8BrCl
B. ����������![]() ��Һ������ɫ��Ӧ
��Һ������ɫ��Ӧ
C. 1mol�������������3mol��ˮ�����ӳɷ�Ӧ
D. һ�������£�1mol�������������8molNaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��B��C��D��EΪ���ڱ�1��36���е�Ԫ�أ����ǵ�ԭ������������A��һ��������Ϊ14��ԭ�ӳ������ⶨ����������C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������Aԭ����ͬ��C2-����D2+���Ӿ�����ͬ�ġ��ȶ��ĵ��Ӳ�ṹ��E�Ļ�̬ԭ�ӵ���Χ�����Ų�ʽΪ3d64s2��
(1)A��B��C��D����Ԫ���У��縺��������_______________(��Ԫ�ط���)��
(2)�ȵ�����������ƵĽṹ�����ʡ�AC��B2��AC2��CAB-����Ϊ�ȵ����壬��AC�ĵ���ʽΪ_________��CAB-��Aԭ�ӵ��ӻ���ʽΪ_________����E����AC�����γ�E(AC)5����ԭ����AC�����к���______________________��
(3)������֣�ֻ��A��D��E����Ԫ�ص�һ�־���(������ͼ��ʾ)���г����ԡ�Aԭ�ӵ���λ��Ϊ___________���þ���Ļ�ѧʽΪ___________��
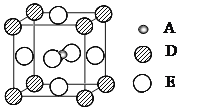
(4)��֪C��E�γɵ�һ�־���ExC�������ṹΪNaCl�ͣ����ھ���ȱ�ݣ�xֵС��1����֪�þ����ܶ�Ϊ��=3.53g/cm3�������߳�Ϊ5.0��10-10m����þ�����xֵ(��ȷ��0.1)Ϊ_______�������е�Fen+�ֱ�ΪFe2+��Fe3+����Fe2+��Fe3+�ı�ֵΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ��ࣩ��(Ba)����(Sr)���仯�����ڹ�ҵ�����Ź㷺��Ӧ�ã������ڵؿ��г��������ε���ʽ���ڣ�BaSO4��SrSO4�����������Ρ���ҵ����ȡ������ʱ���Ƚ�BaSO4��SrSO4ת�������������Ρ�
��֪��SrSO4(s)![]() Sr2��(aq)��SO
Sr2��(aq)��SO![]() (aq)�� Ksp��2.5��10��7
(aq)�� Ksp��2.5��10��7
SrCO3(s)![]() Sr2��(aq)��CO
Sr2��(aq)��CO![]() (aq) ��Ksp��2.5��10��9
(aq) ��Ksp��2.5��10��9
��1����SrSO4ת����SrCO3�����ӷ���ʽΪ________________________________���÷�Ӧ��ƽ�ⳣ��Ϊ__________________����������֣����÷�Ӧ�ܷ�����ԭ����
_________________________________________(�ó����ܽ�ƽ����й����۽���)��
��2������������Ӧ��ʵ��֤������CO![]() ��Ũ�Ȼ��¶ȶ����������SrSO4��ת���ʡ��ж���������������£�ƽ�ⳣ��K�ı仯���(����������������С������������)��
��Ũ�Ȼ��¶ȶ����������SrSO4��ת���ʡ��ж���������������£�ƽ�ⳣ��K�ı仯���(����������������С������������)��
�������¶ȣ�ƽ�ⳣ��K��________��������CO![]() ��Ũ�ȣ�ƽ�ⳣ��K��________��
��Ũ�ȣ�ƽ�ⳣ��K��________��
��3����֪��SrSO4��SrCO3�����е��ܽ�����BaSO4��BaCO3���ƣ����ʵ��֤������������SrSO4�Ƿ���ȫת����SrCO3��ʵ�����õ��Լ�Ϊ________��ʵ����������Ӧ����Ϊ_________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1000mol��L-1NaOH��Һ�ζ�20.00mL0.1000mol��L-1HA��Һ���õζ�������ͼ������˵������ȷ����

A.HA�ĵ���ƽ�ⳣ��Ka=10-5
B.�����ʾ����Һ�У�2c(Na+)=c(A-)+c(HA)
C.�����ʾ����Һ�У�c(HA)>c(OH-)-c(H+)
D.�����ʾ����Һ�У�2c(OH-)-2c(H+)=c(A-)+3c(HA)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��Ӧ2H2��g��+O2��g��=2H2O��g���������仯ʾ��ͼ������˵����ȷ����

A. ��2molH2 ��g����1 molO2��g���еĻ�ѧ����ΪH��Oԭ�ӣ����ų�1368 kJ����
B. ��H��Oԭ���γ�2 molH2O��g����������1852 kJ����
C. 2 molH2 ��g����1 molO2 ��g����Ӧ����2 molH2O��1����������484 kJ����
D. 2 molH2 ��g����1 molO2��g����Ӧ����2 moIH2O��g�������ų�484 kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ������������ѧ�ң�1776.08.09-1856.07.09��������ҵ����ʦ��24�������������ʮ���ڷܣ��ճ�һ����ѧ��ʦ��Ϊ�˼����������ǰ�1 molij���������������е����Ӹ�������Ϊ�����ӵ���������N![]() ��ʾ������˵�����ʾ�в���ȷ����
��ʾ������˵�����ʾ�в���ȷ����

A.��ѧ�Ϲ涨���а����ӵ����������ӵ��κ��������嶼Ϊ1 mol
B.��K37ClO3+6H35Cl��Ũ��=KCl+3Cl2��+3H2O��Ӧ�У�����212���������ɣ���Ӧ�е���ת�Ƶ���ĿΪ5NA
C.60 �˵�����������ǻ������ȼ������2NA��O2
D.6.02��1023mol-1 ���������ӵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.l00mol/L NaOH��Һ�ֱ�ζ�20.00 mL 0.100 mol/L������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ����

A. II��ʾ���ǵζ����������
B. pH=7ʱ���ζ��������ĵ�V(NaOH)С��20 mL
C. V(NaOH)=" 20.00" mLʱ��������Һ��c(Cl-)= C(CH3COO-)
D. V(NaOH) ="10.00" mLʱ��������Һ��c(Na+)> C(CH3COO-)> c(H+)> c(OH-)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com