
(16分)I.将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,各物质浓度随时间变化的关系如图1所示。
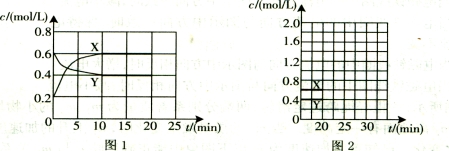
请回答:
(1)下列选项中不能说明该反应已达到平衡状态的是 (填选项字母)。
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)反应进行到10 min时,共吸收热量11.38 kJ,则该反应的热化学方程式为
;
(3)计算该反应的平衡常数K= 。
(4)反应进行到20 min时,再向容器内充入一定量NO2,10min后达到新的平衡,此
时测得c(NO2)=0.9 mol/L。
第一次平衡时混合气体中NO2的体积分数为w1,达到新平衡后混合气体中NO2的体积分数为w2,则w1 w2 (填“>”、“=”或“<”);
请在图2中画出20 min后各物质的浓度随时间变化的曲线(曲线上必须标出“X”和
“Y”)。
II.(1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学
电源的重要原料。如LiFePO4电池中某电极的工作原理如下图所示:

该电池的电解质为能传导Li+的固体材料。放电时该电极是电池的 极(填“正”或“负”),该电极反应式为 。
(2)用此电池电解含有0.1 mol/L CuSO4和0.1 mol/L NaCl的混合溶液100 mL,假如电路中转移了0.02 mol e-,且电解池的电极均为惰性电极,阳极产生的气体在标准状况下的体积是__________L.
Ⅰ.(1)B (2分)
(2)N2O4(g)  2NO2(g) △H=+56.9kJ/mol (2分)
2NO2(g) △H=+56.9kJ/mol (2分)
(3)0.9 (2分) (4)① > (2分) ②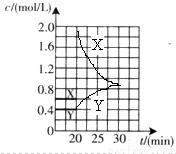 (2分)
(2分)
Ⅱ.正(2分) FePO4+e-+Li+=LiFePO4 (2分) 0.168 (2分)
【解析】
试题分析:Ⅰ.(1)A、反应前后气体的化学计量数之和不等,故容器总压强不随时间改变可作为判断是否达到化学平衡状态的依据,正确;B、总质量不变,体积也不变,故混合气体的密度不随时间变化而改变不能作为判断是否达到化学平衡状态的依据,错误;C、NO2为红棕色气体,N2O4为无色气体,故混合气体的颜色不随时间变化而改变可作为判断是否达到化学平衡状态的依据,正确;D、总质量不变,总物质的量在变,故反应混合气平均分子量不再改变可作为判断是否达到化学平衡状态的依据,正确。
(2)由图1可知,反应物为N2O4,生成物为NO2,反应进行到10min时,N2O4的物质的量变化为0.2mol/L×1L=0.2mol,共吸收热量11.38kJ,故反应1molN2O4共吸收热量11.38×5=56.9kJ,故该反应热化学 方程式为:N2O4(g)?2NO2(g),△H=+56.9kJ?mol?1。
(3)k= c2(NO2)/ c(N2O4) =0.62÷0.4=0.9。
(4)①恒容,充入一定量NO2,相当于增大压强,平衡逆向移动,新平衡后混合气体中NO2的体积分数减小,故W1>W2。
②30min时,c(NO2)=0.9mol/L,k=0.92 ÷c(N2O4) =0.9,c(N2O4)=0.9mol/L,20min-30min,N2O4的浓度增加了0.9-0.4=0.5mol/L,故NO2的浓度减少了1mol/L,则20min时,c(NO2)=1+0.9=1.9mol/L,可画出20 min后各物质的浓度随时间变化的曲线。
Ⅱ.(1)放电时,该装置是原电池,Fe元素化合价由+3价变为+2价,得电子发生还原反应,所以该电极是正极,电极反应式为FePO4+e-+Li+=LiFePO4。
(2)计算得到,电解含有0.01mol CuSO4和0.01molNaCl的混合溶液100mL,电路中转移了0.02mol e-,
阳极:2Cl- -2e- =Cl2↑,
0.01mol 0.01mol 0.005mol
4OH--4e-=2H2O+O2↑,
0.01mol 0.01mol 0.0025mol所以阳极上生成的气体在标准状况下的体积=(0.005mol+0.0025mol)×22.4L/mol=0.168L。
考点:本题考查图像的分析及绘画、化学平衡状态、化学平衡常数、热化学方程式、原电池原理及应用。


科目:高中化学 来源:2015届湖北省襄阳市四校高二下学期期中联考化学试卷(解析版) 题型:选择题
下列元素性质的递变规律正确的是( )
A.原子半径:Be<B<C<N
B.第一电离能:B<Be<Mg<Na
C.元素的电负性:O>N>P>Si
D.气态氢化物的稳定性:NH3<CH4<PH3<SiH4
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3  K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
A.生成40.0LN2(标准状况) B.有0.250molKNO3被氧化
C.转移电子的物质的量为1.25mol D.被氧化的N原子的物质的量为3.5mol
查看答案和解析>>
科目:高中化学 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠而成。则下列分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成的是( )
A.H2 B.HCl C.Cl2 D.F2
查看答案和解析>>
科目:高中化学 来源:2015届湖北省孝感市七校联考高二下学期期中考试化学试卷(解析版) 题型:选择题
下列化合物中含有手性碳原子的是
A.CCl2F2 B.CH3CH3 C.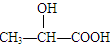 D.CH3CH2OH
D.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2015届浙江省协作体高考摸底测试理科综合化学试卷(解析版) 题型:选择题
(1)已知t ℃时AgCl的Ksp=2×10-10 ;(2)在t ℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )。

A.在t ℃时,Ag2CrO4的Ksp为1×10-9
B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点
C.在t℃时,以0.01 mol/L AgNO3溶液滴定20 mL0.01 mol/LKCl和0.01 mol/L的K2CrO4的混和溶液,Cl-先沉淀
D.在t ℃时,AgCl的溶解度大于Ag2CrO4
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高二下学期期中联考化学试卷(解析版) 题型:实验题
溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。

实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH水溶液和5 mL 溴乙烷,将试管如图固定后,加热。
(1)请写出该反应的化学方程式 。
(2)观察到 现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)欲将生成的乙醇从反应混合物中进行分离出来,最简单的操作是 。
(4)请简述如何检验溴乙烷中含有溴元素 。
实验操作II:在试管中加入5 mL NaOH乙醇溶液和5 mL 溴乙烷,将试管如图固定后,加热。
(5)请写出该反应的化学方程式 。
(6)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是 ,检验的方法是 (需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高二下学期期中联考化学试卷(解析版) 题型:选择题
下列物质的说法不正确的是( )
A.某实验过程中得到一定量的碘水,可用裂化汽油从碘水中萃取出碘
B.芳香烃主要来自于煤焦油和石油化工中的催化重整
C.石油分馏可得到石油气、汽油、煤油、轻柴油等馏分
D.乙烯是轻质油裂解的产物,其产量可用来衡量一个国家的石油化工发展水平
查看答案和解析>>
科目:高中化学 来源:2015届浙江省杭州地区六校高二下学期期中联考化学试卷(解析版) 题型:选择题
根据表中信息,判断下列叙述中正确的是
序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
① |
| FeBr2 | / |
| Cl- |
② | MnO2 | 浓盐酸 | / | Cl2 |
|
③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:MnO2>Fe3+>Cl2>Br2
C.表中②组反应的氧化产物是MnCl2,1molMnO2电子转移数目是2NA
D.表中③组反应的离子方程式为:2MnO4—+3H2O2+6H+=2Mn2++4O2↑+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com