

 ;
;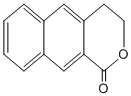 是一种重要的药物合成中间体,请结合题目所给信息,
是一种重要的药物合成中间体,请结合题目所给信息,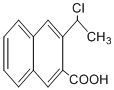 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下: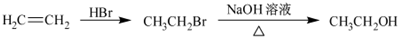
分析 根据合成线路可知,E与新制Cu(OH )2加热条件下反应,酸化后得F,E中含有醛基,则E的结构简式为: ;D催化氧化生成E,则D的结构简式为:
;D催化氧化生成E,则D的结构简式为: ;C水解生成D,则C的结构简式为:
;C水解生成D,则C的结构简式为: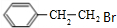 ;F与CH3CH2OH在浓硫酸加热条件下,发生酯化反应生成的G,则G的结构简式为
;F与CH3CH2OH在浓硫酸加热条件下,发生酯化反应生成的G,则G的结构简式为 ,H与H2加成,醛基转化为羟基,则I的结构简式为:
,H与H2加成,醛基转化为羟基,则I的结构简式为: ,据此进行解答.
,据此进行解答.
解答 解:根据合成线路可知,E与新制Cu(OH )2加热条件下反应,酸化后得F,E中含有醛基,则E的结构简式为: ;D催化氧化生成E,则D的结构简式为:
;D催化氧化生成E,则D的结构简式为: ;C水解生成D,则C的结构简式为:
;C水解生成D,则C的结构简式为: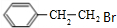 ;F与CH3CH2OH在浓硫酸加热条件下,发生酯化反应生成的G,则G的结构简式为
;F与CH3CH2OH在浓硫酸加热条件下,发生酯化反应生成的G,则G的结构简式为 ,H与H2加成,醛基转化为羟基,则I为:
,H与H2加成,醛基转化为羟基,则I为: ,
,
(1)根据F的结构简式可知,F含有的官能团为羧基;G的结构简式为  ,对比G与H的结构简式,G中CH2上的1个H原子被-CHO代替,所以反应2的反应类型为取代反应;反应3为羟基消去生成碳碳双键,所以反应条件是浓H2SO4、加热,
,对比G与H的结构简式,G中CH2上的1个H原子被-CHO代替,所以反应2的反应类型为取代反应;反应3为羟基消去生成碳碳双键,所以反应条件是浓H2SO4、加热,
故答案为:羧基; 取代; 浓H2SO4、加热;
(2)假设B的相对分子质量等于118,氢的质量分数为7.69%,则可得A中的氢原子个数为9,所以A为苯乙烯,苯与X加成得A,则X为乙炔,
故答案为:乙炔;
(3)D的结构简式为: ,在Cu催化加热条件下,发生催化氧化,生成苯乙醛E,化学方程式为:
,在Cu催化加热条件下,发生催化氧化,生成苯乙醛E,化学方程式为: ,
,
故答案为: ;
;
(4)I( )有多种同分异构体.同时满足下列条件:与FeCl3溶液发生显色反应,含有酚羟基;能发生水解反应和银镜反应,含有甲酸形成的酯基;.苯环上有四个取代基,且苯环上一氯代物只有1种,符合条件的同分异构体有:
)有多种同分异构体.同时满足下列条件:与FeCl3溶液发生显色反应,含有酚羟基;能发生水解反应和银镜反应,含有甲酸形成的酯基;.苯环上有四个取代基,且苯环上一氯代物只有1种,符合条件的同分异构体有: 、
、 、
、 、
、 、
、 、
、 ,总共有6种,
,总共有6种,
故答案为:6;
(5)依次通过消去反应得到碳碳双键,在H2O2条件下与HBr加成,Br在端点的C原子上,水解反应生成-OH,然后发生酯化反应得最终产物,所以合成路线图为: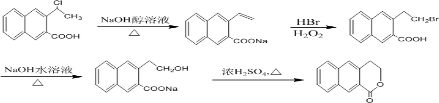 ,
,
故答案为: .
.
点评 本题考查有机合成,题目难度中等,试题涉及有机反应类型、同分异构体书写、有机反应方程式等知识,注意根据反应条件进行推断,需要学生熟练掌握官能团的性质与转化,(4)中同分异构体的书写为易错点、难点.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:解答题
| B | ||
| A | X | C |
| D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
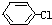 +NaOH→
+NaOH→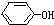 +NaCl,该反应的反应类型属于( )
+NaCl,该反应的反应类型属于( )| A. | 加成反应 | B. | 取代反应 | C. | 氧化还原反应 | D. | 置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
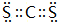 ,Y3-的立体构型为直线形.
,Y3-的立体构型为直线形.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
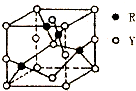 X、Y、Z、R为前四周期元素,原子序数依次增大.X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素; R+离子的3d轨道全充满.请回答下列问题:
X、Y、Z、R为前四周期元素,原子序数依次增大.X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素; R+离子的3d轨道全充满.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
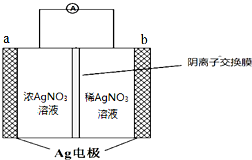 银是一种在工业、生活上有广泛用途的金属.
银是一种在工业、生活上有广泛用途的金属.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| B. | PM 2.5亦称可入肺颗粒物,分散在空气中形成胶体,能吸附有毒有害物$\frac{2b}{a-2b}$质 | |
| C. | “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化 | |
| D. | 绚丽缤纷的烟花中添加了含钾、钠、钙、钡等金属元素的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉与烧碱溶液反应:Al+6OH+═[Al(OH)4]-+H2↑ | |
| B. | 水玻璃中加入稀盐酸:Na2SiO4+2H+═H2SiO3↓+2Na+ | |
| C. | 二氧化硅与苛性钠溶液反应:SiO2+2OH-═SiO32-+H2O | |
| D. | 将氯气通入到水中:Cl2+H2O═2HCl-+ClO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com