
°æƒø°ø”…œ¬¡– µ—Ⱥ∞œ÷œÛ≤ªƒÐÕ∆≥ˆœý”¶Ω·¬€µƒ «
µ—È | œ÷œÛ | Ω·¬€ | |
A. | œÚ | ª∆…´÷Ω•œ˚ ߣ¨º” | ªπ‘≠–‘£∫ |
B. | Ω´Ω Ùƒ∆‘⁄»º…’≥◊÷–µ„»º£¨—∏ÀŸ…ϻκج˙ | ºØ∆¯∆ø÷–≤˙…˙¥Û¡ø∞◊—ã¨∆øƒ⁄”–∫⁄…´ø≈¡£≤˙…˙ |
|
C. | Ω´◊„¡øµƒ | À·–‘ |
|
D. | Ω´ | œ»”–∞◊…´≥¡µÌ…˙≥…£¨∫Û±‰Œ™¿∂…´≥¡µÌ |
|
A.AB.BC.CD.D
°æ¥∞∏°øC
°æΩ‚Œˆ°ø
A£ÆFeCl3µƒ»Ð“∫÷–º”◊„¡øÃ˙∑€£¨ª∆…´÷Ω•œ˚ ߣ¨º”KSCN»Ð“∫—’…´≤ª±‰£¨Àµ√˜∑¥”¶…˙≥…¡À¬»ªØ—«Ã˙£¨ƒÐπªÀµ√˜ªπ‘≠–‘£∫Fe£æFe2+£¨π A’˝»∑£ª
B£Æƒ∆”Î∂˛—ıªØú∑¥”¶£¨ºØ∆¯∆ø÷–≤˙…˙¥Û¡ø∞◊—ã¨∆øƒ⁄”–∫⁄…´ø≈¡£≤˙…˙£¨Àµ√˜…˙≥…¡ÀúÀ·ƒ∆°¢C£¨Àµ√˜CO2æþ”–—ıªØ–‘£¨π B’˝»∑£ª
C£Æ—«Ã˙¿Î◊”º∞π˝¡øµƒ∂˛—ıªØ¡Úæ˘ π∏þ√ÃÀ·ºÿ»Ð“∫Õ …´£¨”…œ÷œÛ≤ªƒÐÀµ√˜SO2”ÎFeCl3∑¢…˙¡À—ıªØªπ‘≠∑¥”¶£¨π C¥ÌŒÛ£ª
D£Æœ»”–∞◊…´≥¡µÌ…˙≥…£¨∫Û±‰Œ™¿∂…´≥¡µÌ£¨Àµ√˜∑¢…˙¡À≥¡µÌµƒ◊™ªØ£¨”…œ÷œÛø…÷™Ksp[Cu(OH)2]£ºKsp[Mg(OH)2]£¨π D’˝»∑£ª
π —°C°£


 ¿ºÕ∞ŸÕ®∆⁄ƒ©ΩæÌœµ¡–¥∞∏
¿ºÕ∞ŸÕ®∆⁄ƒ©ΩæÌœµ¡–¥∞∏
| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø»˝¡Ú¥˙úÀ·ƒ∆(Na2CS3)≥£”√◊˜…±æ˙º¡°¢≥¡µÌº¡°£ƒ≥–°◊ȅ˺∆ µ—ÈÃΩæø»˝¡Ú¥˙úÀ·ƒ∆µƒ–‘÷ ≤¢≤‚∂®∆‰»Ð“∫µƒ≈®∂»°£
µ—È1£∫ÃΩæøNa2CS3µƒ–‘÷
≤Ω÷Ë | ≤Ÿ◊˜º∞œ÷œÛ |
¢Ÿ | »°…Ÿ¡øNa2CS3πÃûД⁄’Ù¡ÛÀÆ≈‰÷∆≥…»Ð“∫≤¢∑÷≥…¡Ωµ»∑ð |
¢⁄ | œÚ∆‰÷–“ª∑ð»Ð“∫÷–µŒº”º∏µŒ∑”Ù ‘“∫£¨»Ð“∫±‰∫Ï…´ |
¢€ | œÚ¡Ì“ª∑ð»Ð“∫÷–µŒº”À·–‘KMnO4»Ð“∫£¨◊œ…´Õ »• |
£®1£©H2CS3 «________À·£®ÃÓ°∞«ø°±ªÚ°∞»ı°±£©°£
£®2£©“—÷™≤Ω÷Ë¢€µƒ—ıªØ≤˙ŒÔ «SO42£≠,–¥≥ˆ∏√∑¥”¶µƒ¿Î◊”∑Ω≥à Ω______
£®3£©ƒ≥Õ¨—ß»°≤Ω÷Ë¢€À˘µ√»Ð“∫”⁄ ‘πÐ÷–£¨µŒº”◊„¡ø—ŒÀ·°¢BaCl2»Ð“∫≤˙…˙∞◊…´≥¡µÌ£¨À˚»œŒ™Õ®π˝≤‚∂®≤˙…˙µƒ∞◊…´≥¡µÌµƒ÷ ¡øº¥ø…«Û≥ˆ µ—ÈÀ˘”√Na2CS3µƒ¡ø£¨ƒ„ «∑ÒÕ¨“‚À˚µƒπ€µ„≤¢Àµ√˜¿Ì”…______°£
µ—È2£∫≤‚∂®Na2CS3»Ð“∫µƒ≈®∂»

∞¥»ÁÕºÀ˘ æ¡¨Ω”∫√◊∞÷√£¨»°100mLNa2CS3»Ð“∫÷√”⁄»˝æ±…’∆ø÷–£¨¥Úø™“«∆˜dµƒªÓ»˚£¨µŒ»Î◊„¡ø2.0mol/Lœ°H2SO4£¨πÿ±’ªÓ»˚°£
“—÷™£∫Na2CS3 + H2SO4=Na2SO4 + CS2 + H2S°¸°£CS2∫ÕH2Sæ˘”–∂æ°£CS2≤ª»Ð”⁄ÀÆ£¨∑–µ„46°Ê£¨”ÎCO2ƒ≥–©–‘÷ œýÀ∆£¨”ÎNaOH◊˜”√…˙≥…Na2COS2∫ÕH2O°£
£®4£© ¢∑≈ŒÞÀÆCaCl2µƒ“«∆˜µƒ√˚≥∆ «______£¨B÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «______°£
£®5£©∑¥”¶Ω· ¯∫Û¥Úø™ªÓ»˚k£¨‘Ÿª∫¬˝Õ®»Î»»N2“ª∂Œ ±º‰£¨∆‰ƒøµƒ «______°£
£®6£©Œ™¡Àº∆À„Na2CS3»Ð“∫µƒ≈®∂»£¨∂‘B÷–ªÏ∫œŒÔΩ¯––π˝¬À°¢œ¥µ”°¢∏…‘Ô°¢≥∆÷ÿ£¨µ√19.2gπÃ㨑ÚA÷–Na2CS3µƒŒÔ÷ µƒ¡ø≈®∂»Œ™______°£
£®7£©∑÷Œˆ…œ ˆ µ—È∑Ω∞∏£¨ªπø…“‘Õ®π˝≤‚∂®C÷–»Ð“∫÷ ¡øµƒ‘ˆº”÷µ¿¥º∆À„Na2CS3»Ð“∫µƒ≈®∂»£¨»Ù∑¥”¶Ω· ¯∫ÛΩ´Õ®»»N2∏ƒŒ™Õ®»»ø’∆¯£¨º∆À„÷µ______£®ÃÓ°∞∆´∏þ°±°¢°∞∆´µÕ°±ªÚ°∞ŒÞ”∞œÏ°±£©°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø”√œ¬¡– µ—È◊∞÷√ÕÍ≥…∂‘”¶µƒ µ—È(≤ø∑÷“«∆˜“— °¬‘)£¨ƒÐ¥ÔµΩ µ—ȃøµƒµƒ «£®°°°°£©
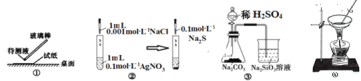
A.¢Ÿ”√pH ‘÷Ω≤‚ƒ≥»Ð“∫µƒÀ·ºÓ–‘
B. µ—È “”√Õº¢⁄À˘ æ◊∞÷√»Ùœ»≥ˆœ÷∞◊…´≥¡µÌ∫Û”÷±‰∫⁄£¨‘ڃб»ΩœKsp(AgCl)©ÉKsp(Ag2S)
C. µ—È “”√Õº¢€À˘ æ◊∞÷√÷§√˜À·–‘£∫H2SO4>H2CO3>H2SiO3
D.Õº¢Ðø…”…AlCl3±•∫ջГ∫÷∆±∏AlCl3æßÃÂ
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø2019ƒÍ≈µ±¥∂˚ªØ—ßΩ±∞‰∏¯¡À»˝ŒªŒ™ÔÆ¿Î◊”µÁ≥ÿ∑¢’π◊˜≥ˆ÷ÿ“™π±œ◊µƒø∆—ߺ“°£¡◊À·Ã˙ÔÆÔÆ¿Î◊”µÁ≥ÿ≥‰µÁ ±—Ùº´∑¥”¶ ΩŒ™,![]() £¨∑≈µÁπ§◊˜ æ“‚Õº»ÁÕº°£œ¬¡–– ˆ≤ª’˝»∑µƒ «
£¨∑≈µÁπ§◊˜ æ“‚Õº»ÁÕº°£œ¬¡–– ˆ≤ª’˝»∑µƒ «
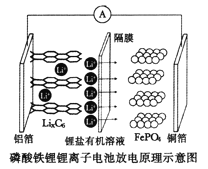
A.∑≈µÁ ±£¨Li+Õ®π˝∏Ùƒ§“∆œÚ’˝º´
B.∑≈µÁ ±£¨µÁ◊””…¬¡≤≠—ÿµºœþ¡˜œÚÕ≠≤≠
C.∑≈µÁ ±’˝º´∑¥”¶Œ™£∫![]()
D.¡◊À·Ã˙ÔÆÔÆ¿Î◊”µÁ≥ÿ≥‰∑≈µÁπ˝≥ÃÕ®π˝Li+«®“∆ µœ÷£¨C°¢Fe°¢P‘™ÀÿªØ∫œº€æ˘≤ª∑¢…˙±‰ªØ
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øƒø«∞£¨¥¶¿Ì—Ã∆¯÷– SO2 ≥£≤…”√¡Ω÷÷∑Ω∑®£∫ºÓ“∫Œ¸ ’∑®∫ÕÀÆ√∫∆¯ªπ‘≠∑®°£
¢Ò.ºÓ“∫Œ¸ ’∑®
25°Ê ±£¨Kb(NH3°§H2O)£Ω1.8°¡10£≠5£ªH2SO3£∫Ka1£Ω1.5°¡10£≠2£¨Ka2£Ω1.0°¡10£≠7£ªKsp(CaSO4)£Ω7.1°¡10£≠5°£
µ⁄1≤Ω£∫”√π˝¡øµƒ≈®∞±ÀÆŒ¸ ’ SO2£¨≤¢‘⁄ø’∆¯÷–—ıªØ£ª
µ⁄2≤Ω£∫º”»Î ت“ÀÆ£¨∑¢…˙∑¥”¶ Ca2£´£´2OH£≠£´2NH4£´£´SO42£≠CaSO4°˝£´2NH3°§H2O K°£
(1)25°Ê ±£¨0.1 mol°§L£≠1(NH4)2SO3 »Ð“∫µƒ pH_____(ÃÓ°∞>°±°∞<°±ªÚ°∞£Ω°±)7°£
(2)º∆À„µ⁄2≤Ω÷–∑¥”¶µƒ K£Ω_____°£
¢Ú.ÀÆ√∫∆¯ªπ‘≠∑®
“—÷™£∫¢Ÿ2CO(g)£´SO2(g)=S(l)£´2CO2(g) ¶§H1£Ω£≠37.0 kJ°§mol£≠1
¢⁄2H2(g)£´SO2(g)=S(l)£´2H2O(g) ¶§H2£Ω£´45.4 kJ°§mol£≠1
¢€CO µƒ»º…’»»¶§H3£Ω£≠283 kJ°§mol£≠1
(3)±Ì æ“∫è¡Ú(S)µƒ»º…’»»µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™_________°£
(4)∑¥”¶¢⁄÷–£¨’˝∑¥”¶ªÓªØƒÐ E1_____(ÃÓ°∞>°±°∞<°±ªÚ°∞£Ω°±)¶§H2°£
(5)‘⁄“ª∂®—π«øœ¬£¨∑¢…˙∑¥”¶¢Ÿ°£∆Ω∫‚ ±SO2µƒ◊™ªØ¬ ¶¡(SO2)”ÎÕ∂¡œ±»µƒ±»÷µ[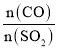 £Ωy]°¢Œ¬∂» T µƒπÿœµ»ÁÕºÀ˘ æ°£
£Ωy]°¢Œ¬∂» T µƒπÿœµ»ÁÕºÀ˘ æ°£
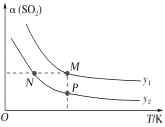
±»Ωœ∆Ω∫‚ ±COµƒ◊™ªØ¬ ¶¡(CO)£∫N_____M°£ƒÊ∑¥”¶ÀŸ¬ £∫N_____P(ÃÓ°∞>°±°∞<°±ªÚ°∞£Ω°±)°£
(6)ƒ≥Œ¬∂»œ¬£¨œÚ10L∫„»ð√б’»ð∆˜÷–≥‰»Î2molH2°¢2 molCO∫Õ2molSO2∑¢…˙∑¥”¶¢Ÿ°¢¢⁄£¨µ⁄5min ±¥ÔµΩ∆Ω∫‚£¨≤‚µ√ªÏ∫œ∆¯ÃÂ÷–CO2°¢H2O(g)µƒŒÔ÷ µƒ¡ø∑÷±Œ™1.6 mol°¢1.8 mol°£
¢Ÿ∏√Œ¬∂»œ¬£¨∑¥”¶¢⁄µƒ∆Ω∫‚≥£ ˝KŒ™_____°£
¢⁄∆‰À˚Ãıº˛≤ª±‰£¨‘⁄µ⁄ 7 min ±Àı–°»ð∆˜Ãª˝£¨SO2µƒ∆Ω∫‚≈®∂»_____(ÃÓ°∞‘ˆ¥Û°±°∞ºı–°°±ªÚ°∞≤ª±‰°±)°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø‘⁄≥£Œ¬œ¬£¨œÚ![]() »Ð“∫÷–÷µŒº”»Î
»Ð“∫÷–÷µŒº”»Î![]() »Ð“∫£¨ªÏ∫œ»Ð“∫µƒ
»Ð“∫£¨ªÏ∫œ»Ð“∫µƒ![]() ±‰ªØ«Èøˆ»ÁÕº÷–À˘ æ«˙œþ£®Ãª˝±‰ªØ∫ˆ¬‘≤ªº∆£©°£œ¬¡–– ˆ’˝»∑µƒ «£® £©
±‰ªØ«Èøˆ»ÁÕº÷–À˘ æ«˙œþ£®Ãª˝±‰ªØ∫ˆ¬‘≤ªº∆£©°£œ¬¡–– ˆ’˝»∑µƒ «£® £©
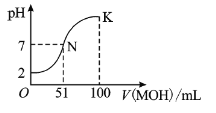
A.![]() »Ð“∫µƒ
»Ð“∫µƒ![]() B.
B.![]() µ„ ±º”ÀÆœ° ջГ∫£¨
µ„ ±º”ÀÆœ° ջГ∫£¨![]() ºı–°
ºı–°
C.‘⁄![]() µ„£¨
µ„£¨![]() D.‘⁄
D.‘⁄![]() µ„£¨
µ„£¨![]()
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø¢Ò.ªÿ¥œ¬¡–Œ £∫
£®1£©Ã˛AµƒΩ·ππºÚ ΩŒ™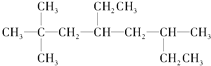 £¨”√œµÕ≥√¸√˚∑®√¸√˚Ã˛A£∫____________°£
£¨”√œµÕ≥√¸√˚∑®√¸√˚Ã˛A£∫____________°£
£®2£©ƒ≥Ã˛µƒ∑÷◊” ΩŒ™![]() £¨∫À¥≈π≤’Ò«‚∆◊Õº÷–œ‘ æ4∏ˆ∑£¨‘Ú∏√Ã˛µƒ“ª¬»¥˙ŒÔ”–_______÷÷£¨∏√Ã˛µƒΩ·ππºÚ ΩŒ™____________°£
£¨∫À¥≈π≤’Ò«‚∆◊Õº÷–œ‘ æ4∏ˆ∑£¨‘Ú∏√Ã˛µƒ“ª¬»¥˙ŒÔ”–_______÷÷£¨∏√Ã˛µƒΩ·ππºÚ ΩŒ™____________°£
£®3£©¬Èª∆Àÿ”÷≥∆ª∆ºÓ£¨ «Œ“π˙Ãÿ∂®÷–“©≤ƒ¬Èª∆÷–À˘∫¨”–µƒ“ª÷÷…˙ŒÔºÓ°£æ≠ø∆—ߺ“—–æø∑¢œ÷∆‰Ω·ππŒ™£∫ £¨œ¬¡–∏˜ŒÔ÷ £∫A.
£¨œ¬¡–∏˜ŒÔ÷ £∫A. 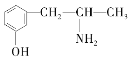 B.
B. ![]() C.
C. 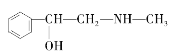 D.
D. 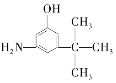 E.
E. 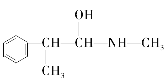
”άȪ∆Àÿª•Œ™Õ¨∑÷“Ïππõƒ «_________£®ÃÓ◊÷ƒ∏£¨œ¬Õ¨£©£¨ª•Œ™Õ¨œµŒÔµƒ «___________£®ÃÓ◊÷ƒ∏£©°£
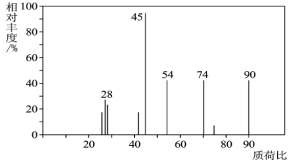
¢Ú.”–ª˙ŒÔC≥£”√”⁄ ≥∆∑––“µ°£“—÷™![]() ‘⁄◊„¡ø
‘⁄◊„¡ø![]() ÷–≥‰∑÷»º…’£¨Ω´…˙≥…µƒªÏ∫œ∆¯Ã“¿¥ŒÕ®π˝◊„¡øµƒ≈®¡ÚÀ·∫ÕºÓ Øª“£¨∑÷±‘ˆ÷ÿ
÷–≥‰∑÷»º…’£¨Ω´…˙≥…µƒªÏ∫œ∆¯Ã“¿¥ŒÕ®π˝◊„¡øµƒ≈®¡ÚÀ·∫ÕºÓ Øª“£¨∑÷±‘ˆ÷ÿ![]() ∫Õ
∫Õ![]() £¨æ≠ºÏ—È £”ý∆¯ÃÂŒ™
£¨æ≠ºÏ—È £”ý∆¯ÃÂŒ™![]() °£
°£
£®1£©C∑÷◊”µƒ÷ ∆◊Õº»ÁÕºÀ˘ 棨¥”Õº÷–ø…÷™∆‰œý∂‘∑÷◊”÷ ¡ø «________£¨‘ÚCµƒ∑÷◊” Ω «_______°£
£®2£©CƒÐ”Î![]() »Ð“∫∑¢…˙∑¥”¶£¨C“ª∂®∫¨”–µƒπŸƒÐÕ≈ «_____________°£
»Ð“∫∑¢…˙∑¥”¶£¨C“ª∂®∫¨”–µƒπŸƒÐÕ≈ «_____________°£
£®3£©C∑÷◊”µƒ∫À¥≈π≤’Ò«‚∆◊”–4∏ˆ∑£¨∑Â√ʪ˝÷Ʊ» «![]() £¨‘ÚCµƒΩ·ππºÚ Ω «________°£
£¨‘ÚCµƒΩ·ππºÚ Ω «________°£
£®4£©![]() ”Î
”Î![]() µƒ«‚—ıªØƒ∆»Ð“∫∑¥”¶£¨–˻Г∫µƒÃª˝ «_____
µƒ«‚—ıªØƒ∆»Ð“∫∑¥”¶£¨–˻Г∫µƒÃª˝ «_____![]() °£
°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø£®1£©Õ®≥£∞—≤ø™1 molƒ≥ªØ—ߺ¸À˘Œ¸ ’µƒƒÐ¡øø¥≥…∏√ªØ—ߺ¸µƒº¸ƒÐ°£º¸ƒÐµƒ¥Û–°ø…“‘∫‚¡øªØ—ߺ¸µƒ«ø»ı£¨“≤ø…”√”⁄π¿À„ªØ—ß∑¥”¶µƒ∑¥”¶»»(¶§H)£¨ªØ—ß∑¥”¶µƒ¶§Hµ»”⁄∑¥”¶÷–∂œ¡—慪ؗߺ¸µƒº¸ƒÐ÷Æ∫Õºı»•∑¥”¶÷––Œ≥…–¬ªØ—ߺ¸µƒº¸ƒÐ÷Æ∫Õ°£œ¬√Ê¡–柡À“ª–©ªØ—ߺ¸µƒº¸ƒÐ ˝æð£¨π©º∆À„ π”√°£
ªØ—ߺ¸ | Si°™O | Si°™Cl | H-H | H°™Cl | Si°™Si | Si°™C |
º¸ƒÐ/kJ°§mol£≠1 | 460 | 360 | 436 | 431 | 176 | 347 |
“—÷™£∫1molæßÃÂπË∫¨”–2molSi-Siº¸°£π§“µ…œø…“‘Õ®π˝œ¬¡–∑¥”¶÷∆»°∏þ¥øπË£∫SiCl4(g)£´2H2(g)£ΩSi(s)£´4HCl(g)£¨‘Ú∏√∑¥”¶µƒ∑¥”¶»»(¶§H)Œ™______°£
£®2£©Ãº «–Œ≥…ªØ∫œŒÔ÷÷¿ý◊Ó∂ýµƒ‘™Àÿ£¨∆‰µ•÷ º∞ªØ∫œŒÔ «»À¿ý…˙≤˙…˙ªÓµƒ÷˜“™ƒÐ‘¥ŒÔ÷ °£«Îªÿ¥œ¬¡–Œ £∫
¢Ÿ”–ª˙ŒÔMæ≠π˝Ã´—Ùπ‚π‚’’ø…◊™ªØ≥…N£¨◊™ªØπ˝≥ûÁœ¬£∫
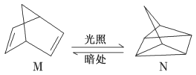 ¶§H£Ω£´88.6 kJ°§mol£≠1
¶§H£Ω£´88.6 kJ°§mol£≠1
‘ÚMµƒªØ—ß ΩŒ™_________________£¨M°¢Nœý±»£¨ΩœŒ»∂®µƒ «____________°££®ÃÓMªÚN£©
¢⁄“—÷™CH3OH(l)µƒ»º…’»»Œ™238.6 kJ°§mol£≠1£¨CH3OH(l)£´1/2O2(g)=CO2(g)£´2H2(g)°°¶§H£Ω£≠a kJ°§mol£≠1£¨‘Úa____________238.6(ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±)°£
¢€ πCl2∫ÕH2O(g)Õ®π˝◊∆»»µƒÃø≤„£¨…˙≥…HCl∫ÕCO2£¨µ±”–1 mol Cl2≤Œ”Î∑¥”¶ ± Õ∑≈≥ˆ145 kJ»»¡ø£¨–¥≥ˆ∏√∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã Ω£∫____________°£
¢Ðªº˝∫ÕµºµØ±Ì√ʵƒ±°≤„ «ƒÕ∏þŒ¬ŒÔ÷ °£Ω´ ؃´°¢¬¡∑€∫Õ∂˛—ıªØÓ—∞¥“ª∂®±»¿˝ªÏ∫œ‘⁄∏þŒ¬œ¬Ï—…’£¨À˘µ√ŒÔ÷ ø…◊˜ƒÕ∏þŒ¬≤ƒ¡œ£¨4Al(s)£´3TiO2(s)£´3C(s)=2Al2O3(s)£´3TiC(s)°°¶§H£Ω£≠1176 kJ°§mol£≠1£¨‘Ú∑¥”¶π˝≥Ã÷–£¨√ø◊™“∆1 molµÁ◊” ±∑≈≥ˆµƒ»»¡øŒ™_______°£
£®3£©“—÷™£∫
¢ŸH2O(g)£ΩH2O(l) °˜H1=°™Q1kJ/mol
¢⁄CH3OH(g)£ΩCH3OH(l) °˜H2=°™Q2kJ/mol
¢€2CH3OH(g)+3O2(g)£Ω2CO2(g)+4H2O(g) °˜H3=°™Q3kJ/mol£®Q1°¢Q2°¢Q3æ˘¥Û”⁄0£©
»Ù“™ π32g“∫èº◊¥ºÕÍ»´»º…’£¨◊Ó∫Ûª÷∏¥µΩ “Œ¬£¨∑≈≥ˆµƒ»»¡øŒ™______kJ°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–”–πÿ√Ë ˆº∞ªØ—ß”√”Ôµƒ±Ì æ∑Ω∑®’˝»∑µƒ «£® £©
A.‘≠◊”∫Àƒ⁄”–8∏ˆ÷–◊”µƒª˘Ã¨Ãº‘≠◊”º€µÁ◊”≈≈≤ºÕºŒ™£∫![]()
B.NH4FµƒµÁ◊” ΩŒ™£∫![]() £¨»˝÷÷‘™Àÿ÷–∑˙µƒµ⁄“ªµÁ¿ÎƒÐ◊Ó¥Û
£¨»˝÷÷‘™Àÿ÷–∑˙µƒµ⁄“ªµÁ¿ÎƒÐ◊Ó¥Û
C.Õ≠ Ù”⁄d«¯‘™Àÿ£¨‰Â Ù”⁄p«¯‘™Àÿ£¨∂˛’þª˘Ã¨‘≠◊”Œ¥≥…∂‘µÁ◊” ˝ƒøœýÕ¨
D.CO2∑÷◊”µƒΩ·ππ ΩŒ™£∫O=C=O£¨Ãºµƒ‘≠◊”∞Îæ∂¥Û”⁄—ıµƒ‘≠◊”∞Îæ∂
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com