
【题目】现代化学测定有机物组成及结构的分析方法较多。下列有关说法正确的是
A.元素分析仪不仅可以测出试样常见的组成元素及含量,还可以测定其分子的空间结构
B.![]()
C.通过红外线光谱图分析可以区分乙醇和乙酸乙酯
D.质谱法和紫外光谱法不属于测定有机物组成和结构的现代分析方法
科目:高中化学 来源: 题型:
【题目】己知:25℃时,CaCO3的Ksp=2.8×10-9,现将Na2CO3浓度为2×10-4mol·L-1的Na2CO3溶液与CaCl2溶液等体积混合,若要产生沉淀,则所用CaCl2溶液的浓度至少应大于
A. 2.8×10-2mol·L-1 B. 5.6×10-5mol·L-1
C. 2.8×l0-5 mol·L-1 D. 1.4×l0-5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解答下列问题:
Ⅰ.某同学做如下实验![]() 图
图![]() ,以检验反应中的能量变化。
,以检验反应中的能量变化。

(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是 ______ 热反应;该反应中 ______ 能转化成 ______ 能。
(2)(b)中温度降低,下列各图![]() 图
图![]() 所表示的反应是(b)反应的是 ______ 。
所表示的反应是(b)反应的是 ______ 。
Ⅱ.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图3所示。
(1)该反应中 ______ 是反应物,反应是 ______ 反应。
(2)反应开始到10s,用Z表示的反应速率为 ______ ![]() 。
。
(3)反应开始到10s时,Y的物质的量浓度减少了 ______ ![]() 。
。
(4)反应的化学方程式为 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组研究AgCl的溶解平衡:向10 mL 1mol/L KCl 溶液中加入1 mL 0.2 mol/LAgNO3溶液,将浑浊液均分为2份,进行如下实验:
实验序号 | 实验操作 | 实验现象 |
I | 将其中一份浑浊液过滤,向滤液中放入Mg条
| i. 滤液澄清透明,用激光照射有丁达尔现象。 ii. 放入Mg条后,立即有无色气泡产生,气体可燃,滤液中出现白色浑浊。 iii. 一段时间后开始出现棕褐色浑浊物,Mg条表面也逐渐变为棕褐色,产生气泡的速率变缓慢。 |
II | 向另一份浑浊液中放入大小相同的Mg条
| iv. 棕褐色浑浊物的量明显多于实验I,Mg条表面棕褐色更深,其他现象与ii、iii相同。 |
已知:AgOH不稳定,立即分解为Ag2O(棕褐色或棕黑色),Ag粉为黑色,AgCl、Ag2O可溶于浓氨水生成Ag(NH3)2+
(1)滤液所属分散系为________。
(2)现象ii中无色气泡产生的原因是_________(写出化学方程式)。
(3)现象iii中,导致产生气泡的速率下降的主要影响因素是________。
(4)甲认为Mg条表面的棕褐色物质中一定有Ag和Ag2O,其中生成Ag的离子方程式为____。
(5)甲设计实验检验Ag:取实验I中表面变为棕褐色的Mg条于试管中,向其中加入足量试剂a,反应结束后,继续向其中加入浓硝酸,产生棕色气体,溶液中有白色不溶物。
① 白色不溶物为_____(填化学式),棕色气体产生的原因是_____(写离子方程式)。
② 试剂a为________,加入试剂a的目的是________。
③ 该实验能证明棕褐色物质中一定有Ag的实验现象是________。
(6)甲进一步设计实验验证了Mg条表面的棕褐色物质中有Ag2O,实验方案是:取实验I中表面变为棕褐色的Mg条_________。
(7)综合上述实验,能说明存在AgCl(s) ![]() Ag+(aq) + Cl-(aq)的证据及理由有________。
Ag+(aq) + Cl-(aq)的证据及理由有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列化合物的名称或结构简式:
(1)结构简式为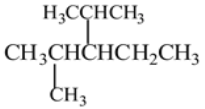 的烃可命名为:________________________________。
的烃可命名为:________________________________。
(2)结构简式为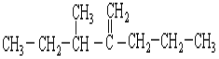 此烃名称为____________________________。
此烃名称为____________________________。
(3)2,5-二甲基-2,4-己二烯 的结构简式:__________________________。
(4)有机物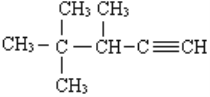 的系统名称为________________
的系统名称为________________
(5)结构简式  的烃可命名为___________________。
的烃可命名为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据合成氨反应的能量变化示意图,下列有关说法正确的是

A. N2(g)+3H2(g)=2NH3(g) △H=-2(a-b)kJ·mol-1
B. 断裂0.5moIN2 (g)和1.5molH2(g)中所有的化学键释放akJ热量
C. 2NH3 (l)= N2(g)+3H2(g) △H=2(b+c-a) kJ·mol-1
D. 若合成氨反应使用催化剂,反应放出的热量增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 、
、![]() 、
、![]() 为原子序数依次增大的短周期元素,
为原子序数依次增大的短周期元素,![]() 为地壳中含量最高的过渡金属元素,
为地壳中含量最高的过渡金属元素,![]() 与
与![]() 同主族,
同主族,![]() 与
与![]() 同周期,且
同周期,且![]() 与
与![]() 的原子序数之和为20,
的原子序数之和为20,![]() 单质能与无色无味液体
单质能与无色无味液体![]() 反应置换出
反应置换出![]() 单质,
单质,![]() 单质也能与
单质也能与![]() 反应置换出
反应置换出![]() 单质,
单质,![]() 、
、![]() 、
、![]() 均能与
均能与![]() 形成离子化合物,下列说法不正确的是( )
形成离子化合物,下列说法不正确的是( )
A. ![]() 、
、![]() 两元素的形成的化合物都为黑色固体
两元素的形成的化合物都为黑色固体
B. ![]() 、
、![]() 形成的离子化合物可能含有其价键
形成的离子化合物可能含有其价键
C. ![]() 的单质只有还原性,没有氧化性
的单质只有还原性,没有氧化性
D. 工业上可以用铝热法制取金属![]() 用于野外焊接铁轨
用于野外焊接铁轨
查看答案和解析>>
科目:高中化学 来源: 题型:
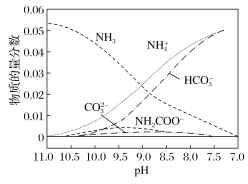
【题目】40 ℃时,在氨—水体系中不断通入![]() ,各种离子的变化趋势如图所示。下列说法不正确的是( )
,各种离子的变化趋势如图所示。下列说法不正确的是( )
A.在![]() 时,
时,![]()
B.不同pH的溶液中存在关系:![]()
C.随着![]() 的通入,
的通入,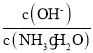 不断增大
不断增大
D.在溶液中pH不断降低的过程中,有含![]() 的中间产物生成
的中间产物生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠![]() 在溶液中会生成
在溶液中会生成![]() 、
、![]() 、
、![]() 、
、![]() 等,其中
等,其中![]() 和
和![]() 都是具有漂白作用。已知
都是具有漂白作用。已知![]() ,经测定
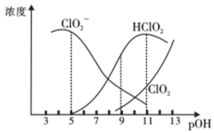
,经测定![]() 时各组分含量随pOH变化情况如图所示
时各组分含量随pOH变化情况如图所示![]() 没有画出
没有画出![]() ,此温度下,下列分析正确的是
,此温度下,下列分析正确的是![]()
A.![]() 的电离平衡常数的数值
的电离平衡常数的数值![]()
B.![]() 时,
时,![]() 部分转化成
部分转化成![]() 和
和![]() 离子的方程式为:
离子的方程式为:![]()
C.![]() 时,溶液中含氯微粒的浓度大小为:
时,溶液中含氯微粒的浓度大小为:![]()
D.同浓度的![]() 溶液和
溶液和![]() 溶液等体积混合,则混合溶液中有:
溶液等体积混合,则混合溶液中有:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com