
【题目】牛至是一种质地坚硬、树枝茂密的多年生药草,下列三种结构简式表示的物质是从牛至中提取出来的活性成分。下列有关说法正确的是

A.c分子中最多有7个碳原子共平面
B.可用溴的CCl4溶液将a、b两种物质区别开
C.a分子与HCl发生加成反应时可得到四种以上产物
D.完全燃烧1mol三种物质时消耗氧气的量:a>c>b
【答案】C
【解析】
A. c分子中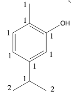 ,1类碳原子一定共平面,2类碳原子中的1个可能与1类碳原子共面,即c分子中至少有8个碳原子共面,最多有9个碳原子共面,故A错误;
,1类碳原子一定共平面,2类碳原子中的1个可能与1类碳原子共面,即c分子中至少有8个碳原子共面,最多有9个碳原子共面,故A错误;
B.a和b中均含有碳碳双键,均能与溴的四氯化碳溶液发生加成反应而使之褪色,即用溴的四氯化碳溶液不能区分a和b,故B错误;
C. 结合a的结构简式可知,a与HCl按物质的量之比1:1发生加成反应可得到四种产物,还可以按物质的量之比1:2发生加成反应,故a与HCl发生加成反应可得到四种以上产物,故C正确;
D.根据a、b、c的结构简式可确定其分子式分别为C15H24、C11H20O、C10H14O,完全燃烧1mol三种物质时消耗氧气的物质的量分别为21mol、15.5mol、13mol,即消耗氧气的量:a>b>c,故D错误;
故选C。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子,在指定环境中一定能大量共存的是
A.能使pH试纸变深蓝色的溶液中:S2、SO42、AlO2、Na+
B.加入铝粉能放出氢气的溶液中:K+、H+、I、NO3-
C.pH=3的溶液中:Al3+、K+、SO42、HCO3
D.由水电离出的[OH]=1×10![]() mol/L的溶液中:Fe2+、NH4+、ClO、Cl
mol/L的溶液中:Fe2+、NH4+、ClO、Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化石燃料是有机物的重要来源,从煤和石油获取的有机物苯和乙烯等简单有机物还是合成其他有机物的原料。如图的转化关系中,已知C能使碳酸钠溶液释放出CO2,反应①②反应机理类似且原子利用率均为 100%,请回答下列问题:
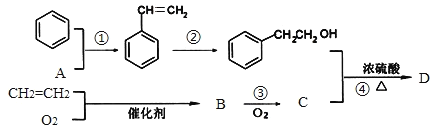
(1)有机物B中含有的官能团名称是_________________。
(2)反应①的反应类型为_________________。
(3)写出反应④的化学方程式__________________________。
(4)下列说法正确的是_________________。
A.乙烯与氧气在催化剂作用下反应也可以生成 C
B.纯C在 16.6℃ 以下呈冰状固体
C.在制备D时,D中常混有一些挥发出来的反应物,可以通过加入NaOH溶液振荡再分液的方法提纯
D.石油裂解气通过净化和分离也能得到丙烯这样的短链烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍铬钢俗称不锈钢,在日常生活中应用广泛,含有铁、铬、镍、碳等元素。
请回答下列问题:
(1)镍的基态原子核外价层电子排布式为_______________,基态Fe3+有_____种不同运动状态的电子,基态铬原子有__________个未成对电子。
(2)配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是_______________(填元素符号),铬的高价化合物可将CH3CH2OH 氧化为CH3CHO,CH3CHO 中—CH3和—CHO 中碳原子的杂化方式分别为_______________、___________________。
(3)镍能与CO 形成Ni(CO)4,常温下Ni(CO)4是无色液体,易溶于有机溶剂,推测Ni(CO)4是__________晶体,组成Ni(CO)4的三种元素电负性由大到小的顺序为_______________(填元素符号),CO 分子中π键与σ键的个数比为_______________。
(4)NiO 的立方晶体结构如图所示,则O2-填入Ni2+构成的________空隙(填“正四面体”、“正八面体”、“ 立方体”或“压扁八面体”)。NiO晶体的密度为ρg·cm-3,Ni2+和O2-的半径分别为r1pm和r2pm,阿伏加德罗常数值为NA,则该晶胞中原子的体积占晶胞体积的百分率为___________________________________。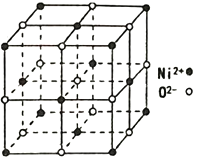
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)铅蓄电池的总反应为:Pb + PbO2 + 2H2SO4 ![]() 2PbSO4 + 2H2O,放电时,负极反应式为___________,充电时,阳极反应式为___________。
2PbSO4 + 2H2O,放电时,负极反应式为___________,充电时,阳极反应式为___________。
(2)利用如图装置,可以模拟铁的电化学防护。
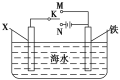
①若X为石墨,为减缓铁的腐蚀,将开关K置于N处,该电化学防护法称为___________。
②若X为锌,开关K置于M处,该电化学防护法称为__________。
(3)我国的科技人员为了消除SO2的污染,利用原电池原理,设计如图2装置用SO2和O2制备硫酸,电极A、B为多孔的材料。
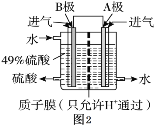
① A极的电极反应式是________。
② B极的电极反应式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳的氧化物对环境的影响较大,CO是燃煤工业生产中的大气污染物,CO2则促进了地球的温室效应。给地球生命带来了极大的威胁。
(1)已知:①甲醇的燃烧热△H=-726.4kJ·mol-1
②H2(g)+ ![]() O2(g)=H2O(l) △H=-285.8kJ·mol-1。
O2(g)=H2O(l) △H=-285.8kJ·mol-1。
则二氧化碳和氢气合成液态甲醇,生成液态水的热化学方程式为_____________________________。
(2)二氧化碳合成CH3OH 的热化学方程式为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1,过程中会产生副反应:CO2(g)+H2(g)
CH3OH(g)+H2O(g)△H1,过程中会产生副反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)△H2。图1是合成甲醇反应中温度对CH3OH、CO的产率影响曲线图,△H2________0(填“>”或“<”)。增大反应体系的压强,合成甲醇的反应速率___________(填“增大”“减小”或“ 不变”),副反应的化学平衡________(填“向正反应方向”“向逆反应方向”或“不”)移动。
CO(g)+H2O(g)△H2。图1是合成甲醇反应中温度对CH3OH、CO的产率影响曲线图,△H2________0(填“>”或“<”)。增大反应体系的压强,合成甲醇的反应速率___________(填“增大”“减小”或“ 不变”),副反应的化学平衡________(填“向正反应方向”“向逆反应方向”或“不”)移动。
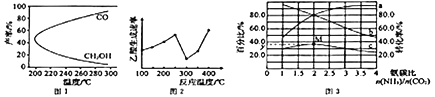
(3)以某些过渡金属氧化物作催化剂,二氧化碳与甲烷可转化为乙酸:CO2(g) +CH4(g)![]() CH3COOH(g) △H=+36.0kJ·mol-1。不同温度下,乙酸的生成速率变化曲线如图2。结合反应速率,使用催化剂的最佳温度是________℃,欲提高CH4的转化率,请提供一种可行的措施:____________________________。
CH3COOH(g) △H=+36.0kJ·mol-1。不同温度下,乙酸的生成速率变化曲线如图2。结合反应速率,使用催化剂的最佳温度是________℃,欲提高CH4的转化率,请提供一种可行的措施:____________________________。
(4)一定条件下,CO2 与NH3 可合成尿素[CO(NH2)2]:CO2(g)+2NH3(g)![]() CO(NH2)2(g)+H2O(g)△H。某温度下。在容积为1L的恒容密闭容器中,加入一定氨碳比
CO(NH2)2(g)+H2O(g)△H。某温度下。在容积为1L的恒容密闭容器中,加入一定氨碳比![]() 的3molCO2 和NH3的混合气体。图3是有关量的变化曲线,其中表示NH3转化率的是曲线________(填“a”或“b”),曲线c 表示尿素在平衡体系中的体积分数变化曲线,则M点的平衡常数K=________,y=________。
的3molCO2 和NH3的混合气体。图3是有关量的变化曲线,其中表示NH3转化率的是曲线________(填“a”或“b”),曲线c 表示尿素在平衡体系中的体积分数变化曲线,则M点的平衡常数K=________,y=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
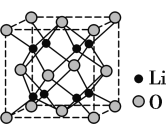
【题目】(1)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为0.466 5 nm,阿伏加德罗常数的值为NA,则Li2O的密度为__________ g·cm-3(列出计算式)。
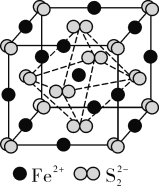
(2)FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为________g·cm-3;晶胞中Fe2+位于S![]() 所形成的正八面体的体心,该正八面体的边长为____nm。
所形成的正八面体的体心,该正八面体的边长为____nm。
(3)我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________。
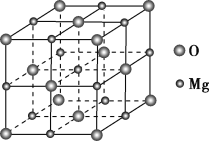
(4)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a′=0.448 nm,则r(Mn2+)为____________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题。
(1)氮、磷、砷的电负性的大小关系是 ,砷原子M层电子排布式为 。
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为 ,该化学键能够形成的原因是 。
(3)已知:
CH4 | SiH4 | NH3 | PH3 | |
沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
分解温度(K) | 873 | 773 | 1073 | 713.2 |
分析上表中四种物质的相关数据,请回答:
① CH4和SiH4比较,沸点高低的原因是 。
② NH3和PH3比较,分解温度高低的原因是 。
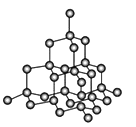
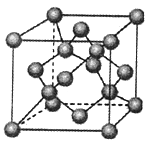
(4)金刚石是原子晶体,含有的最小环是六元环(如右边图),每个碳原子连接 个六元环,如左边图是金刚石的晶胞,若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,碳原子在晶胞中的空间占有率 (不要求计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1L0.3mol L1HA溶液与0.1molNaOH固体混合,使之充分反应得到溶液(a)。然后向该溶液中通入HCl或加入NaOH固体(忽略体积和温度变化),溶液pH随通(加)入物质的量的变化如图。下列叙述错误的是

A. HA是一种弱酸
B. 向a点对应溶液中通入HCl,充分反应后,c(H+)/c(HA)增大
C. b点对应溶液中:c(Na+)=c(Cl-)>c(HA)>c(H+)>c(OH-)
D. c点对应溶液中:c(Na+)=c(A-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com