
【题目】下列常用危险化学药品与对应的分类正确的是( )
①酒精——剧毒品 ②浓硫酸——腐蚀品 ③汽油——易燃品 ④液氯——放射性物品 ⑤高锰酸钾——氧化剂 ⑥黑火药——爆炸品
A.②③④⑥B.①②⑤C.①④⑤D.②③⑤⑥
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组测定某Fe2(SO4)3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:
①称取a g样品,置于烧杯中;
②加入50 mL 1.0 mol/L稀硫酸和一定量的蒸馏水,使样品溶解,然后准确配制成250.0 mL溶液;
③量取25.0 mL步骤②中配得的溶液,置于烧杯中,加入适量氯水,使反应完全;
④加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤,洗涤沉淀;将沉淀转移到某容器内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;
⑥……
请根据上面叙述,回答:
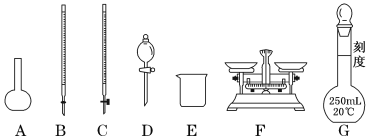
(1)上图所示仪器中,步骤①②③中必须用到的仪器有E和___________(填字母)。
(2)步骤②中:配制50 mL 1.0 mol/L稀H2SO4,需要用量筒量取98%(密度1.84 g/cm3)的浓H2SO4体积为________ mL。
(3)样品中的杂质Fe2+有较强的还原性,完成并配平下列反应的离子方程式
____Fe2++ ClO2+ === Fe3++ Cl-+ H2O
从理论上分析,上述实验中若将氯水改为ClO2时,对实验结果的影响是__________(填“偏大”“偏小”或“不影响”),等物质的量ClO2与Cl2的氧化效率之比为__________。
(4)若步骤⑤不在干燥器中冷却,则测定的铁元素的质量分数会________(填“偏大”“偏小”或“不影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的说法正确的是( )
A. 钠是银白色金属、密度比水略大 B. 钠着火时,可用水灭火
C. 金属钠在空气中燃烧,生成氧化钠 D. 通常情况下,钠的熔点略低于水的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为_____________________________。
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为____________________________ 。
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为___________________。相同状况下,能量较低的是_____________。
(4)③C(s)+ ![]() O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为____。写出CO燃烧的热化学方程式__________。
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为____。写出CO燃烧的热化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe@Fe2O3纳米线是一种新型铁基材料,在催化、生物医药、环境科学等领域具有广阔应用前景。某研究小组以赤泥(铝土矿提取氧化铝过程中产生的固体废弃物,含SiO2、Fe2O3、Al2O3)为原料,设计下列流程制备Fe@Fe2O3纳米线并探究其在水处理中的应用。
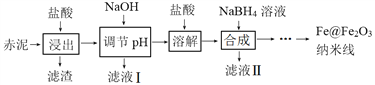
回答下列问题:
(1)“浸出”实验中,盐酸起始浓度对铁、铝浸出率的影响如图所示:
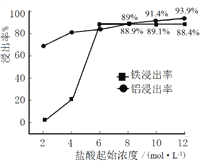
①盐酸的合适浓度为______________。
②盐酸起始浓度为2 mol·L﹣1时,铁的浸出率很低,原因是______________。
(2)已知:25℃时,Al(OH)3(s)![]() AlO2-+ H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为______________(设调节pH过程中溶液体积不变)。
AlO2-+ H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为______________(设调节pH过程中溶液体积不变)。
(3)Fe@Fe2O3纳米线为壳层结构(核是Fe、壳是Fe2O3),壳是由中心铁核在合成过程中被氧化而形成。
①“合成”时滴加NaBH4溶液过程中伴有气泡产生,滤液Ⅱ中含B(OH)3,合成铁核的离子方程式为____________________________。
②“合成”后,经过滤、______________、______________获得Fe@Fe2O3纳米线。
(4)Fe@Fe2O3纳米线去除水体中Cr2O72-的机理是,纳米线将Cr2O72-吸附在表面并还原。在“无氧”和“有氧”条件下将纳米线分别置于两份相同的水体中,80 min后回收该纳米线,测得其表面元素的原子个数比如下表:

①在水体中Fe@Fe2O3纳米线形成的分散系是____________________________。
②样本2的实验条件是______________(填“有氧”或“无氧”)。
③已知水体中检测不到Cr(Ⅲ),样本1中Fe@Fe2O3纳米线的表面Cr(Ⅵ)的去除率为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要配制0.2 mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称量的NaCl的质量分别是( )
A.1000 mL,l1.7gB.950mL,11.1 gC.500mL,11.7gD.100mL,11.7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.6 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.15mol·L-1·s-1
③2s时物质A的转化率为30%
④2s时物质B的浓度为0.3 mol·L-1
其中正确的是
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是( )
A.MnO4-,K+,Na+,NO3-B.Na+,K+,HCO3-,Cl-
C.Ba2+,K+,S2-,SO42-D.Na+,NH4+,Cl-,SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了①~⑥六种元素在周期表中的位置:
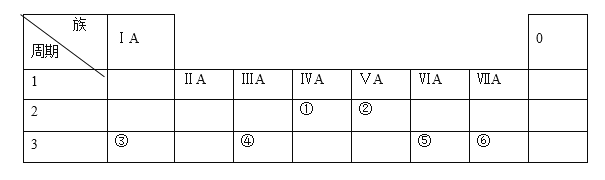
请按要求回答下列问题。
(1)元素①的元素符号是________。 元素②的单质电子式是_______。元素⑤的原子结构示意图是_______。
(2)③和⑥形成的化合物中所含化学键类型_______。
(3)HF沸点比⑥氢化物的沸点_____(高或低),原因是________。
(4)这六种元素中,位于第三周期且原子半径最小的是(填元素符号)________。
(5)这六种元素的最高价氧化物中,属于两性氧化物的元素是(填元素符号)___________。
(6)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为_________________。向上述反应后的溶液中再加入元素④的单质,发生反应的化学方程式为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com