
【题目】下表列出了①~⑥六种元素在周期表中的位置:
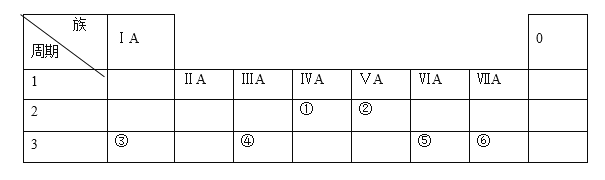
请按要求回答下列问题。
(1)元素①的元素符号是________。 元素②的单质电子式是_______。元素⑤的原子结构示意图是_______。
(2)③和⑥形成的化合物中所含化学键类型_______。
(3)HF沸点比⑥氢化物的沸点_____(高或低),原因是________。
(4)这六种元素中,位于第三周期且原子半径最小的是(填元素符号)________。
(5)这六种元素的最高价氧化物中,属于两性氧化物的元素是(填元素符号)___________。
(6)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为_________________。向上述反应后的溶液中再加入元素④的单质,发生反应的化学方程式为________________。
【答案】C ![]()
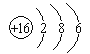 离子键 高 HF分子间存在氢键 Cl Al 2Na+2H2O=2Na++2OH-+H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
离子键 高 HF分子间存在氢键 Cl Al 2Na+2H2O=2Na++2OH-+H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
【解析】
由元素在周期表中的位置可知,①为C,②为N,③为Na,④为Al,⑤为S,⑥为Cl,然后结合化学用语及元素的单质、化合物的性质来解答。
由元素在周期表中的位置可知,①为C,②为N,③为Na,④为Al,⑤为S,⑥为Cl。
(1)①号元素位于第二周期第ⅣA族,为C元素,元素②为N,单质为N2,N最外层有5个电子,形成稳定结构N和N之间形成3对共用电子对,电子式为![]() ;元素⑤为S,16号元素,各电子层的电子数为2、8、6,原子结构示意图为
;元素⑤为S,16号元素,各电子层的电子数为2、8、6,原子结构示意图为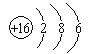 ;
;
(2)③和⑥分别是Na和Cl,活泼金属和活泼非金属形成的化合物为离子化合物;
(3)HF的沸点比⑥的氢化物HCl的沸点高,由于HF分子间可以形成氢键;
(4)同周期元素原子的半径,从左到右原子半径越来越小,则半径最小的是元素⑥,Cl元素;
(5)元素④是Al,其氧化物Al2O3可以与酸又可以与碱反应,属于两性氧化物;
(6) Na和水反应生成NaOH和H2,离子方程式为2Na+2H2O=2Na++2OH-+H2↑。在所得溶液中,加入金属Al,得到偏铝酸钠和氢气,化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列常用危险化学药品与对应的分类正确的是( )
①酒精——剧毒品 ②浓硫酸——腐蚀品 ③汽油——易燃品 ④液氯——放射性物品 ⑤高锰酸钾——氧化剂 ⑥黑火药——爆炸品
A.②③④⑥B.①②⑤C.①④⑤D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图。依图回答:

(1)该反应的化学方程式可表示为________。
(2)反应起始至t min(设t=5),Y的平均反应速率是________。
(3)反应至t min时,Z所占体积(标准状况下)________。
(4)在t min时,该反应达到了_____状态,下列可判断反应已达到该状态的是______(填字母)。
A X、Y、Z的反应速率相等 B X、Y的反应速率比为2:3
C 混合气体的密度不变 D 生成1molZ的同时生成2molX
E X、Y、Z物质的量之比等于系数比 F 混合气体的总压强不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是 ( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④B.③④⑥⑦⑧C.③⑤⑥⑦⑧D.⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量的Zn与一定量的盐酸反应,由于反应速率太快,为减慢反应速率,但又不影响生成氢气的总量,可向盐酸中加入适量的物质是 ( )
A.NaOH固体 B.CH3COONa固体 C.NaCl晶体 D .Na2CO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途正确且具有对应关系的是
A.SO2具有氧化性,可用于漂白纸浆
B.NH4HCO3受热易分解,可用作氮肥
C.金属钠具有还原性,可从硫酸铜溶液中置换出铜
D.Al2O3熔点高,可用作耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学购买了一瓶“84消毒液”,包装说明如下,请根据以上信息和相关知识判断,下列分析不正确的是

A. 该“84消毒液”的物质的量浓度约为4.0 mol·L-1
B. 一瓶该“84消毒液”敞口放置一段时间后浓度会变小
C. 取100 mL该“84消毒液”稀释100倍,稀释后溶液中c(Na+)约为0.04mol·L-1
D. 参阅该“84消毒液”的配方,欲用NaClO固体配制含25%NaClO的消毒液480mL,需要称量的NaClO固体质量为143g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度和压强下,对反应CO2(g)+H2(g) ![]() CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
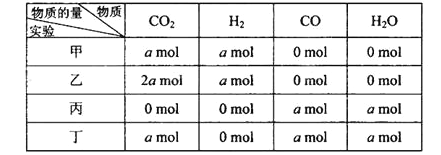
上述四种情况达到平衡后,n(CO)的大小顺序是( )
A. 乙=丁>丙=甲 B. 乙>丁>甲>丙
C. 丁>乙>丙=甲 D. 丁>丙>乙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。
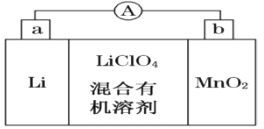
回答下列问题:
(1)外电路的电流方向是由______极流向______极。(填字母)
(2)电池正极反应式为 _____________________。
(3)MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,反应的化学方程式为 _________________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为__________。
(4)电解Na2CO3溶液,原理如图所示。
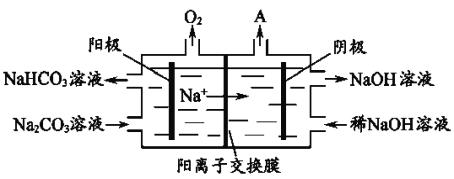
阳极的电极反应式为__________________,阴极产生的物质A的化学式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com