
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是
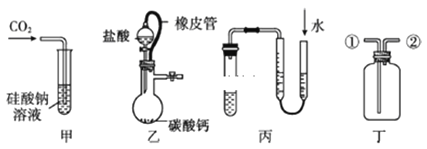
A. 甲装置:可用来证明碳酸的酸性比硅酸强
B. 乙装置:橡皮管的作用是平衡气压,使液体顺利流下
C. 丙装置:用图示的方法不能检查此装置的气密性
D. 丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气
【答案】C
【解析】
碳酸的酸性大于硅酸,根据强酸制取弱酸判断;橡皮管的作用是能让分液漏斗和蒸馏烧瓶间压强平衡;利用压强差检验装置的气密性;根据气体的溶解性及密度确定收集方法。
二氧化碳和水反应生成碳酸,碳酸酸性大于硅酸,所以二氧化碳和硅酸钠溶液反应生成不溶性硅酸,则该装置能证明碳的非金属性比硅强,A正确;分液漏斗和蒸馏烧瓶间用橡皮管连接,可使它们之间气体流通,保证了分液漏斗和蒸馏烧瓶间压强平衡,能使水顺利流下,B正确;如果装置的气密性良好,甲、乙两侧水面高度不同,否则水面相同,所以能检验装置的气密性,C错误;二氧化碳的密度大于空气、氢气的密度小于空气,所以氢气采用向下排空气法收集、二氧化碳采用向上排空气法收集,D正确。
故选C。


科目:高中化学 来源: 题型:
【题目】某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如下图所示(气体体积数据已换算成标准状况下的体积)。关于该固体混合物,下列说法正确的是( )

A. 一定含有MgCl2和FeCl2
B. 一定不含FeCl2,可能含有MgCl2和AlCl3
C. 一定含有Al,其质量为4.5 g
D. 一定含有(NH4)2SO4和MgCl2,且物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列微粒的电子式:NaOH__________;CS2_________;Na2S_________NH3__________;NH4H________;
(2)用电子式表示下列物质的形成过程MgCl2______________________
(3)现有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl①只由离子键构成的物质是________________。
②只由极性键构成的物质是_______________。
③由极性键和非极性键构成的物质是________________。
④由离子键和极性键构成的物质是________________。
⑤由离子键和非极性键构成的物质是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期。下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物。下列分析正确的是
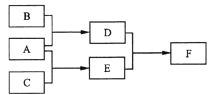
A. Y的氢化物在常温下是液体
B. 与Y同周期氢化物中D最稳定
C. Z的含氧酸均为强酸
D. F含离子键和共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物H ( )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:

已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels-Alder反应:![]() 。
。
(1)生成A的反应类型是_______。D的名称是_______。F中所含官能团的名称是_______。
(2)B的结构简式是_______;“B→C”的反应中,除C外,另外一种产物是_______。
(3)D+G→H的化学方程式是______。
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有______种,其中核磁共振氢谱有4组峰,且峰面积比为1:2:2:3的结构简式为______(任写一种)。
(5)已知:乙炔与1,3-丁二烯也能发生Diels-Alder反应。请以1,3-丁二烯和乙炔为原料,选用必要的无机试剂合成 ,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途。下列关于铝的说法正确的是
A.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B.常温下不与任何酸、碱反应
C.铝元素在地壳中的含量高,储量丰富,仅次于铁
D.工业上通常用钠与铝盐溶液反应来制备铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.焰色反应为黄色,说明该物质中肯定含有钠元素
B.某物质的焰色反应不显紫色(未透过蓝色钴玻璃),说明该物质中肯定没有钾元素
C.焰色反应不能用于物质的鉴别
D.焰色反应是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)根据计算用托盘天平需称取氯化钠_________ g;
(2)配制溶液时,除需要烧杯、玻璃棒外,还必须用到的玻璃仪器有 ;
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.定容.正确的操作顺序是 ;
(4)下列操作结果使溶液物质的量浓度偏低的是___ ______ ;
A.没有将洗涤液转入容量瓶中 |
B.加水定容时,水的量超过了刻度线 |
C.定容时,俯视容量瓶的刻度线 |
D.容量瓶洗涤后,未经干燥处理 |
(5)取出该NaCl溶液10mL加水稀释到200mL,稀释后溶液中NaCl的物质的量浓度是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)如图中的A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。请填空:

(1)电源A的a为____极。
(2)滤纸B上发生的总反应方程式为___________________。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为_____________,电极f上发生的反应为____,槽中盛放的电镀液可以是____(只要求填一种电解质溶液)。
(Ⅱ)电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极)。
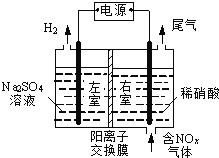
若用NO2气体进行模拟电解法吸收实验。
①写出电解时NO2发生反应的电极反应式_____________________。
②若有标准状况下2.24LNO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为_____mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com