
【题目】(1)写出下列微粒的电子式:NaOH__________;CS2_________;Na2S_________NH3__________;NH4H________;
(2)用电子式表示下列物质的形成过程MgCl2______________________
(3)现有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl①只由离子键构成的物质是________________。
②只由极性键构成的物质是_______________。
③由极性键和非极性键构成的物质是________________。
④由离子键和极性键构成的物质是________________。
⑤由离子键和非极性键构成的物质是________________。
【答案】![]()
![]()
![]()
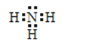
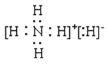
![]() ⑥ ④ ⑤ ③⑦ ②
⑥ ④ ⑤ ③⑦ ②
【解析】
本题考查的是离子化合物的结构特征与性质、共价键的形成及共价键的主要类型、 极性键和非极性键。活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,据此分析解答。
(1)NaOH中钠离子与氢氧根离子通过离子键结合,氢氧根离子中的氢原子和氧原子通过共价键结合,电子式为![]() ;CS2中的硫原子和氧原子通过共用电子对相结合共形成了四对共用电子对,电子式为
;CS2中的硫原子和氧原子通过共用电子对相结合共形成了四对共用电子对,电子式为![]() ;Na2S中的钠离子和硫离子通过离子键结合,电子式为
;Na2S中的钠离子和硫离子通过离子键结合,电子式为![]() ;NH3中的氮原子和氢原子通过共用电子对结合共形成了三对共用电子对,电子式为
;NH3中的氮原子和氢原子通过共用电子对结合共形成了三对共用电子对,电子式为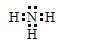 ;NH4H中的铵根离子和H-通过离子键相结合,铵根离子中的氮原子和氢原子通过共价键相结合,电子式为
;NH4H中的铵根离子和H-通过离子键相结合,铵根离子中的氮原子和氢原子通过共价键相结合,电子式为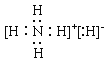 。本小题答案为:
。本小题答案为:![]() ;
;![]() ;
;![]() ;
;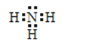 ;
;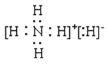 。
。
(2)MgCl2中的镁离子和氯离子通过离子键相结合,形成过程为![]() 。本小题答案为:
。本小题答案为:![]() 。
。
(3)①Cl2中ClCl原子之间只存在非极性键,为单质;②Na2O2中钠离子和过氧根离子之间存在离子键、OO原子之间存在非极性键,为离子化合物;③NaOH中钠离子和氢氧根离子之间存在离子键、OH原子之间存在极性键,为离子化合物;④HCl分子中HCl原子之间只存在极性键,为共价化合物;⑤H2O2中HO之间存在极性键、OO原子之间存在非极性键,为共价化合物;⑥MgF2中镁离子和氟离子之间只存在离子键,为离子化合物;⑦NH4Cl中铵根离子和氯离子之间存在离子键、NH原子之间存在极性共价键,为离子化合物;
①通过以上分析知,只含离子键的是⑥。本小题答案为⑥。
②只有极性键构成的物质是④。本小题答案为④。
③由极性键和非极性键构成的物质是⑤。本小题答案为⑤。
④由离子键和极性键构成的物质是③⑦,本小题答案为③⑦。
⑤由离子键和非极性键构成的物质是②,本小题答案为②。


科目:高中化学 来源: 题型:
【题目】某芳香烃X(相对分子貭量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种高分子。

回答下列问题:
(1)B的名称是________,物质Y是乙酸吗_____(填“是”或 “不是”)?反应⑧属于____反应。H的含N官能团的名称是______。
(2)反应⑥、⑦两步能否互换____(填“能”或“不能”),理由是__________。
(3)上图中反应②的化学方程式是__________。
(4)比 相对分子质量大14的同系物M的同分异构体中,写出能同时满足以下条件的M(不考虑立体异构):_____________。
相对分子质量大14的同系物M的同分异构体中,写出能同时满足以下条件的M(不考虑立体异构):_____________。
①苯环上的一氯代物有2种,②能发生水解反应,③与FeCl3溶液能够发生显色反应。
(5)请用合成反应流程图表示出由![]() 和其他无机物合成
和其他无机物合成![]() 最合理的方案(不用写条件)__________。
最合理的方案(不用写条件)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,相关示意图错误的是( )
A | B | C | D |
将二氧化硫通入到一定量氯水中 | 将NaHCO3溶液滴入到一定量Ba(OH)2溶液中 | 将铜粉加入到一定量浓硝酸中 | 将铁粉加入到一定量氯化铁溶液中 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】党的十九大强调树立“社会主义生态文明观”。下列做法不应该提倡的是( )
A.研发可降解高分子材料,缓解白色污染问题
B.扩大铅蓄电池、含汞干电池的生产,满足消费需求
C.采用碳捕集和封存技术,逐步实现二氧化碳零排放
D.大力发展太阳能、风能等清洁能源,减少对化石燃料的依赖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中正确的是( )
A. 钠原子的结构示意图: 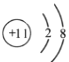
B. 过氧化钠的电子式:![]()
C. 碳酸氢钠的电离方程式:NaHCO3= Na++ H+ + CO32-
D. 中子数为12的钠的核素符号为: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)是无色离子晶体,遇高热或剧烈震动能发生强烈爆炸,快速分解成钠单质和氮气,是汽车安全气囊中的成分之一。下列有关说法正确的是
A. NaN3中只含有离子键
B. 1 mol NaN3完全分解最多可以产生33.6L N2
C. 当有4.2g N2生成时,转移电子数约为6.02×1022
D. 常温下,NaN3化学性质稳定,包装盒上无需特别说明注意事项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫酸铝溶液为原料之一,在实验室里制取少量氢氧化铝,并且容易分离,最好向溶液中加入是( )
A.氢氧化钠溶液
B.氢氧化钡溶液
C.稀盐酸
D.氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是
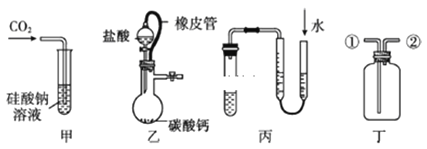
A. 甲装置:可用来证明碳酸的酸性比硅酸强
B. 乙装置:橡皮管的作用是平衡气压,使液体顺利流下
C. 丙装置:用图示的方法不能检查此装置的气密性
D. 丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于自发进行的变化的是( )
A.红墨水加到蒸馏水中使整杯水变红B.冰在室温下融化成水
C.NaHCO3受热转化为Na2CO3 D.铁在潮湿的空气中生锈
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com