
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子结构示意图为________。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是________(填序号)。
a.Cl2、Br2、I2的熔点
b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性
d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液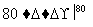 NaClO3溶液
NaClO3溶液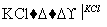 KClO3晶体①完成Ⅰ中反应的总化学方程式:
KClO3晶体①完成Ⅰ中反应的总化学方程式:
 NaCl+
NaCl+ H2O===
H2O=== NaClO3+
NaClO3+ ________。
________。
②Ⅱ中转化的基本反应类型是________________,该反应过程能析出KClO3晶体而无其他晶体析出的原因是____________________________________。
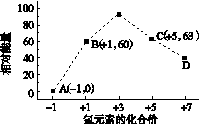
(4)一定条件下,在水溶液中1 mol Cl-、ClO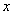 (x=1,2,3,4)的能量(kJ)相对大小如右图所示。
(x=1,2,3,4)的能量(kJ)相对大小如右图所示。
①D是________(填离子符号)。
②B→A+C反应的热化学方程式为________________(用离子符号表示)。
(1)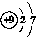 (2)b、c (3)①
(2)b、c (3)① NaCl+
NaCl+ H2O===
H2O=== NaClO3+
NaClO3+ H2↑
H2↑
②复分解反应
室温下,氯酸钾在水中的溶解度明显小于其他晶体
(4)①ClO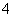 ②3ClO-(aq)===ClO
②3ClO-(aq)===ClO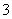 (aq)+2Cl-(aq) ΔH=-117 kJ·mol-1
(aq)+2Cl-(aq) ΔH=-117 kJ·mol-1
[解析] (1)与氯元素同族的短周期元素为F,F的原子结构示意图为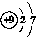 。
。
(2)Cl2、Br2、I2都是分子晶体,其熔点受分子间作用力影响,与非金属性无关,a项错误;单质的氧化性越强则其元素的非金属性越强,b项正确;非金属性强弱可用气态氢化物的稳定性判断,c项正确;卤素氢化物的酸性可用来判断氢原子与卤素原子形成的共价键强弱,d项错误。(3)①根据氧化还原反应的化合价升降法配平可得:NaCl+3H2O===NaClO3+3H2↑;②步骤Ⅱ发生的反应NaClO3+KCl===KClO3↓+NaCl↑,各元素的化合价没有变化,则该反应属于复分解反应。在室温下,氯酸钾在水中的溶解度小于其他晶体,则有氯酸钾晶体析出而无其他晶体析出。(4)①从图可知D中氯元素的化合价为+7,则D为ClO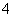 ;②从图中可知:A为Cl-,B为ClO-,C为ClO
;②从图中可知:A为Cl-,B为ClO-,C为ClO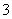 , B→A+C的氧化还原反应用升降法配平可得该热化学方程式为3ClO-(aq)=== ClO
, B→A+C的氧化还原反应用升降法配平可得该热化学方程式为3ClO-(aq)=== ClO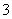 (aq)+ 2Cl-(aq) ΔH=(63 kJ/mol+2×0)-3×60 kJ/mol=-117 kJ/mol。
(aq)+ 2Cl-(aq) ΔH=(63 kJ/mol+2×0)-3×60 kJ/mol=-117 kJ/mol。


科目:高中化学 来源: 题型:
800℃时在2L密闭容器内反应:2NO(g)+O2(g) 2NO2(g)体系中,
2NO2(g)体系中,
n(NO)随时间的变化如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)达平衡时NO的转化率_________________。
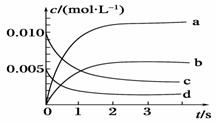 (2)下图中表示NO2的变化的曲线是________, 用O2表示从0=2s内该反应的平均速率v(O2)=_____。
(2)下图中表示NO2的变化的曲线是________, 用O2表示从0=2s内该反应的平均速率v(O2)=_____。
(3)能说明该反应一定达到平衡状态的是_ _
a.v(NO2)=2v(O2) b.容器内颜色保持不变
c.2V逆 (NO)=v正(O2) d.容器内压强保持不变
(4)能增大该反应的反应速率是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
燃料电池是燃料(如H2、CO、CH4等)跟氧气或空气起反应,将化学能转变为电能的装置,电解液为强碱溶液。下列关于甲烷燃料电池的说法正确的是( )
A. 负极反应为CH4+10OH-→CO32-+7H2O+8e- B. 负极反应为O2+2H2O+4e-→4OH-
C. 随着放电进行,溶液中的阳离子向负极移动 D. 随着放电进行,溶液的PH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在1.01×105 Pa下测得某些烷烃的沸点见下表,下列选项正确的是( )

A.在标准状况下,新戊烷是气体
B.在1.01×105 Pa、20℃,C5H12都是液体
C.烷烃随碳原子数的增加,沸点降低
D.C5H12随支链增加,沸点降低
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是( )
A.原子最外层电子数:X>Y>Z
B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z-
D.原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是( )
A.原子最外层电子数:X>Y>Z
B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z-
D.原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式:__________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为__________,其水溶液与F单质反应的化学方程式为____________________________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显______色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的性质比较中不正确的是( )
A.热稳定性:SiH4>PH3>H2S
B.酸性:HClO4>H2SO4>H3PO4
C.碱性:NaOH>Mg(OH)2>Al(OH)3
D.氧化性:F2>Cl2>Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阿伏伽德罗常数说法正确的是
A.含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA
B.标况下,22.4L四氯化碳所含分子数大于NA
C.0.1mol/L 的AgNO3溶液中,阳离子所带正电荷数目为0.1NA
D. 0.2mol/L的 H2SO4的硫酸溶液与0.1mol/L的 H2SO4的硫酸溶液等质量混合溶液浓度大于0.15mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com