
【题目】某溶液可能含有Cl﹣、SO42﹣、CO32﹣、NH4+、Fe3+、Fe2+和Na+ . 某同学为了确认其成分,取部分溶液,设计并完成了如图实验:下列说法正确的是( ) 
A.原溶液中c(Fe3+)=0.2molL﹣1
B.SO42﹣、NH4+、Na+一定存在,CO32﹣一定不存在
C.要确定原溶液中是否含有Fe2+ , 其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+
D.溶液中至少有4种离子存在,其中Cl﹣一定存在,且c(Cl﹣)≥0.2molL﹣1
【答案】D
【解析】解:A.根据以上分析可知,原溶液中含有0.02mol铁元素,无法判断存在的是铁离子或者亚铁离子,故A错误;
B.根据以上分析可知,原溶液中一定存在SO42﹣、NH4+、Cl﹣ , 只是存在Fe3+、Fe2+中的一种,其离子的物质的量为0.02mol,一定不存在CO32﹣;由于第一步中加入了氢氧化钠溶液,引进了钠离子,无法确定原溶液中是否含有钠离子,故B错误;
C.检验亚铁离子时,取少量原溶液于试管中,加KSCN溶液,此时溶液现象必须是无色,然后再加入适量氯水,溶液呈血红色,则含有Fe2+ , 否则如果加入硫氰化钾溶液后显示红色,则无法证明原溶液中是否含有亚铁离子,故C错误;
D.根据以上分析,原溶液中一定存在0.02molNH4+ , 0.02molSO42﹣ , 0.02molFe3+、Fe2+中的一种,当铁元素全部为亚铁离子时,阳离子所带电荷的物质的量最小,所以正电荷物质的量最少为:0.02mol×2+0.02mol=0.06mol,而负电荷的物质的量为:0.02mol×2=0.04mol,根据溶液电中性可知,原溶液中一定存在Cl﹣ , 且c(Cl﹣)≥ ![]() =0.2 molL﹣1 , 故D正确.
=0.2 molL﹣1 , 故D正确.
故选D.


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组,欲在常温常压下,用一定质量的铜镁合金与足量稀盐酸反应,利用图装置,测定样品中铜的质量分数.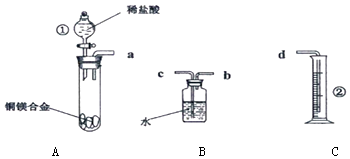
(1)实验反应原理:写出A中发生反应的离子方程式 .
(2)仪器识别:写出上图中仪器①的名称 .
(3)实验中,该兴趣小组同学测得以下数据
a.反应前样品铜镁合金的质量,记为m1 g
b.反应结束后,经过处理后的残余固体的质量,记为m2 g
c.经过一系列正确的操作后,读取量筒中的水的体积,记为V mL
d.查阅资料,常温常压下,H2的密度为ρ g/L
四位同学分成甲、乙两个小组,甲组同学利用重量法为思路,请合理选择以上数据,列式求铜的质量分数:×100%;乙组同学利用排水法测量气体体积为思路,请合理选择以上数据,列式求铜的质量分数:×100%
(4)误差分析环节中指导教师提出,甲、乙两组同学的思路中,会有很多因素导致测得的铜的质量分数出现误差,现将可能导致误差的因素罗列如下,回答相关问题:
a.读取量筒中水的体积时,未等装置中气体恢复至室温
b.未考虑B、C装置间连接导管中残留的水
c.未对反应后剩余的残余物进行洗涤
d.未对反应中挥发出的HCl气体进行除杂处理
导致铜的质量分数大于理论值的原因可能是(填符号)
导致铜的质量分数小于理论值的原因可能是(填符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做如表实验:下列说法正确的是( )
装 |
|
|
现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
A.“电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀
B.铁片Ⅳ的电极反应式可能为Fe﹣3e﹣=Fe3+
C.用K3Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断装置的正、负极
D.铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,所以二者的腐蚀速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期表和周期律的说法中,正确的是
A. 元素周期表有7个主族,7个副族,1个0族,1个VIII族,共16纵行
B. F是原子半径最小的非金属元素
C. 短周期中,Cl的非金属性最强
D. 原子半径Na>O,离子半径Na+<O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中只可能含有K+、Ag+、Ba2+、Cu2+、Cl-、OH-、CO ![]() 、SO
、SO ![]() 中的一种或几种,对其进行如下实验操作:( )
中的一种或几种,对其进行如下实验操作:( )
⑴取少量溶液,滴加无色酚酞试液,酚酞变红;
⑵另取少量溶液,加入足量BaCl2溶液,产生白色沉淀;
⑶向(2)所得混合物中加足量盐酸,沉淀部分溶解,并有无色气体生成;
⑷将(3)所得混合物过滤,向滤液中加入AgNO3溶液,有白色沉淀生成。
下列对该溶液的说法正确的是
A.一定含有OH-、CO ![]() 、SO
、SO ![]() 、Cl-
、Cl-
B.可能含有K+、Cl-
C.一定不含有Ag+、Ba2+、Cu2+
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化铝(AlON)属原子晶体,是一种超强透明材料,可以由反应Al2O3+C+N2 ![]() 2AlON+CO合成,下列有关说法正确的是( )
2AlON+CO合成,下列有关说法正确的是( )
A.氮氧化铝中氮的化合价是﹣3
B.反应中氧化产物和还原产物的物质的量之比是1:2
C.反应中每生成5.7gAlON同时生成1.12LCO
D.AlON和CO的化学键类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.01mol氯化铬(CrCl36H2O)在水溶液中用过量AgNO3处理,产生0.02mol AgCl沉淀,此氯化铬最可能为( )
A.[Cr(H2O)6]Cl3
B.[Cr(H2O)5Cl]Cl2H2O
C.[Cr(H2O)4Cl2]Cl2H2O
D.[Cr(H2O)3Cl3]3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包铁粉和氧化铜混合均匀的粉末样品4.40g,加入50mL稀硫酸恰好充分反应后,得到只含一种金属阳离子的浅绿色溶液和1.28g固体铜.并放出H2 . 试计算:
(1)固体铜的物质的量为mol,该样品中铁粉和氧化铜的物质的量之比为 .
(2)硫酸的物质的量的浓度molL﹣1 , 产生H2在标准状况下的体积L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数,下列叙述中正确的是( )
A.在标准状况下,1L庚烷完全燃烧后,所生成的气态产物的分子数为 ![]() NA
NA
B.1mol碳正离子CH5+所含的电子数为10NA
C.56g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA
D.0.5molC3H8分子中含C﹣H共价键2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com