
【题目】分枝酸可用于生化研究,其结构简式如图所示.下列关于分枝酸的叙述正确的是( ) 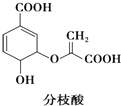
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分枝酸分子中含2mol﹣OH(羟基)
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
【答案】B
【解析】A.分子中含﹣COOH、﹣OH、碳碳双键、醚键,共4种官能团,故A不符合题意;
B.含﹣COOH与乙醇发生酯化反应,含﹣OH与乙酸发生酯化反应,故B符合题意;
C.不是苯环,只有﹣COOH与NaOH反应,则1mol分枝酸最多可与2molNaOH发生中和反应,故C不符合题意;
D.碳碳双键与溴的四氯化碳溶液发生加成反应,双键与﹣OH均能被酸性高锰酸钾溶液氧化,原理不同,故D不符合题意;
所以答案是:B.
【考点精析】关于本题考查的有机物的结构和性质,需要了解有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解才能得出正确答案.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,一定条件下,它们之间有如下反应关系。A + B![]() C + D + E
C + D + E
(1)若A是碳,B是浓硫酸,C、D都是气体,试写出此反应的化学方程式_______________。
(2)若A是铜,B是硝酸,反应时生成的C是红棕色气体,反应的离子方程式是________________,生成的C与水反应的化学方程式为______________________________。
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式____________________________________________;实验室检验C的方法__________________________________________________。
(4)若A是焙制糕点所用的发酵粉的主要成分,B是稀盐酸,则A和B在水溶液反应的离子方程式是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为几种短周期元素的性质,回答下列问题:
元素编号 | A | B | C | D | E | F | G | H |
原子半径/10-1nm | 0.74 | 1.54 | 1.30 | 1.18 | 1.11 | 1.06 | 0.99 | 0.75 |
最高或最低化合价 | -2 | +1 | +2 | +3 | +4,-4 | +5,-3 | +7,-1 | +5,-3 |
(1)E元素在元素周期表中的位置是_____;C元素与G元素形成化合物的电子式_____ 。
(2)D的单质与B的最高价氧化物对应水化物的溶液反应,其离子方程式为_________。
(3)B2A2中含有的化学键为_______,该物质与水反应的化学反应方程式为________。
(4)下列说法不正确的是______(填序号)。
①H的气态氢化物水溶液能导电,说明H的气态氢化物为电解质
②最高价氧化物对应水化物的碱性:B>C>D
③D的最高价氧化物对应水化物可以溶于氨水
④元素气态氢化物的稳定性:F>A>G
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
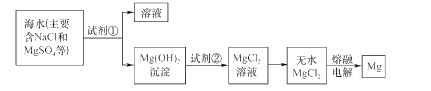
(1)为了使MgS04转化为Mg(OH)2,试剂①可以选用____(填化学式)。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是____。
(3)试剂②可以选用 ___(填化学式)。
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、D、E、F是原子序数依次增大的六种常见元素。E的单质在Z2中燃烧的产物可使品红溶液褪色。F和Z元素形成的化合物F3Z4具有磁性。X的单质在Z2中燃烧可生成XZ和XZ2两种气体。D的单质是一种金属,该金属在XZ2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)F元素在周期表中的位置是________,Y的单质分子的结构式为__________,DZ的电子式为________,DZ化合物中离子半径较大的是________(填离子符号)。
(2)X元素形成的同素异形体的晶体类型可能是________(填序号)。
①原子晶体 ②离子晶体 ③金属晶体 ④分子晶体
(3)X、Y、Z形成的10电子氢化物中,X、Y的氢化物沸点较低的是(写化学式):__________;Y、Z的氢化物分子结合H+能力较强的是(写化学式)________。
(4)下列可作为比较D和Na金属性强弱的依据是________。(填序号)
a.测两种元素单质的硬度和熔、沸点
b.比较两元素最高价氧化物对应的水化物溶液的碱性强弱
c.比较两种元素在氯化物中化合价的高低
d.比较单质与同浓度盐酸反应的剧烈程度
(5)Y的氢化物和Z的单质在一定条件下反应生成Z的氢化物(产物之一),该反应的方程式为___________。
(6)有人建议将氢元素排在元素周期表的ⅣA族,请你从化合价的角度给出一个理由__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱.可以将  转变为
转变为 ![]() 的方法是( )
的方法是( )
①与足量的NaOH溶液共热,再通入CO2
②与稀硫酸共热后,加入足量的NaOH溶液
③加热溶液,通入足量的SO2
④与稀H2SO4共热后,加入足量的NaHCO3 .
A.①②
B.①④
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某羧酸衍生物A,其分子式为C6H12O2 , 实验表明A和氢氧化钠溶液共热生成B和C,B和盐酸反应生成有机物D,C在铜催化和加热的条件下氧化为E,其中D、E都不能发生银镜反应.由此判断A的可能的结构有( )
A.6种
B.2种
C.4种
D.3种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com