
【题目】已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,一定条件下,它们之间有如下反应关系。A + B![]() C + D + E
C + D + E
(1)若A是碳,B是浓硫酸,C、D都是气体,试写出此反应的化学方程式_______________。
(2)若A是铜,B是硝酸,反应时生成的C是红棕色气体,反应的离子方程式是________________,生成的C与水反应的化学方程式为______________________________。
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式____________________________________________;实验室检验C的方法__________________________________________________。
(4)若A是焙制糕点所用的发酵粉的主要成分,B是稀盐酸,则A和B在水溶液反应的离子方程式是______________________________。
【答案】 C+2H2SO4(浓)![]() CO2↑+ 2H2O + SO2↑ Cu +2NO3-+ 4H+ = Cu 2++2NO2↑+ 2H2O 3NO2+H2O = 2H NO3+ NO 2NH4Cl+ Ca(OH)2
CO2↑+ 2H2O + SO2↑ Cu +2NO3-+ 4H+ = Cu 2++2NO2↑+ 2H2O 3NO2+H2O = 2H NO3+ NO 2NH4Cl+ Ca(OH)2![]() CaCl2 +2NH3↑+2H2O 把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气。(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气。) H+ + HCO3— = H2O+ CO2↑
CaCl2 +2NH3↑+2H2O 把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气。(或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气。) H+ + HCO3— = H2O+ CO2↑
【解析】本题考查的是无机推断,根据物质的颜色和气味入手,掌握常见物质的基本性质是关键。
常温下,E是一种无色无味的液体,则说明其为水。(1) 若A是碳,B是浓硫酸,C、D都是气体,则碳和浓硫酸反应生成二氧化碳和二氧化硫和水,方程式为:C+2H2SO4(浓)![]() CO2↑+ 2H2O + SO2↑。 (2) 若A是铜,B是硝酸,反应时生成的C是红棕色气体,即二氧化氮,则说明是铜和浓硝酸反应生成硝酸铜和二氧化氮和水,离子方程式为:Cu +2NO3-+ 4H+ = Cu 2++2NO2↑+ 2H2O。二氧化氮和水反应生成硝酸和一氧化氮,方程式为:3NO2+H2O = 2HNO3+ NO。 (3) 若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,即为氨气,则为氯化铵和氢氧化钙反应生成氯化钙和氨气和水,方程式为: 2NH4Cl+ Ca(OH)2
CO2↑+ 2H2O + SO2↑。 (2) 若A是铜,B是硝酸,反应时生成的C是红棕色气体,即二氧化氮,则说明是铜和浓硝酸反应生成硝酸铜和二氧化氮和水,离子方程式为:Cu +2NO3-+ 4H+ = Cu 2++2NO2↑+ 2H2O。二氧化氮和水反应生成硝酸和一氧化氮,方程式为:3NO2+H2O = 2HNO3+ NO。 (3) 若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,即为氨气,则为氯化铵和氢氧化钙反应生成氯化钙和氨气和水,方程式为: 2NH4Cl+ Ca(OH)2![]() CaCl2 +2NH3↑+2H2O,实验室检验氨气的方法利用了氨气溶于水显碱性的性质,把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气。或利用氨气和氯化氢反应生成氯化铵,用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气。(4) 若A是焙制糕点所用的发酵粉的主要成分,即为碳酸氢钠,B是稀盐酸,则二者反应生成二氧化碳和水和氯化钠,离子方程式为:H+ + HCO3— = H2O+ CO2↑。
CaCl2 +2NH3↑+2H2O,实验室检验氨气的方法利用了氨气溶于水显碱性的性质,把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气。或利用氨气和氯化氢反应生成氯化铵,用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气。(4) 若A是焙制糕点所用的发酵粉的主要成分,即为碳酸氢钠,B是稀盐酸,则二者反应生成二氧化碳和水和氯化钠,离子方程式为:H+ + HCO3— = H2O+ CO2↑。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】由芳香烃X合成一种功能高分子H的过程如下。(部分产物、合成路线、反应条件略去)。
其中A是一氯代物,H的链节组成为C7H5NO
已知:I芳香烃X用质谱仪测出的质谱图如图所示
请根据所学知识与本题所给信息回答下列问题
(1)H的结构简式是_____________;(2)反应③和④的类型分别是_____________、_____________
(3)反应⑤的化学方程式是__________________________
(4)阿司匹林中含氧官能团的名称为__________________________
(5) 的一种同系物
的一种同系物 有多种同分异构体,其中符合下列要求的共有_____________种(不考虑立体异构),写出其中核磁共振氢谱为6组峰,且峰面积比为2:2:2:2:1:1的结构简式_____________
有多种同分异构体,其中符合下列要求的共有_____________种(不考虑立体异构),写出其中核磁共振氢谱为6组峰,且峰面积比为2:2:2:2:1:1的结构简式_____________
①能与 NaHCO3反应放出CO2
②能与FeCl3溶液发生显色反应
③苯环上的一取代物有两种
(6)请用合成反应流程图表示出由A和其他无机物合成 最合理的方案。_______________
最合理的方案。_______________
例:  。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的用途非常广泛,以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴的碳酸盐及SiO2杂质)为原料生产金属锰的工艺流程如下:

已知25℃,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | Fe(OH)3 | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.1×10-36 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)步骤Ⅰ中,为加快溶浸速率,可采取的措施是____________________(至少答两条)
(2)步骤Ⅱ中,加氨水调节溶液的pH为5.0~6.0,则滤渣1的成分主要为______(填化学式);已知MnO2的作用为氧化剂,“除杂1”中涉及的离子方程式为:NH3﹒H2O+H+==NH4+ +H2O、__________________、___________________。
(3)步骤Ⅲ中,所加(NH4)2S的浓度不宜过大的原因是_______________________。
(4)滤液2中,c(Co2+) :c(Ni2+)=_______________。
(5)将质量为a㎏的碳酸锰矿经上述流程处理后得到单质Mn b kg。若每一步都进行完全,假设滤渣1为含铁元素的纯净物,质量为c kg,则原碳酸锰矿中MnCO3的质量分数为_________(用含a、b、c的式子表达,无需化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下物质①NaCl晶体②CO2③液态的纯醋酸④铜⑤BaSO4固体⑥蔗糖⑦酒精⑧氨水,请回答下列问题(填序号)
(1)能导电的是
(2)属于电解质的是
(3)属于非电解质的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
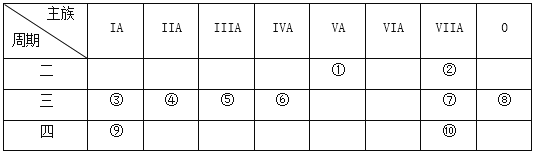
(1)在③~⑦中元素,原子半径最大的是_____________,其离子的结构示意图是__________________。
(2)表中的①~⑩中元素,非金属性最强的是_______,化学性质最稳定的是________,金属性最强的是__________,最高价氧化物的水化物的酸性最强的是(写该水化物的化学式)______________。
(3)⑦的氢化物的水溶液与①的氢化物的水溶液反应的离子方程式为___________________________。
(4)用一个化学反应说明⑦比⑩的单质化学性质活泼,写出反应的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选用的仪器和药品和实验结论正确的是( )
A | B | C | D |
|
|
|
|
制取乙烯并验证其还原性 | 加热熔融 NaOH固体 | 获得金属钙装置(熔融CaF2-CaO 作电解质),并用钙还原 TiO2 制备金属钛,制备金属钛前后装置中 CaO 的总量不变 | 准确量取一定体积K2Cr2O7标准溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图示说法正确的是( )

A. 图甲为微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质, (a、b 均为石墨电极),a 电极发生反应:H2N(CH2)2NH2+16e-+4H2O==2CO2↑+N2↑+16H+
B. 图乙表示反应物键能小于生成物键能
C. 常温下向 10mL 0.1mol/L 的某酸(HA) 溶液中逐滴加入 0.1mol/L 的氨水,所得溶液的 pH及导电能力与加入氨水的体积关系如图,b 点 HA 溶液与氨水恰好完全反应
D. 图丁表示反应 N2(g)+3H2(g)![]() 2NH3(g)平衡时 NH3体积分数随起始 n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
2NH3(g)平衡时 NH3体积分数随起始 n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列科研成果不是由我国发明或创造的是( )
A.世界上第一个由人工合成的、具有生理活性的蛋白质﹣﹣结晶牛胰岛素
B.黑火药和造纸
C.发现元素周期律
D.青蒿素的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图所示.下列关于分枝酸的叙述正确的是( ) 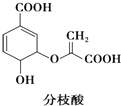
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分枝酸分子中含2mol﹣OH(羟基)
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com