
【题目】锰的用途非常广泛,以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴的碳酸盐及SiO2杂质)为原料生产金属锰的工艺流程如下:

已知25℃,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | Fe(OH)3 | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.1×10-36 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)步骤Ⅰ中,为加快溶浸速率,可采取的措施是____________________(至少答两条)
(2)步骤Ⅱ中,加氨水调节溶液的pH为5.0~6.0,则滤渣1的成分主要为______(填化学式);已知MnO2的作用为氧化剂,“除杂1”中涉及的离子方程式为:NH3﹒H2O+H+==NH4+ +H2O、__________________、___________________。
(3)步骤Ⅲ中,所加(NH4)2S的浓度不宜过大的原因是_______________________。
(4)滤液2中,c(Co2+) :c(Ni2+)=_______________。
(5)将质量为a㎏的碳酸锰矿经上述流程处理后得到单质Mn b kg。若每一步都进行完全,假设滤渣1为含铁元素的纯净物,质量为c kg,则原碳酸锰矿中MnCO3的质量分数为_________(用含a、b、c的式子表达,无需化简)。
【答案】 溶浸时加热(或升高温度)、适当增大硫酸浓度、搅拌、再减小矿粉颗粒直径 SiO2、Fe(OH)3 2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O Fe3++3NH3﹒H2O=Fe(OH)3↓+3NH4+ 若(NH4)2S的浓度过大,产生MnS沉淀造成产品损失 5:1 ![]() ×100%
×100%
【解析】向碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)中加入硫酸,可以发生反应生成硫酸盐,向其中就如具有氧化性的二氧化锰,可以将亚铁离子氧化为铁离子,调节pH可以将氢氧化铁沉淀下来,向滤液中加入硫化铵,可以将镍离子、钴离子形成硫化物沉淀下来,最后对得到的含有锰离子的盐电解,可以得到金属锰。
(1)搅拌固体和液体的混合物,升高温度、增大浓度等,都可加快反应速率,所以为了提高浸取率可采取的措施有加热或搅拌或增大硫酸浓度等,故答案为:溶浸时加热(或升高温度)、适当增大硫酸浓度、搅拌、再减小矿粉颗粒直径;
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,反应的离子方程式MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,加入氨水调节pH为5.06.0,发生Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+,可得到沉淀Fe(OH)3,故答案为:Fe(OH)3;2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;Fe3++3NH3﹒H2O=Fe(OH)3↓+3NH4+;
(3)向滤液中滴入适量的(NH4)2S溶液,目的是除去Cu2+、Zn2+,若(NH4)2S的浓度过大,产生MnS沉淀,造成产品损失、故答案为:若(NH4)2S的浓度过大,产生MnS沉淀,造成产品损失;
(4)CoS、NiS的Ksp分别为5.0×1022、1.0×1022,加入足量(NH4)2S溶液后,生成CoS、NiS沉淀,溶液中c(Co2+):c(Ni2+)=5.0×1022:1.0×1022=5:1,故答案为:5:1;
(5)滤渣1为为Fe(OH)3,质量为ckg,则n(Fe3+)=n[Fe(OH)3]=![]() mol,由2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O可知n(MnO2)=
mol,由2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O可知n(MnO2)=![]() ×
×![]() mol,
mol,
将质量为a kg的碳酸锰矿经上述流程处理后得到单质Mnbkg,n(Mn)=![]() mol,
mol,
可知n(MnCO3)=![]() mol -
mol -![]() ×
×![]() mol,m(MnCO3)=(
mol,m(MnCO3)=(![]() mol -
mol -![]() ×
×![]() mol)×115g/mol,
mol)×115g/mol,
则原碳酸锰矿中MnCO3的质量分数为![]() ,故答案为:
,故答案为:![]()


科目:高中化学 来源: 题型:
【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点231.9C)与Cl2 反应制备SnCl4装置如下图所示。
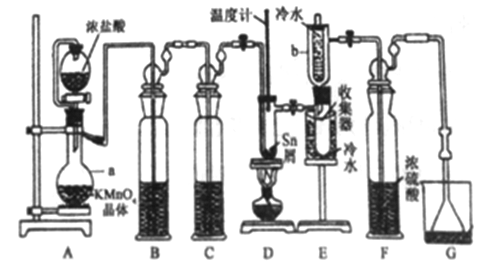
已知,① SnCl4在空气中极易水解生成SnO2xH2O;②SnCl2、SnCl4有关物理性质如下表。
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
回答下列问题:
(1)仪器a的名称是__________,其中发生反应的离子方程式为________。
(2)装置B、C 中盛装的试剂分别是_______、__________。
(3)当观察到装置F液面上方出现_____现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的有:①加快氯气与锡反应,②__________。
(4)E装置中b的作用是___________。
(5)若制得产品中含有少量Cl2,则可采用下列_____(填字母)措施加以除去。
A.加入NaOH 萃取分液 B.加入足量锡再加热蒸馏
C.加入碘化钾冷凝过滤 D.加入饱和食盐水萃取
(6)可用滴定法测定最后产品的纯度。准确称取该样品mg加入到适量浓盐酸溶解,然后再加水稀释至250 mL,用移液管移取25.00 ml,稀释后的溶液于锥形瓶中,加入两滴淀粉溶液作指示制,用cmol/L 的KIO3 标准溶液进行滴定,平行滴定3 次,平均消耗V mL的标准溶液。已知滴定时发生的反应为:Sn2++IO3-+H+→Sn4++I2+H2O(未配平)。回答下列问题:
①判断达到滴定终点的现象为____________。
②产品中SnCl2(摩尔质量为M g/mol )的含量为____%(用含m、c、V、M 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去KNO3固体中少量的KCl,有以下可供选择的8个操作:
①过滤 ②萃取 ③固体溶于水 ④冷却结晶 ⑤蒸发浓缩 ⑥干燥 ⑦洗涤 ⑧分液
从中选出正确的操作且排序正确的是( )
A.⑤④①B.③②⑧C.③①⑦⑥D.③⑤④①⑦⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应SO2+O2=2SO3在密闭容器中进行。下列关于该反应的说法正确的是
A. 增大压强能减慢反应速率
B. v(SO2):v(O2)=2:1证明该反应已达到化学平衡状态
C. 当反应物和生成物浓度不变时,反应已达平衡
D. 增大02的浓度可使SO2完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1mol/LNaOH溶液滴定10 mL 0.1 mol/LH2A溶液,溶液的pH与NaOH溶液的体积关系如图所示。下列说法不正确的是
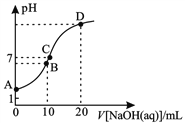
A. A点溶液中加入少量水:![]() 增大
增大
B. B点:c( HA -)>c(H+)>c(A2一)>c(H2A)
C. 水电离出来的c(OH -):B点>D点
D. C点:c(Na+) =c(HA-)+2c( A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火法炼铜的主要反应原理:Cu2S+O2=2Cu+SO2,下列说法正确的是
A. Cu是还原产物 B. SO2只是还原产物
C. 氧化剂只有O2 D. 1molS02生成转移4 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究氨、乙醇的性质,某同学设计并进行了下列实验。
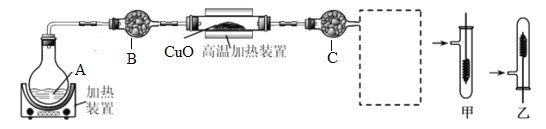
请回答:
(1)仪器B的名称为_____________。
(2)为快速制备氨气,A中应加入的试剂为______,B中应放入的试剂为_______。
(3)若A中加入乙醇,B中加入生石灰,C中加入无水硫酸铜,反应一段时间后,C中的现象为_________。经检测反应中既生成了乙醛,又生成了少量乙酸。请写出乙醇与氧化铜反应生成乙醛的化学方程式_____________________。
(4)在(3)中实验里,某同学为检验尾气中是否含有乙醇,虚线框处宜选择的装置是______(填“甲”或“乙”);实验时应先将螺旋状铜丝加热,变黑后再趁热迅速伸入试管中,观察到铜丝由黑渐渐变红,由此可得出的结论是____________________。(并简述其理由)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,一定条件下,它们之间有如下反应关系。A + B![]() C + D + E
C + D + E
(1)若A是碳,B是浓硫酸,C、D都是气体,试写出此反应的化学方程式_______________。
(2)若A是铜,B是硝酸,反应时生成的C是红棕色气体,反应的离子方程式是________________,生成的C与水反应的化学方程式为______________________________。
(3)若实验室中利用A和B的反应制备气体C,C是一种无色、刺激性气味、密度比空气小的气体,试写出此反应的化学方程式____________________________________________;实验室检验C的方法__________________________________________________。
(4)若A是焙制糕点所用的发酵粉的主要成分,B是稀盐酸,则A和B在水溶液反应的离子方程式是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为几种短周期元素的性质,回答下列问题:
元素编号 | A | B | C | D | E | F | G | H |
原子半径/10-1nm | 0.74 | 1.54 | 1.30 | 1.18 | 1.11 | 1.06 | 0.99 | 0.75 |
最高或最低化合价 | -2 | +1 | +2 | +3 | +4,-4 | +5,-3 | +7,-1 | +5,-3 |
(1)E元素在元素周期表中的位置是_____;C元素与G元素形成化合物的电子式_____ 。
(2)D的单质与B的最高价氧化物对应水化物的溶液反应,其离子方程式为_________。
(3)B2A2中含有的化学键为_______,该物质与水反应的化学反应方程式为________。
(4)下列说法不正确的是______(填序号)。
①H的气态氢化物水溶液能导电,说明H的气态氢化物为电解质
②最高价氧化物对应水化物的碱性:B>C>D
③D的最高价氧化物对应水化物可以溶于氨水
④元素气态氢化物的稳定性:F>A>G
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com