
����Ŀ����ͼ��ʾ��ijͬѧ�����һ��ȼ�ϵ�ز�̽���ȼҵԭ���ʹ�ͭ�ľ���ԭ����������װ����XΪ�����ӽ���Ĥ���밴Ҫ��ش�������⣺


��1������ȼ�ϵ�ظ�����Ӧʽ��__________________��
��2��ʯī(C)���ĵ缫��ӦʽΪ________________________��
��3�����ڱ�״���£���2.24 L�����μӷ�Ӧ������װ�������������ɵ��������Ϊ________L ����װ������������ͭ������Ϊ________g��
��4��ijͬѧ���ü���ȼ�ϵ����Ƶ�ⷨ��ȡFe(OH)2��ʵ��װ��(��ͼ��ʾ)��������Fe(OH)2��ʹ�����������������Һ������ѡ��________���缫��
���𰸡�CH4-8e-+10OH-=CO32-+7H2O 2Cl--2e-=Cl2�� 4.48L 12.8 ��
��������
���⣨1������ȼ�ϵ�أ������ڸ�����Ӧ������ʽ��CH4-8e-+10OH-=CO32-+7H2O��
��2����������һ��Ϊ����������һ��Ϊ����������������Ϊ������ʯīΪ��������Ӧ��2Cl--2e-=Cl2��
��3����״���£�2.24 L�������ʵ���=0.1mol��ת�Ƶ���0.4mol��������Ӧ��2H++2e-=H2��������0.2mol���������=0.2��22.4=4.48L����ת�Ƶ�����ȣ�����������Ӧ��Cu2++2e-=Cu������ͭ���ʵ�����0.2mol������=0.2��56=12.8g��
��4��Ϊ���ɶ��������������������缫��


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(��Ҫ�ɷ�Ϊ�����Ͻ𣬺�����ͭ)Ϊԭ�ϣ�����NiO�IJ��ֹ����������£�
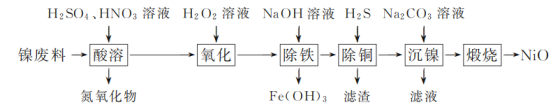
��֪���±��г��˼��ֽ������������������������pH(��ʼ������pH����������Ũ��Ϊ1.0 mol��L��1����)��
�������� | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
��ʼ������pH | 1.5 | 6.5 | 7.7 |
������ȫ��pH | 3.3 | 9.9 | 9.2 |
��1����������ʱ�������Һ��pH��ΧΪ________��
��2��������������Ҫ�ɷ�Ϊ________(�ѧʽ)��
��3����������ʱ�õ���ʽ̼����[��xNiCO3��yNi(OH)2��ʾ]������
���ڸ������������£�����������ʽ̼�����õ�NiO���÷�Ӧ�Ļ�ѧ����ʽΪ________��
����������ʱ����ҺpH����ʽ̼������NiԪ�غ��������ӣ�ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȤС�����ⶨijNaOH��Һ��Ũ�ȣ�������������£�
�ٽ���ʽ�ζ���������ˮϴ�����ô�����Һ��ϴ����ע�������Һ�����ڵζ��ܵļ��첿�ֳ�����Һ����ʹҺ�洦����0���̶����µ�λ�ã����¶���������ƿ������ˮϴ�����ô�����Һ��ϴ��ƿ2��3�Σ��Ӽ�ʽ�ζ����зų�25.00mL������Һ����ƿ�С�
�ڽ���ʽ�ζ���������ˮϴ��������������ע��0.1000mol��L��1�����ᣬ���ڵζ��ܵļ��첿�ֳ�����Һ����ʹҺ�洦����0���̶����µ�λ�ã����¶�����
������ƿ�е����̪��ָʾ�������еζ����ζ����յ㣬���������������ΪV1mL��
���ظ����Ϲ��̣����ڵζ�����������ƿ�м���5mL������ˮ�����������������ΪV2mL���Իش��������⣺
��1���ζ��յ�ʱ������Ϊ��______________________________________��
��2���ζ�ʱ�ߵα�ҡ����ƿ���۾�Ӧ�۲�_________________________��
��3����С���ڲ�����еĴ�����________________���ɴ���ɵIJⶨ��� ______(����ƫ��������ƫ����������Ӱ����)��
��4�������ȱ�ٵIJ�����____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л������ʽΪ C4H8���ݴ��Ʋ���ṹ�����ʲ����ܵ���
A. ������ϩ������ͬϵ��
B. һ�ȴ���ֻ��һ��
C. ���ӽṹ�м�����Ŀ������ 0��1��2
D. ������CH4��C4H8�ֱ�����������ȫȼ�գ�CH4�ĺ�����С��C4H8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������������ݻ�Ϊ2L���ܱ�����������2 mol ����M��3 mol N���������������·�Ӧ��2M(g) + 3N(g) ![]() x Q(g) +3R(g)���÷�Ӧ��ƽ��ʱ������2.4mol R�������Q��Ũ��Ϊ0.4 mol/L�������й�������ȷ����
x Q(g) +3R(g)���÷�Ӧ��ƽ��ʱ������2.4mol R�������Q��Ũ��Ϊ0.4 mol/L�������й�������ȷ����
A. xֵΪ2 B. ���������ܶ�����
C. N��ת����Ϊ20% D. ƽ��ʱN��Ũ��Ϊ0.3 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ���־������ʾ��ͼ��


��ش��������⣺
��1�����������У�����֮���Թ��ۼ�����γɵľ�����____��
��2���������ʯ��MgO��CaCl2���ɱ�5�־�����۵��ɸߵ��͵�˳��Ϊ��___��
��3��NaCl������MgO������ͬ��NaCl����ľ�����___(����ڡ���С�ڡ�)MgO���壬ԭ����____��
��4��ÿ��Cu������ʵ��ռ��___��Cuԭ�ӣ�CaCl2������Ca2������λ��Ϊ__��
��5�������۵�Զ���ڸɱ�����H2O�Ǽ��Է��ӡ�CO2�ǷǼ��Է����⣬����һ����Ҫ��ԭ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������Ա�ϩ����ϩΪԭ�Ͻ��л�����������Ҫ�������¡������й�˵���������( )
![]() ������
������![]()
A����Ӧ���뷴Ӧ������ȡ����Ӧ
B����Ӧ���뷴Ӧ�����Ǽӳɷ�Ӧ
C����Ӧ���в���Ľṹ��ʽΪCH2BrCH2CHClBr
D����Ӧ������������������ϩ��ˮ��Ӧ�Ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǰ��ȫ����Դ���š������ů�Ѷ����������ͷ�չ�γ����Ͼ�����ս����չ��̼���á�������̼�������������ȣ����Ǵ��������������û�ѧ��Ӧԭ�������֪ʶ�о�̼���仯��������ʡ�
(1)��ҵ�Ͻ�CO2�뽹̿��������CO��CO�������������䷴Ӧԭ��Ϊ��
��Fe2O3(s)+3C(s)=2Fe(s)+3CO(g) ��H1=+489.0kJ��mol-1
��C(s)+CO2(g)=2CO(g) ��H2=+172.5 kJ��mol-1
��CO��ԭFe2O3���Ȼ�ѧ����ʽΪ___________��
(2)�ʵ������½�CO2��H2��1:3������Ȼ�Ϻϳɼ״���ˮ��CO2(g)+3H2(g)CH3OH(g) +H2O(g) ��H =-49.0 kJ��mol-1�������Ϊ2 L���ܱ������У�����2 mol CO2��6 mol H2�����CO2(g)��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��

�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ________��
�ڴӷ�Ӧ��ʼ��ƽ�⣬![]() (H2)=______��������ת����=______����ʹƽ����ϵ��n(CH3OH)����Ĵ�ʩ��___________��
(H2)=______��������ת����=______����ʹƽ����ϵ��n(CH3OH)����Ĵ�ʩ��___________��
(3)CO����������ȼ�ϵ�ص�ȼ�ϣ�ij������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ��õ����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����为����ӦʽΪ��2CO-4e-+2![]() =4CO2����������ӦʽΪ__________��
=4CO2����������ӦʽΪ__________��
(4)CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp =3.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ���(���Ի�Ϻ���Һ����ı仯)����Na2CO3��Һ��Ũ��Ϊ2��10-4mol��L-1�������ɳ�������CaCl2��Һ����СŨ��Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ֻ�ѧ��Ϊ 2��4��4�����ȡ�2�� �ǻ��������ѵ�����(����ͼ)�����㷺Ӧ���ڷ�������������û�ѧƷ֮�У���ɱ�����������á��������й�˵������ȷ���� �� ��

A. �������� FeCl3��Һ��Ϻ���ɫ
B. ������������ԭ��һ������ͬһƽ��
C. �����ʱ����ϵ�һ��ȡ������ 6 ��
D. ���ʵķ���ʽΪ C12H6Cl3O2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com