
【题目】某溶液X含有H+、Al3+、NH4+、Fe2+、Fe3+、HCO3-、S2-、SO42-、Cl-、OH-中的一种或几种,取该溶液进行实验,实验内容和相关数据(气体体积在标准状况下测定)如下:
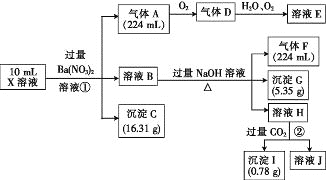
(1)通过上述实验过程,一定不存在的离子是_______。
(2)反应①中生成A的离子方程式为________。
(3)若测得X溶液中c(H+)=6mol·L-1,则X溶液中_______(填“含”或“不含”)Fe3+,c(Fe3+)=________mol·L-1(若填不含,则不需计算),X溶液中c(Cl-)=_______mol·L-1。
【答案】HCO3-、S2-、OH- 3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O 含 2 8
【解析】
测得X溶液中c(H+)=6mol/L,在强酸性溶液中与H+反应的离子不能大量存在;一定不会存在HCO3-、S2-、OH-离子,加入过量硝酸钡生成沉淀,则沉淀C为BaSO4 沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E 为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量 NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于 CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,沉淀G为Fe(OH)3,说明原溶液中含有Al3+离子,通过计算氢氧化铁物质的量和原溶液中亚铁离子物质的量判断原溶液中含有Fe3+,溶液显酸性,溶液中含有Fe2+离子,就一定不含NO3-离子,根据已知溶液中电荷守恒计算确定是否含有的离子Cl-,以此解答。
通过上述分析可知:气体A是NO,溶液B中含有Al3+、NH4+、Fe2+,沉淀C是BaSO4,气体D是NO2,溶液E为HNO3,气体F是NH3,I为Al(OH)3,H为NaAlO2,沉淀G为Fe(OH)3:
(1)由于测得X溶液中c(H+)=6mol/L,溶液显酸性,在强酸性溶液中与H+反应的离子HCO3-、S2-、OH-不能大量存在;故原溶液一定不会存在HCO3-、S2-、OH-离子;
(2)在X中含有Fe2+、H+,当加入Ba(NO3)2溶液时,会发生氧化还原反应,产生Fe3+、NO、H2O,反应的离子方程式:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)n(NO)=0.224L÷22.4L/mol=0.01mol,根据3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O中Fe2+与NO的关系可知n(Fe2+)=3n(NO)=0.03mol,n[Fe(OH)3]=5.35g÷107g/mol=0.05mol>n(Fe2+)=0.03mol,根据Fe元素守恒,说明在原溶液中含有Fe3+,其物质的量是0.02mol,由于溶液的体积是0.01L,所以c(Fe3+)=0.02mol÷0.01L=2mol/L;该溶液中,n(H+)=6mol/L×0.01L=0.06mol,根据元素守恒可得n(NH4+)=n(NH3)=0.224L÷22.4L/mol=0.01mol,n(SO42-)=n(BaSO4)=16.31g÷233g/mol=0.07mol,n(Al3+)=n[Al(OH)3]=0.78g÷78g/mol=0.01mol,根据(3)计算可知n(Fe2+)=0.03mol,n(Fe3+)=0.02mol,由于正电荷总数:3n(Al3+)+ 3n(Fe3+)+2n(Fe2+)+ n(NH4+)+ n(H+)=3×0.01mol+3×0.02mol+2×0.03mol+0.01mol+0.06mol=0.22mol,n(SO42-)=0.07mol,其所带的负电荷数0.07mol×2=0.14mol<0.22mol,所以该溶液中还含有带负电荷的Cl-,其物质的量为n(Cl-)=0.22mol-0.14mol=0.08mol,其物质的量浓度c(Cl-)=0.08mol÷0.01L=8mol/L。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强烈氧化时,最终都氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸 。反应原理:
![]() +2KMnO4
+2KMnO4 ![]() +KOH+2MnO2 +H2O
+KOH+2MnO2 +H2O
![]() +HCl
+HCl![]() +KCl
+KCl
反应试剂、产物的物理常数:
名称 | 相对分 子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
水 | 乙醇 | 乙醚 | ||||||
甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
主要实验装置和流程如下:
下图回流搅拌装置
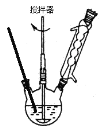
下图抽滤装置

实验方法:一定量的甲苯和KMnO4溶液置于图1装置中,在90℃时, 反应一段时间,再停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
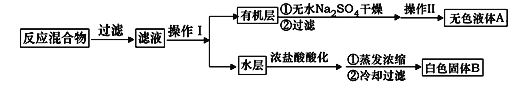
(1)无色液体A的结构简式为___________。操作Ⅱ为__________。
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是______。
(3)下列关于仪器的组装或者使用正确的是__________。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是下进上出
(4)除去残留在苯甲酸中的甲苯应先加入__________,分液,水层再加入__________,然后抽滤,干燥即可得到苯甲酸。
(5)纯度测定:称取1.220g产品,配成100ml溶液,取其中25.00ml溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+ ![]() H2↑ + Cl2↑
H2↑ + Cl2↑
B. 向Al2(SO4)3溶液中加入过量的NH3·H2O:Al3+ + 4NH3·H2O ═ AlO2-+ 4NH4+ + 2H2O
C. 苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O-→ 2C6H5OH + 2 CO32-
D. Na2SO3溶液使酸性KMnO4溶液褪色:5SO32- + 6H+ + 2MnO4- ═ 5SO42-+ 2Mn2+ + 3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,下列说法正确的是( )
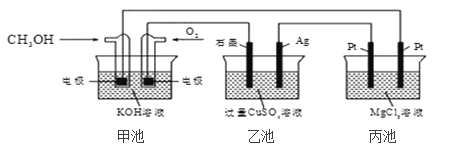
A. 若将乙池电解液换成 AgNO3 溶液,则可以实现在石墨棒上镀银
B. 甲池通入 CH3OH 的电极反应式为 CH3OH+6e+2H2O═CO32-+8H+
C. 反应一段时间后,向乙池中加入一定量 Cu(OH)2 固体,能使 CuSO4 溶液恢复到原浓度
D. 甲池中消耗 224mL(标准状况下)O2,此时丙池中理论上产生 1.16g 固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据了解,铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。

下列说法正确的是
A. Cu2(OH)3Cl属于有害锈
B. Cu2(OH)2CO3属于复盐
C. 青铜器表面刷一层食盐水可以做保护层
D. 用NaOH溶液法除锈可以保护青铜器的艺术价值,做到“修旧如旧”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2SO2(g)+O2(g)![]() 2SO3(g)+196.64kJ,则下列判断正确的是
2SO3(g)+196.64kJ,则下列判断正确的是
A.2SO2(g)+O2(g)![]() 2SO3(l)+Q,Q>196.64kJ
2SO3(l)+Q,Q>196.64kJ
B.2molSO2气体和过量的O2充分反应放出196.64kJ热量
C.1LSO2(g)完全反应生成1LSO3(g),放出98.32kJ热量
D.使用催化剂,可以减少反应放出的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )

A. 该有机物的分子式为C7H7O3
B. 该有机物能发生取代、加成和氧化反应
C. 1mol该有机物最多能与2mol H2发生加成反应
D. 该有机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1 L 0.5 mol/L Na2CO3溶液中含有的CO32-数目为0.5NA
B. 物质的量浓度为0.5mol/LAlCl3溶液中,含有Cl-个数为1.5NA
C. 6g乙烷中含有的共价键的数目为1.4NA
D. l mol甲基(- CH3)所含电子数为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com