
【题目】下列说法错误的是( )
A.O3与SO2的结构相似
B.硫粉不溶于水,易溶于CS2中
C.Be(OH)2是两性氢氧化物
D.在相同条件下,![]() 的沸点高于
的沸点高于![]()
【答案】D
【解析】
A.O3与SO2的结构相似,都是V型分子,故A正确;
B.根据相似相溶原理,硫粉不溶于水,易溶于CS2中,故B正确;
C.Be与铝处于对角线位置,性质相似,Be(OH)2是两性氢氧化物,故C正确;
D.在相同条件下,![]() 容易形成分子内氢键,使得沸点降低,
容易形成分子内氢键,使得沸点降低,![]() 容易形成分子间氢键,使得沸点升高,故D错误;
容易形成分子间氢键,使得沸点升高,故D错误;
故选D。
【点晴】
常见易形成氢键的化合物:H2O、HF、NH3等.(1)分子间氢键:①同种分子间:以HF为例说明氢键的形成。在HF分子中,由于F的电负性(4.0)很大,共用电子对强烈偏向F原子一边,而H原子核外只有一个电子,其电子云向F原子偏移的结果,使得它几乎要呈质子状态。这个半径很小、无内层电子的带部分正电荷的氢原子,使附近另一个HF分子中含有负电子对并带部分负电荷的F原子有可能充分靠近它,从而产生静电吸引作用,这个静电吸引作用力就是所谓氢键,即F-H…F;②不同种分子间:不仅同种分子之间可以存在氢键,某些不同种分子之间也可能形成氢键.例如 NH3与H2O之间。所以这就导致了氨气在水中的惊人溶解度:1体积水中可溶解700体积氨气;(2)分子内氢键:某些分子内,例如HNO3、邻硝基苯酚分子可以形成分子内氢键,还有一个苯环上连有两个羟基,一个羟基中的氢与另一个羟基中的氧形成氢键,分子内氢键由于受环状结构的限制,X-H…Y往往不能在同一直线上,分子内氢键使物质熔沸点降低。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】SiH4是一种无色的气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O,已知室温下2gSiH4自燃放出热量89.2kJ,其热化学方程式为:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I-具有还原性,含碘食盐中的碘元素主要以KIO3的形式存在,I-、I2、IO3-在一定条件下可发生如图转化关系,下列说法不正确的是

A.用淀粉-KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为Cl2>IO3->I2
C.生产等量的碘,途径I和途径II转移电子数目之比为5 :2
D.途径III反应的离子方程式:3Cl2+I-+3H2O=6Cl-+IO3-+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
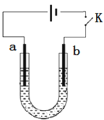
【题目】高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
c(NaOH) | 阴极现象 | 阳极现象 |
1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法正确的是( )
A.a为石墨,b为铁钉
B.阴极主要发生反应 4OH--4e-== O2↑+ 2H2O
C.高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-== FeO42-+ 4H2O
D.制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.NH3中氮原子的杂化方式为sp3杂化
B.[Cu(NH3)4]2+中,NH3是配体
C.NH4+、PH4+、CH4、BH4-互为等电子体
D.NH3的沸点比PH3的沸点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据反应2NaIO3+5SO2+4H2O=I2+3H2SO4+2NaHSO4,并利用下列装置从含NaIO3的废液中制取单质碘的CCl4溶液并回收NaHSO4。

其中装置正确且能达到实验目的的组合是( )
A.①②③④B.①②③
C.②④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某无机化合物的二聚分子结构示意图,该分子中A、B两种元素都是第3周期的元素,分子中所有原子的最外层都达到8个电子的稳定结构。下列说法不正确的是( )
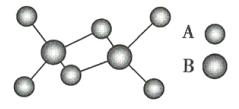
A.该物质的化学式是Al2Cl6B.该物质是离子化合物,在熔融状态下能导电
C.该物质在固态时所形成的晶体是分子晶体D.该物质中不存在离子键,也不含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是化学中常用的思维方法。下列推理正确的是
A.lmol晶体硅含Si-Si键的数目为2NA,则1mol金刚砂含C-Si键的数目也为2NA
B.Ca(HCO3)2溶液中加入过量的NaOH溶液,发生化学反应的方程式:![]()
则Mg(HCO3)2溶液中加入过量的NaOH溶液,发生化学反应的方程式: ![]()
C.标准状况下,22.4 L CO2中所含的分子数目为NA个,则22.4 LCS2中所含的分子数目也为NA个
D.NaClO溶液中通人过量CO2发生了反应:![]() ,则Ca(ClO)2溶液中通入过量CO2发生了:
,则Ca(ClO)2溶液中通入过量CO2发生了:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用乙醇制备溴乙烷:CH3CH2OH+HBr![]() CH3CH2Br+H2O,但通常采用溴化钠和浓硫酸与乙醇共热的方法。下面是某同学对该实验的猜想,你认为可能错误的是( )
CH3CH2Br+H2O,但通常采用溴化钠和浓硫酸与乙醇共热的方法。下面是某同学对该实验的猜想,你认为可能错误的是( )
A.制备过程中可能看到有气泡产生
B.可以将适量的NaBr、H2SO4(浓![]() 、CH3CH2OH三种药品置入一种容器中加热制备CH3CH2Br
、CH3CH2OH三种药品置入一种容器中加热制备CH3CH2Br
C.如在夏天做制备CH3CH2Br的实验,实际收集到的产物可能较少
D.为了除去CH3CH2Br中混有的HBr,可用热的NaOH溶液洗涤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com