
【题目】I-具有还原性,含碘食盐中的碘元素主要以KIO3的形式存在,I-、I2、IO3-在一定条件下可发生如图转化关系,下列说法不正确的是

A.用淀粉-KI试纸和食醋可检验食盐是否加碘
B.由图可知氧化性的强弱顺序为Cl2>IO3->I2
C.生产等量的碘,途径I和途径II转移电子数目之比为5 :2
D.途径III反应的离子方程式:3Cl2+I-+3H2O=6Cl-+IO3-+6H+
【答案】C
【解析】
A. KIO3、KI在酸性条件下发生氧化还原反应产生I2,I2遇淀粉溶液变为蓝色,因此可以用淀粉-KI试纸和食醋可检验食盐是否加碘,A正确;
B. 由途径I可知氧化性Cl2>I2,由途径II可知氧化性:IO3->I2,由途径III可知氧化性:Cl2>IO3-,故物质氧化性有强到弱的顺序为:Cl2>IO3->I2,B正确;
C. 假设反应产生1 molI2,途径I转移2 mol电子,途径II转移10 mol电子,因此生产等量的碘,途径I和途径II转移电子数目之比为2 :10=1:5,C错误;
D. 途径III中,Cl2把I-氧化为IO3-,Cl2被还原为Cl-,根据电子守恒、电荷守恒、原子守恒,可得反应的离子方程式:3Cl2+I-+3H2O=6Cl-+IO3-+6H+,D正确;
故合理选项是C。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】元素ⅹ位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子。X与Y形成的化合物的晶胞结构如图所示,下列关于该晶体的说法正确的是( )
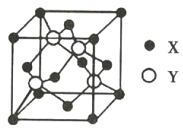
A.1个晶胞中所含离子总数为18
B.X2+的配位数为8,Y2-的配位数为4
C.与每个X2+距离最近且相等的X2+共有12个
D.该化合物的化学式为CaS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20mL0.1mol/LH2R溶液中滴加0.1mol/LNaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。已知pKa = –lgKa,二元弱酸H2R的pKa1=1.89,pKa2=7.21.下列有关说法错误的是
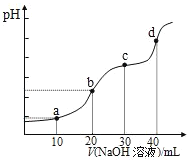
A.H2R + R22HR平衡常数K>105,反应趋于完全
B.常温下,Kh(HR-)的数量级为10-13
C.点b时,pH<7且 c(R2)·c(H+)<c(H2R)·c(OH)
D.点c时,溶液中2c(OH)-2c(H+)=3c(H2R)+ c(HR)-c(R2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推论错误的是
A.NaCl为离子晶体,可推测CsCl也为离子晶体
B.CO2晶体是分子晶体,可推测CS2晶体也是分子晶体
C.NH4+为正四面体结构,可推测PH4+也为正四面体结构
D.NCl3中N原子是sp3杂化,可推测BCl3中B原子也是sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前四周期的一部分,下列有关X、Y、Z、R、W五种元素的叙述中,错误的是
X | ||||
Y | Z | |||
R | W |
A.常压下五种元素的单质中,Y的沸点最高
B.元素电负性:X>Z>Y
C.基态原子中未成对电子数最多的是R
D.元素最高价氧化物对应的水化物酸性:W>Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1 mol·L1KOH溶液滴定10 mL 0.1 mol·L1 HA溶液的滴定曲线如图所示。下列说法不正确的是( )

A.a≈3,说明HA属于弱酸
B.水的电离程度:d点>c点
C.e点溶液中:c(K+)=2c(A-)+2c(HA)
D.b点溶液中粒子浓度大小:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.O3与SO2的结构相似
B.硫粉不溶于水,易溶于CS2中
C.Be(OH)2是两性氢氧化物
D.在相同条件下,![]() 的沸点高于
的沸点高于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是
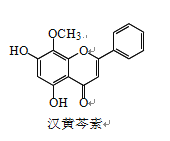
A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com