
 ��Һ���ֱ���ͬŨ�ȵ��ռ���Һ��Ӧ��Ҫʹ��Ӧ�����Һ�����ԣ������ռ���Һ�������ϵΪ_________________��
��Һ���ֱ���ͬŨ�ȵ��ռ���Һ��Ӧ��Ҫʹ��Ӧ�����Һ�����ԣ������ռ���Һ�������ϵΪ_________________�� �ۼ��εζ�����NaOH��Һ���������:
�ۼ��εζ�����NaOH��Һ���������:| ʵ����� | 1 | 2 | 3 | 4 |
| ����NaOH��Һ�����(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
 ϴ
ϴ
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������£�c(H+)/c(OH-)=1��10-12����Һ��I-��Cl-��HCO3-��Na+ |
| B�����д���Fe3+����Һ��Na+��HCO3-��NO3-��CO32- |
| C�����������ܲ�����������Һ��NH4+��Fe2+��SO42-��Cl- |
| D����ˮ�������c(H+)=1��10-12 mol?L��1��Һ�У�K+��Cl-��NO3-��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NO3����Cl����Fe2����Na�� | B��Ag����NO3����Cl����K�� |
| C��K����Ba2����OH����SO42�� | D��Cu2����NH4����Br����Cl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ں��д���HCO3�D����Һ�У�K+��Na+��Al3+��Br�� |
| B��ʹpH��ֽ��������Һ�У�NH4+��Na+��Cl����ClO�� |
C������O��1 mol��L-1Br�����ӵ���Һ�У� �� �� �� ��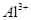 �� ��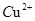 |
| D����ʹ���ȱ�����Һ�У�Na+��K+��SO2-4��AlO-2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | �� | �� | �� | �� |
| ��Һ | ��ˮ | ����������Һ | ������Һ | ���� |
| pH | 11 | 11 | 3 | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ں�K+�����ʾ�������ˮ���������ӷ���ʽ�в��ܳ���K+ |
| B������кͷ�Ӧ�����ӷ���ʽ���ɱ�ʾΪ��H+ +OH- ��H2O |
| C�����ӷ���ʽ���ߵ�Ԫ�����ࡢԭ�Ӹ���������������ʱ���÷���ʽһ����ȷ |
D����Һ�н��еķ�Ӧ��FeCl3 +3KSCN 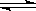 Fe(SCN)3 +3KCl�ﵽƽ��ʱ����������KCl���壬ƽ�ⲻ�ƶ� Fe(SCN)3 +3KCl�ﵽƽ��ʱ����������KCl���壬ƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na+��OH����S 2����ClO�� | B��H+��Na+��Fe2+��NO3�� �� | C��K+��Ba2+��OH����SO32�� | D��Na+��K+��Ba2+��OH- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com