
【题目】双酚A作为食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大.下列有关双酚A的叙述不正确的是( ) 
A.双酚A的分子式是C15H16O2
B.双酚A的核磁共振氢谱显示氢原子数之比是1:2:2:3
C.反应①中,1mol双酚A最多消耗2 mol Br2
D.反应②的产物中只有一种官能团
【答案】C
【解析】解:A.有结构简式可知分子中含有15个C原子、16个H原子、2个O原子,则分子式为C15H16O2 , 故A正确;
B.两个甲基相同,两个苯酚基相同,根据苯环的对称可知有4种不同的H,H原子数之比是2:4:4:6=1:2:2:3,故B正确;
C.双酚A中,2个酚羟基有4个邻位H可被取代,则1mol双酚A最多消耗4molBr2 , 故C错误;
D.加成反应后,产物的官能团只有﹣OH,故D正确.
故选C.
【考点精析】根据题目的已知条件,利用有机物的结构和性质的相关知识可以得到问题的答案,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解.


科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料和燃料。将CO2与含少量CO的H2混合,在恒容密闭容器中发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1是在两种投料比[c(CO2)/c(H2+CO)]分别为1:4 和1:6 时,CO2平衡转化率随温度变化的曲线,图2 是生成的甲醇/过氧化氢燃料电池的工作原理示意图:
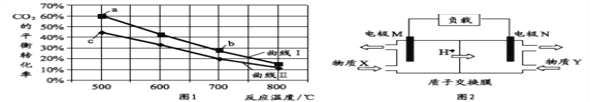
下列有关说法正确的是( )
A. 图2中电极M上发生还原反应
B. 图2中电极N的反应式:H2O2+2e+2H+=2H2O
C. 图1中b点对应的平衡常数K值大于c点
D. 图1中a点对应的H2的转化率等于30%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaCl2xH2O是用途广泛的基础化工产品。我国目前主要是用盐酸和硫化钡(含少量Mg2+、Fe3+等)反应生产BaCl2xH2O,工艺流程如下图所示。
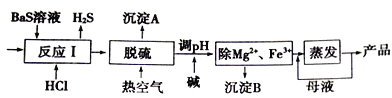
已知: 室温时Ksp[Mg(OH)2]= 1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38,请回答下列问题:
(1)写出氯化钡的电子式______,盐酸和硫化钡反应的化学方程式为___________。
(2)反应I中生成的H2S用足量氨水吸收,一定条件下向所得溶液中通入空气,可得到单质硫并使吸收液再生,吸收液再生反应的化学方程式为_______________________。
(3)沉淀A的成分是__________。
(4)热空气吹除时会有部分HS-转变为S2O32-,使产品仍达不到纯度要求,可再进行酸化脱硫,酸化脱硫时的离子方程式为________________。
(5)室温时,若加碱调溶液pH至9,则完全沉淀的离子是_____________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的沸点见附表).
附表:相关物质的沸点(101KPa)
物质 | 沸点/℃ | 物质 | 沸点/℃ |
溴 | 58.8 | 1,2﹣二氯乙烷 | 83.5 |
苯甲醛 | 179 | 间溴苯甲醛 | 229 |
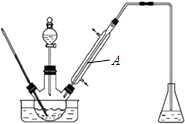
其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2﹣二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经H2SO4干燥过的液溴,保温反应一段时间,冷却.
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液.有机相用10%NaHCO3溶液洗涤.
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤.
步骤4:减压蒸馏有机相,收集相应馏分.
(1)实验装置A的名称是 , 锥形瓶中的溶液应为 .
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为;
(3)步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的(填化学式).
(4)步骤3中加入无水MgSO4固体的作用是 , 分离的方法是;
(5)步骤4中采用减压蒸馏技术,是为了防止 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列模型分别表示C2H2、S8、SF6的结构,下列说法错误的是( ) 
A.32 g S8分子中含有0.125 mol σ键
B.SF6是由极性键构成的非极性分子
C.1 mol C2H2分子中有3 mol σ键和2 mol π键
D.1 mol S8中含有8 mol S﹣S键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)E、F、G三种元素的原子序数依次增大,其原子的最外层电子排布均为4s1 . 则F元素在其化合物中最高化合价为 .
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4属于晶体;基态Ni原子的电子占有种能量不同的原子轨道.
(3)很多不饱和有机物在Ni催化下可以与H2发生加成反应.
如①CH2═CH2②CH≡CH③ ![]() ④
④ ![]() 等,其中C原子为sp2杂化的分子有(填序号),预测HCHO分子的立体结构为形.
等,其中C原子为sp2杂化的分子有(填序号),预测HCHO分子的立体结构为形.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在规定范围内使用食品添加剂,一般认为对人体健康无害,如果违反规定,均会损害人体健康.下列物质可用作食品防腐剂的是( )
A.甲醛
B.维生素E
C.柠檬酸
D.苯甲酸及其钠盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组探究SO2和Fe(NO3)3溶液的反应,其反应装置如下图所示:
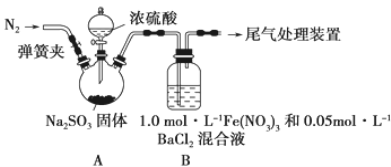
已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1(即c(H+)=0.1 mol·L-1),回答下列问题:
(1)装置A中反应的化学方程式是_____________________________________________
(2)滴加浓硫酸之前应打开弹簧夹向装置中通入一段时间的N2,目的是________________________________
(3)装置B中产生了白色沉淀,其成分是___________,说明SO2具有___________性。
(4)分析B中产生白色沉淀的原因:
猜想1:SO2与Fe3+、酸性条件下NO3-都反应;
猜想2:___________________;
猜想3:在酸性条件下SO2与NO3—反应;
①按猜想2,装置B中反应的离子方程式是 _____________________________________;
②按猜想3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是________________(填字母)。
A.1.5 mol·L-1Fe(NO3)2溶液
B.0.1 mol·L-1硝酸钠溶液
C.6.0 mol·L-1 NaNO3和0.2 mol·L-1盐酸等体积混合的溶液
D.3.0 mol·L-1 NaNO3和0.1 mol·L-1盐酸等体积混合的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有6种短周期元素,原子序数按E、D、B、A、F、C的顺序依次增大;A、C同周期,B、C同主族;A与B可形成离子化合物A2B,且离子的电子数均相同;D和E可形成4核10电子的分子;F是第三周期元素的简单离子中半径最小的。试回答下列问题(用相应的元素符号表示):
(1)写出B在元素周期表中的位置: _______________;C的原子结构示意图为_______________。
(2)B与E形成的化合物E2B2的电子式为__________;D和E形成4核10电子的分子的结构式为__________;A、B、E形成的化合物中存在的化学键____________________。
(3)元素A与元素F相比,金属性较弱的是________(用元素符号表示),写出实验室制备其最高价氧化物的水化物反应的离子方程式为____________________________________________。
(4)常压下1.6gC的单质在足量的空气中完全燃烧放出14.85kJ的热量,写出表示其燃烧热的热化学方程式_______________________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com