
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是坏境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(s)+O2(g) 2SO3(g).
2SO3(g).
某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
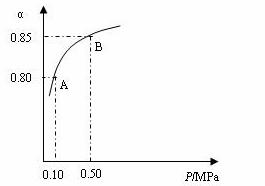
①将2.0 molSO2和1.0molO2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于__________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为__________(阿伏加德罗常数的值用NA表示),放出的热量为___________kJ。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:
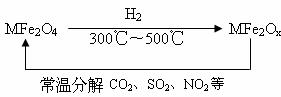
请写出MFe2Ox分解SO2的化学方程式________________(不必配平)。
【答案】
(1)①800L·mol-1
② =
(2)1.60NA(或1.6NA)
173.4
(3)MFe2Ox+SO2→MFe2O4+S
【解析】本题考查有关化学平衡的概念、计算、有关反应热的计算及氧化还原知识。由图象中的数据可计算平衡常数;(2)中计算是有关电子转移数目的计算。
(1)0.10 MPa时:c(SO2)=2 mol×(1-0.8)×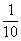 =0.04 mol·L-1
=0.04 mol·L-1
c(O2)=(1 mol-1.6 mol×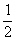 )×
)×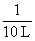 =0.02 mol·L-1
=0.02 mol·L-1
c(SO3)=1.6 mol×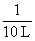 =0.16 mol·L-1
=0.16 mol·L-1
K=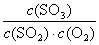 =
=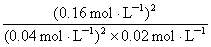 =800 L·mol-1
=800 L·mol-1
②由A到B,温度不变,只增大压强,K不变。
(2)本小题是有关氧化还原和反应热的计算,由 盖斯定律把两式相加,得2CH4(g)+4NO2(g)===2N2(g)+2CO2(g)+4H2O(g) ΔH=-1734 kJ·mol-1
盖斯定律把两式相加,得2CH4(g)+4NO2(g)===2N2(g)+2CO2(g)+4H2O(g) ΔH=-1734 kJ·mol-1
转移电子数: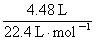 ×8=1.6 mol,故为1.6NA
×8=1.6 mol,故为1.6NA
放出热量:0.2 mol×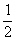 ×1 734 kJ·mol-1=173.4 kJ
×1 734 kJ·mol-1=173.4 kJ
(3)由于信息转化关系已确定,只要确定被分解物质的产物即可写出反应方程式。分解SO2由条件可推出SO2作氧化剂,只有还原为单质硫时才防止污染环境。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
分子式为C4H8O2的有机物在酸性条件下水解为酸和醇。若不考虑立体异构,
这些酸和醇重新组合可形成的酯共有
A.3种 B.6种 C.9种 D.12种
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中下列各物质间不能实现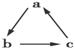 (“→”表示一步完成)转化的是 ( )
(“→”表示一步完成)转化的是 ( )
|
| A | B | C | D |
| a | CH3CH2OH | CH2===CH2 | Cl2 | C |
| b | CH3CHO | CH3CH2Br | HClO | CO |
| c | CH3COOH | CH3CH2OH | HCl | CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程 式是
式是
;
(2)PCl5分解成PCl3和Cl2的热化学方程式是
;
上述分解反应是一个可逆反应。温度T1时,在密闭容器中加入0.80mol PCl5,反应达平衡时PCl5还剩0.60 mol,其分解率α1等于 ;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2 α1(填“大于”、“小于”或“等于”);
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是________________________
(4)P和Cl2分两步反应生成1mol PCl5的△H3=____________,P和Cl2一步反应生成1molPCl5的△H4__________△H3(填“大于”、“小于”或“等于”)。
(5)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
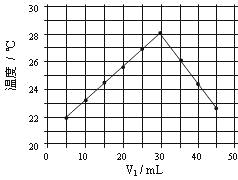
A 做该实验时环境温度为22℃
B 该实验表明化学能可能转化为热能
C NaOH溶液的浓度约为1.0mol/L
D 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①101kPa时,2C(s)+O2(g)==2CO(g);ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)==H2O(l);ΔH=-57.3 kJ/mol
下列结论正确的是
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P akJ·mol-1、P-O bkJ·mol-1、P=O ckJ·mol-1、O=O dkJ·mol-1
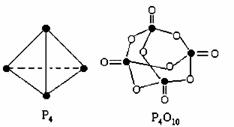
根据图示的分子结构和有关数据估算该反应的 H,其中正确的是
H,其中正确的是
A.(6a+5d-4c-12b) kJ·mol-1
B.(4c+12b-6a-5d) kJ·mol-1
C.(4c+12b-4a-5d) kJ·mol-1
D.(4a+5d-4c-12b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
A.根据纯净物的元素组成,将纯净物分为单质和化合物
B.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类
查看答案和解析>>
科目:高中化学 来源: 题型:
高纯 是制备高性能磁性材料的主要原料。实验室以
是制备高性能磁性材料的主要原料。实验室以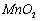 为原料制备少量高纯
为原料制备少量高纯 的操作步骤如下:(1)制备
的操作步骤如下:(1)制备 溶液:
溶液:
在烧瓶中(装置见右图)加入一定量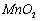 和水,搅拌,通入
和水,搅拌,通入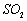 和
和 混合气体,反应3h。停止通入
混合气体,反应3h。停止通入 ,继续反应片刻,过滤(已知
,继续反应片刻,过滤(已知 )。
)。
①石灰乳参与反应的化学方程式为 。

 ②反应过程中,为使
②反应过程中,为使 尽可能转化完全,在通入
尽可能转化完全,在通入 和
和 比例一定、不改变固液投料的条件下,可采取的合理措施有 、 。
比例一定、不改变固液投料的条件下,可采取的合理措施有 、 。
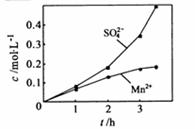
③若实验中将 换成空气,测得反应液中
换成空气,测得反应液中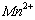 、
、 的浓度随反应时间t变化如右图。导致溶液中
的浓度随反应时间t变化如右图。导致溶液中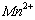 、
、 浓度变化产生明显差异的原因是 。
浓度变化产生明显差异的原因是 。
(2)制备高纯 固体:已知
固体:已知 难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;
难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;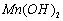 开始沉淀时
开始沉淀时 。请补充由(1)制得的
。请补充由(1)制得的 溶液制备高纯
溶液制备高纯 的操作步骤[实验中可选用的试剂:
的操作步骤[实验中可选用的试剂:  、
、 、
、  、
、 ]。
]。
① ;② ;③ ;④ ;⑤低于100℃干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com