
【题目】I.二甲醚(DME)水蒸气重整制氢是一种有效解决氢源的方案,其包含的化学反应有:

(1)已知某些化学键的键能数据如下表所示:

请据此书写二甲醚(DME)水蒸气重整制氢的总反应的热化学方程式:_____。
(2)对于反应①,一定温度下,在一个 2L 的恒压密闭容器中充人 0.1 mol CH3OCH3(g)和 0.2 mol H2O(g)发生该反应,经过 10 min 反应达到平衡,此时CH3OCH3 ( g)与 CH30H(g)的分压之比为 3:4,则用 CH3OH(g)表示的平均反应速率为_________用分压计算表示该反应的平衡常数 Kp= ______保留两位小数)。(提示:某气体分压=总压×![]()
(3)将中间产物 CH3OH 氧化可制得 HCOOH。常温下,已知 HCOOH 的电离常数 Ka=1.8×10,,则物质的量浓度相同的 HCOOH 与 HCOONa 的混合溶液中,各粒子浓度 (不含 H2O)由大到小的顺序是_____。
(4)已知反应:HCOOH(过量)+K2C2O4 =KHC2O4+HCOOK; KHC2O4+CH3COOK =K2C2O4+CH3COOH。H2C204 的一、二级电 离常数分别记为 K1、K2,HCOOH、 CH3COOH 的电离常数分别记为 K3、K4,则 K1、K2、K3、K4 从大到小的排列顺序为____。
Ⅱ.图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,电解质通过泵不断 在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜;放电前,被膜隔开的电解质为 Na2S2 和 NaBr3,放电后,分别变为 Na2S4 和NaBr。

(1)写出电池放电时,负极的电极反应式:_____。
(2)电池中离子选择性膜宜采用_____(填“阳”或“阴”)离子交换膜。
(3)已知可溶性硫化物在溶液中能与硫单质反应,生成可溶性的多硫化物 Na2Sx。若通过加入 FeCl3 与 Na2S, 溶液作用获得单质 S,其离子方程式为_____。
【答案】(1)CH3OCH3(g)+3H2O(g)=2CO2(g)+6H2(g)![]() H3=+289.98KJ/mol (2)0.004mol.L-1.min-1 (3)0.17。 (4)c(HCOO-)>c(Na+)>c(HCOOH)>c(H+)>c(OH-) (5)K1>K3>K2>K4 (6)2S22--2e-= S42- (7) 阳 (8)2Fe3++Sx2-=2 Fe2++xS
H3=+289.98KJ/mol (2)0.004mol.L-1.min-1 (3)0.17。 (4)c(HCOO-)>c(Na+)>c(HCOOH)>c(H+)>c(OH-) (5)K1>K3>K2>K4 (6)2S22--2e-= S42- (7) 阳 (8)2Fe3++Sx2-=2 Fe2++xS
【解析】
(1) 反应H2O(g)+CO(g)CO2(g)+H2(g),焓变![]() H3=2
H3=2![]() 463KJ/mol+1070KJ/mol-2
463KJ/mol+1070KJ/mol-2![]() 801 KJ/mol -436 KJ/mol =+42 KJ/mol ;二甲醚水蒸气重整制氢是一种有效解决氢源的方案,根据已知反应的方程式再结合盖斯定律用 (1)+(2)+(3)
801 KJ/mol -436 KJ/mol =+42 KJ/mol ;二甲醚水蒸气重整制氢是一种有效解决氢源的方案,根据已知反应的方程式再结合盖斯定律用 (1)+(2)+(3)![]() 2计算得到:CH3OCH3(g)+3H2O(g)=2CO2(g)+6H2(g)
2计算得到:CH3OCH3(g)+3H2O(g)=2CO2(g)+6H2(g)![]() H3=+289.98KJ/mol;本题答案为:CH3OCH3(g)+3H2O(g)=2CO2(g)+6H2(g)
H3=+289.98KJ/mol;本题答案为:CH3OCH3(g)+3H2O(g)=2CO2(g)+6H2(g)![]() H3=+289.98KJ/mol。
H3=+289.98KJ/mol。
(2)已知CH3OCH3(g)+H2O(g)2CH3OH(g),一定温度下在一2L密闭容器中充入0.1mol CH3OCH3(g)和0.2mol H2O(g)发生该反应,根据化学平衡三段式列式,设反应甲醚物质的量为x;
CH3OCH3(g)+ H2O(g)2CH3O(g),
起始量(mol) 0.1 0.2 0
变化量(mol) x x 2x
平衡量 (mol) (0.1-x) 0.2-x 2x
经过10min达到平衡, 此时CH3OCH3 ( g)与 CH30H(g)的分压之比为 3:4,(0.1-x)/2x=3/4,所以x=0.04mol。则CH3OH(g)表示的平均反应速率为V=2![]() 0.04mol/2L
0.04mol/2L![]() 10min=0.004mol.L-1.min-1;用分压计算表示该反应的平衡常数 Kp=(2
10min=0.004mol.L-1.min-1;用分压计算表示该反应的平衡常数 Kp=(2![]() 0.04mol/2L)2/
0.04mol/2L)2/![]() =0.17因此,本题正确答案是:0.004mol.L-1.min-1 0.17。
=0.17因此,本题正确答案是:0.004mol.L-1.min-1 0.17。
(3)因为HCOOH的Ka=1.8×10-4,所以甲酸为弱酸,HCOONa 为可溶性的强电解质,所以HCOOH和HCOONa的混合溶液中离子浓度由大到小的是c(HCOO-)>c(Na+)>c(HCOOH)>c(H+)>c(OH-)。
(4)由反应:HCOOH(过量)+K2C2O4=KHC2O4+HCOOK,知道酸性由强到弱的顺序为H2C2O4>HCOOH> HC2O4- ,由KHC2O4+CH3COOK =K2C2O4+CH3COOH可知,酸性HC2O4-> CH3COOH 。因为H2C204 的一、二级电离常数分别记为 K1、K2,HCOOH、 CH3COOH 的电离常数分别记为 K3、K4,则 K1、K2、K3、K4 从大到小的排列顺序为K1>K3>K2>K4。答案为:K1>K3>K2>K4。
II(1)电池放电时为原电池,Na2S2放电失电子做负极,则负极的电极反应式为2S22--2e-= S42- 。答案:2S22--2e-= S42- 。
(2) 因为负极的电极反应式为2S22--2e-= S42- ,反应中阴离子数目减少,而正极的阴离子增多,根据溶液呈电中性的原理,电池中离子选择性膜宜采用阳离子交换膜。答案:阳。
(3)已知可溶性硫化物在溶液中能与硫单质反应,生成可溶性的多硫化物 Na2Sx。若通过加入 FeCl3 与 Na2S, 溶液作用获得单质 S,根据电子守恒其离子方程式为2 Fe3++Sx2-=2 Fe2++xS。


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】由CO2、H2、CO组成的混合气在同温同压下与氮气的密度相同,则该混合气中CO2、H2、CO的体积比是( )
A. 26:8:1 B. 22:1:14 C. 13:8:7 D. 26:6:17
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。m、p、q、r、s是由这些元素组成的二元化合物,常温常压下r为液体,其余均为无色气体。m的摩尔质量为p的2倍,n是元素Y的单质,是绿色植物光合作用产生的无色气体;p物质能使湿润的红色石蕊试纸变蓝,q能使品红溶液褪色。上述物质的转化关系如图所示。下列说法正确的是( )
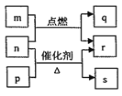
A. q与s均为酸性氧化物
B. Z的含氧酸是一种强酸
C. X、Y分别与W形成10e-的微粒能反应生成一种气体
D. 原子半径:X<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是 ( )
A. 35Cl和37Cl的原子结构示意图均为![]()
B. HC1O的电子式:![]()
C. CO2的比例模型: ![]()
D. 乙烯的结构式:CH2=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同物质的量浓度的 HC1 溶液,分别滴定物质的量浓度均为 0.1 mol/L 的三种碱溶液,滴定 曲线如图所示。下列判断正确的是

A. 滴定前,三种碱溶液中水电离出的 c(H+)大小关系: DOH>BOH>AOH
B. pH= 7 时,c(A+)=c(B+)=c(D+)
C. 滴定至 P 点时,溶液中:c(Cl-)>c(B+)>c(BOH)>c(OH-)>c(H+)
D. 当中和百分数达 100%时,将三种溶液混合后:c(AOH)+c(BOH)+c(DOH)=c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关1mol·L-1硫酸溶液的说法正确的是
A.1L水中含有1mol硫酸
B.1L溶液中含1molH+
C.将98g硫酸溶于1L水所配成的溶液
D.从1L溶液中取出500mL后,剩余溶液的浓度仍为1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学- 选修 5:有机化学基础]白花丹酸具有镇咳祛痰的作用,其合成路线流程图如下:

(1)写出 B 中含氧官能团的名称_____。
(2)写出 A→B 的化学方程式_____ 。
(3) C 的分子式为_____。C→D、E→F 的反应类型分别为_____和_____。
(4)白花丹酸分子中混有 ,写出同时满足下列条件的该有机物的一种同分 异构体的结构简 式_____。①分子中有四种不同化学环境的氢原子;②与 FeCl3 溶液能发生显色反应,且 1mol 该物质最多能与3 mol NaOH 反应。
,写出同时满足下列条件的该有机物的一种同分 异构体的结构简 式_____。①分子中有四种不同化学环境的氢原子;②与 FeCl3 溶液能发生显色反应,且 1mol 该物质最多能与3 mol NaOH 反应。
(5)某物 G 是 A 的同分异构体,满足下列条件的 G 的同分异构体有_____种。
①与三氯化铁溶液发生显色反应。 ②苯环上有两个取代基
(6) 已知:![]() ,根据已有知识并结合相关信息写出以
,根据已有知识并结合相关信息写出以
![]() 为原料制备
为原料制备 的合成路线流 程图 (合成路线流程图示例参考本题题干)_____。
的合成路线流 程图 (合成路线流程图示例参考本题题干)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1mol/L的是( )
A. 含Na+为2mol的Na2SO4溶液
B. 将80g SO3溶于水并配成1L的溶液
C. 将0.5mol/L的某饱和溶液100mL,加热蒸发掉50g水后的溶液
D. 将58.5gNaCl溶于1L水所得的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学需要借助化学专用术语来描述,下列有关化学用语的使用正确的是( )
A. NH4Cl的电子式:![]() B. S2–的结构示意图:
B. S2–的结构示意图: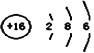
C. CO2的结构式:O=C=OD. 中子数为20的氯原子:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com