
【题目】室温下,用相同物质的量浓度的 HC1 溶液,分别滴定物质的量浓度均为 0.1 mol/L 的三种碱溶液,滴定 曲线如图所示。下列判断正确的是

A. 滴定前,三种碱溶液中水电离出的 c(H+)大小关系: DOH>BOH>AOH
B. pH= 7 时,c(A+)=c(B+)=c(D+)
C. 滴定至 P 点时,溶液中:c(Cl-)>c(B+)>c(BOH)>c(OH-)>c(H+)
D. 当中和百分数达 100%时,将三种溶液混合后:c(AOH)+c(BOH)+c(DOH)=c(H+)-c(OH-)
【答案】D
【解析】
试题三种碱的起始浓度均为0.1mol/L,由图中信息可知,起始时pH都小于13,说明三种碱均为弱碱,且碱性强弱为AOH<BOH<DOH,碱性越强,对水的电离的抑制作用越大。在相同条件下,盐水解的程度由小到大的顺序是DCl<BCl<ACl,它们水解均使溶液显酸性。A.滴定前,三种碱液中水电离的c(H+)大小关系为AOH>BOH>DOH,A不正确;B.滴定至P点时,此时中和百分数为50%,即BOH恰好有一半被中和,溶液为物质的量浓度相同的BOH和BCl混合溶液,pH>7、溶液显碱性,则BOH的电离程度大于BCl的水解程度,所以溶液中c(Cl-)<c(B+), B不正确;C.pH=7时,溶液中c(H+)=c(OH﹣),由电荷守恒可知,三种溶液中c(Cl-)均等于其c(弱碱的阳离子)。由于三种盐在相同的条件下的水解程度由小到大的顺序是DCl<BCl<ACl,且其水解均使溶液显酸性,则滴定到溶液恰好呈中性时,三种溶液中消耗HCl的体积由小到大的顺序为AOH<BOH<DOH,则三种溶液中c(Cl﹣)不相等,且c(Cl﹣)由小到大的顺序为AOH<BOH<DOH,因而c(A+)<c(B+)<c(D+),故C不正确;D.当中和百分数达100%时,三种溶液的物质的量浓度相同,混合后,根据质子守恒,c(DOH)+c(AOH)+c(BOH)+c(OH﹣)=c(H+),则c(AOH)+c(BOH)+c(DOH)=c(H+)﹣c(OH﹣),故D正确。本题选D。


科目:高中化学 来源: 题型:
【题目】以下物质间的每步转化通过一步反应能实现的是( )
A. Al-Al2O3-Al(OH)3-NaAlO2 B. Si-SiO2-H2SiO3-Na2SiO3
C. Cu-CuO-Cu(OH)2-CuSO4 D. Na-Na2O2-Na2CO3-NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某学习小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
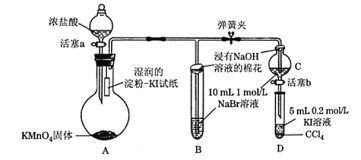
实验过程:
Ⅰ. 打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ. 当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ. 当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
回答问题:
(1)A中产生黄绿色气体,其电子式是_____。实验室在加热条件下制取该气体的离子方程式为_______。
(2)验证氯气的氧化性强于碘单质的实验现象是____________。
(3)C中溶液发生反应的离子方程式是_______________。
(4)过程Ⅲ实验的目的:甲同学认为试管B的作用就是吸收尾气,防止多余Cl2污染空气,因此B中盛装的最佳试剂应该为________。
乙同学经分析认为,B中溶液由黄色变为棕红色,发生反应的化学方程式为____________,以此说明C中_________,从而得出D中氧化I-的氧化剂必为Br2,因此B装置是必不可少的。
(5)过程Ⅳ为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下试管D震荡,静置,观察到的现象为___________,发生反应的离子方程式为_________。
(6)氯、溴、碘单质的氧化性逐渐减弱的本质原因:同主族元素从上到下_________,得电子能力逐渐减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。回答下列问题:
W | X | |||
Y | Z |
(1)X在元素周期表中的位置为____;画出X的简单离子结构示意图____。已知X元素的一种原子,其中子数为10,写出这种原子的原子符号_______。
(2)四种元素简单离子的半径由大到小为______(用离子符号表达)。
(3)W、X的最简单氢化物稳定性为____>____(填化学式)。
(4)Z最高价氧化物的水化物与Y最高价氧化物对应水化物反应的化学方程式为___ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关乙炔的说法不正确的是( )
A.燃烧时有浓厚的黑烟
B.实验室制乙炔时可用CuSO4除杂质气体
C.为了减缓电石和水的反应速率,可用饱和食盐水来代替
D.乙炔的收集方法可用排空气法收集
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.二甲醚(DME)水蒸气重整制氢是一种有效解决氢源的方案,其包含的化学反应有:

(1)已知某些化学键的键能数据如下表所示:

请据此书写二甲醚(DME)水蒸气重整制氢的总反应的热化学方程式:_____。
(2)对于反应①,一定温度下,在一个 2L 的恒压密闭容器中充人 0.1 mol CH3OCH3(g)和 0.2 mol H2O(g)发生该反应,经过 10 min 反应达到平衡,此时CH3OCH3 ( g)与 CH30H(g)的分压之比为 3:4,则用 CH3OH(g)表示的平均反应速率为_________用分压计算表示该反应的平衡常数 Kp= ______保留两位小数)。(提示:某气体分压=总压×![]()
(3)将中间产物 CH3OH 氧化可制得 HCOOH。常温下,已知 HCOOH 的电离常数 Ka=1.8×10,,则物质的量浓度相同的 HCOOH 与 HCOONa 的混合溶液中,各粒子浓度 (不含 H2O)由大到小的顺序是_____。
(4)已知反应:HCOOH(过量)+K2C2O4 =KHC2O4+HCOOK; KHC2O4+CH3COOK =K2C2O4+CH3COOH。H2C204 的一、二级电 离常数分别记为 K1、K2,HCOOH、 CH3COOH 的电离常数分别记为 K3、K4,则 K1、K2、K3、K4 从大到小的排列顺序为____。
Ⅱ.图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,电解质通过泵不断 在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜;放电前,被膜隔开的电解质为 Na2S2 和 NaBr3,放电后,分别变为 Na2S4 和NaBr。

(1)写出电池放电时,负极的电极反应式:_____。
(2)电池中离子选择性膜宜采用_____(填“阳”或“阴”)离子交换膜。
(3)已知可溶性硫化物在溶液中能与硫单质反应,生成可溶性的多硫化物 Na2Sx。若通过加入 FeCl3 与 Na2S, 溶液作用获得单质 S,其离子方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A. 20gD2O与20g氖气所含有的电子数相同
B. 标准状况下,22.4L二氯甲烷的分子数约为NA
C. 常温常压下,100g 17%的双氧水溶液中含有氧原子总数为NA
D. 56g铁与一定量的氯气在一定条件下充分反应,转移的电子数一定为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有HCl气体,另—个盛有H2和Cl2的混合气体。在同温同压下, 两容器内的气体一定具有相同的( )
A. 原子数 B. 密度 C. 质量 D. 质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究反应2X(g)![]() Y(g)+Z(g)的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物X的浓度(molL-1)随反应时间(min)的变化情况如图所示。
Y(g)+Z(g)的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物X的浓度(molL-1)随反应时间(min)的变化情况如图所示。

下列说法不正确的是
A. 比较实验②、④得出:升高温度,化学反应速率加快
B. 比较实验①、②得出:增大反应物浓度,化学反应速率加快
C. 若实验②、③只有一个条件不同,则实验③使用了催化剂
D. 在0~10min之间,实验②的平均速率v(Y)=0.04molL-1min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com