
【题目】为验证卤素单质氧化性的相对强弱,某学习小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
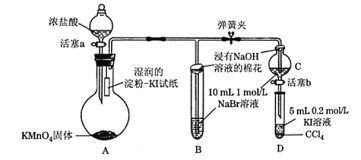
实验过程:
Ⅰ. 打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ. 当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ. 当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
回答问题:
(1)A中产生黄绿色气体,其电子式是_____。实验室在加热条件下制取该气体的离子方程式为_______。
(2)验证氯气的氧化性强于碘单质的实验现象是____________。
(3)C中溶液发生反应的离子方程式是_______________。
(4)过程Ⅲ实验的目的:甲同学认为试管B的作用就是吸收尾气,防止多余Cl2污染空气,因此B中盛装的最佳试剂应该为________。
乙同学经分析认为,B中溶液由黄色变为棕红色,发生反应的化学方程式为____________,以此说明C中_________,从而得出D中氧化I-的氧化剂必为Br2,因此B装置是必不可少的。
(5)过程Ⅳ为:打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下试管D震荡,静置,观察到的现象为___________,发生反应的离子方程式为_________。
(6)氯、溴、碘单质的氧化性逐渐减弱的本质原因:同主族元素从上到下_________,得电子能力逐渐减弱。
【答案】![]() MnO2+4H++2Cl-
MnO2+4H++2Cl-![]() Mn2+ +2H2O+Cl2↑ 淀粉KI试纸变蓝 Cl2+2Br-=Br2+2Cl- NaOH溶液 Cl2+2 NaBr=Br 2+2NaCl Br-过量,溶液中没有Cl2 试管中溶液分层,下层溶液呈紫红色 Br 2+2I-=I2+2Br- 电子层数逐渐增多,原子半径逐渐增大
Mn2+ +2H2O+Cl2↑ 淀粉KI试纸变蓝 Cl2+2Br-=Br2+2Cl- NaOH溶液 Cl2+2 NaBr=Br 2+2NaCl Br-过量,溶液中没有Cl2 试管中溶液分层,下层溶液呈紫红色 Br 2+2I-=I2+2Br- 电子层数逐渐增多,原子半径逐渐增大
【解析】
A中滴加浓盐酸后,发生反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,生成黄绿色气体Cl2,在A、B、C中分别发生反应:Cl2+2KI=2KCl+I2,Cl2+2NaBr=2NaCl+Br2,Cl2+2NaBr=2NaCl+Br2,由于B、C中生成了Br2而使溶液变为黄色,打开活塞b,C中生成的Br2在D中发生反应:Br2+2KI=2KBr+I2。过程Ⅲ实验,当B中黄色溶液继续通入过量Cl2时,溶液变为红棕色,以此为对照,说明C中黄色溶液无Cl2,从而排除Cl2对溴置换碘实验的干扰,据此答题。
(1)A中产生黄绿色气体为氯气,氯原子间形成1对共用电子对,电子式为:![]() ,实验室用二氧化锰与浓盐酸在加热条件下反应制取氯气,离子方程式为MnO2+4H++2Cl-
,实验室用二氧化锰与浓盐酸在加热条件下反应制取氯气,离子方程式为MnO2+4H++2Cl-![]() Mn2+ +2H2O+Cl2↑,故答案为:
Mn2+ +2H2O+Cl2↑,故答案为:![]() ,MnO2+4H++2Cl-
,MnO2+4H++2Cl-![]() Mn2+ +2H2O+Cl2↑。
Mn2+ +2H2O+Cl2↑。
(2)因Cl2的氧化性大于I2的氧化性,可发生反应:Cl2+2I-=I2+2Cl-,I2能使淀粉变蓝;故答案为:淀粉KI试纸变蓝。
(3)因Cl2的氧化性大于Br2的氧化性,可发生反应:Cl2+2Br-=Br2+2Cl-,故答案为:Cl2+2Br-=Br2+2Cl-。
(4)Cl2是有毒的酸性气体,应用碱液吸收,因此B中盛装的最佳试剂应该为NaOH溶液,为防止多余Cl2污染空气;B中溶液由黄色变为棕红色,说明生成了Br2,发生反应的化学方程式为Cl2+2NaBr=Br2+2NaCl,以此说明C中Br-过量,溶液中没有Cl2,从而得出D中氧化I-的氧化剂必为Br2,故答案为:NaOH溶液,Cl2+2NaBr=Br2+2NaCl,Br-过量,溶液中没有Cl2。
(5)打开活塞b,将少量C中溶液滴入D中,发生反应:Br2+2I-=I2+2Br-,关闭活塞b,取下D震荡,静至后CCl4层溶液变为紫(或紫红)色,故答案为:试管中溶液分层,下层溶液呈紫红色,Br 2+2I-=I2+2Br-。
(6)因同一主族元素,从上到下,电子层数依次增多,原子半径逐渐增大,元素的非金属性逐渐减弱,得电子能力逐渐减弱;故答案为:电子层数依次增多,原子半径逐渐增大.


科目:高中化学 来源: 题型:
【题目】下列化学用语表达正确的是:
A. HCl 的电子式:![]() B. F-结构示意图:
B. F-结构示意图: ![]()
C. H2 燃烧的热化学方程式: 2H2 (g) + O2 (g) = 2H2O (g) △H = - 571.6 kJ·mol-1D. Cl2 与水反应的离子方程式: Cl2 + H2O = 2H+ +Cl- + ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①增大浓度,或加热或加压,或使用催化剂,一定可以加快反应速率.
②气态氢化物的稳定性:H2O>NH3>SiH4
③如图所示实验可证明元素的非金属性:Cl>C>Si
|
④用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
A. ①②B. ②③C. ③④D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是

A. 该分子中含有1个手性碳原子
B. 1mol乙酰紫草素最多可与2mol NaOH反应
C. 1mol 乙酰紫草素最多可与2mol Br2反应
D. 能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气净化器中发生的反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定温度下,在三个体积均为1.0L恒容密闭容器中发生上述反应,测得有关实验数据如下:
容器 | 温度/(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | ||||
NO | CO | N2 | CO2 | N2 | CO2 | ||
I | 400 | 0.2 | 0.2 | 0 | 0 | 0.12 | |
II | 400 | 0.4 | 0.4 | 0 | 0 | ||
III | 300 | 0 | 0 | 0.1 | 0.2 | 0.075 | |
下列说法正确是
A. 容器I中达到平衡所需时间2s,则v(N2)=0.06 molL-1·s-1
B. 该反应的ΔS<0、ΔH<0
C. 达到平衡时,体系中c(CO)关系:c(CO,容器II)>2c(CO,容器I)
D. 若起始时向I中充入NO、CO、N2、CO2各0.1mol,开始时V正>V逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。m、p、q、r、s是由这些元素组成的二元化合物,常温常压下r为液体,其余均为无色气体。m的摩尔质量为p的2倍,n是元素Y的单质,是绿色植物光合作用产生的无色气体;p物质能使湿润的红色石蕊试纸变蓝,q能使品红溶液褪色。上述物质的转化关系如图所示。下列说法正确的是( )
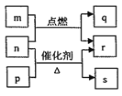
A. q与s均为酸性氧化物
B. Z的含氧酸是一种强酸
C. X、Y分别与W形成10e-的微粒能反应生成一种气体
D. 原子半径:X<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值。
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:
FeCl3+2NH2OHHCl= 4FeCl2+N2O↑+6HCl+H2O
① Fe3+在基态时,核外电子排布式_____;
② 羟胺中(NH2OH)采用sp3杂化的原子有______,三种元素电负性由大到小的顺序为______;
③ Fe2+与邻啡罗啉(用A表示)形成的配合物[FeA3] 2+中,Fe2+的配位数为____;
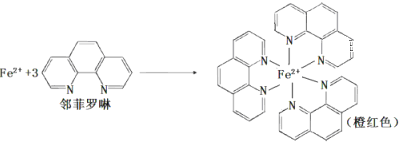
④N2O分子的空间构型为______(用文字描述)。
(2)氢的规模化制备是氢能应用的基础。在光化学电池中,以紫外线照钛酸锶电极时,可产生电流。钛酸锶晶体结构如图所示,则钛酸锶的化学式为_____。
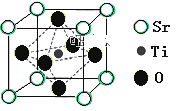
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同物质的量浓度的 HC1 溶液,分别滴定物质的量浓度均为 0.1 mol/L 的三种碱溶液,滴定 曲线如图所示。下列判断正确的是

A. 滴定前,三种碱溶液中水电离出的 c(H+)大小关系: DOH>BOH>AOH
B. pH= 7 时,c(A+)=c(B+)=c(D+)
C. 滴定至 P 点时,溶液中:c(Cl-)>c(B+)>c(BOH)>c(OH-)>c(H+)
D. 当中和百分数达 100%时,将三种溶液混合后:c(AOH)+c(BOH)+c(DOH)=c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种关于酸的使用,其中正确的是
A. 为了抑制Fe2+的水解,用稀硝酸酸化 B. 检验溶液中是否含有SO42—时,先用盐酸酸化
C. 检验氯乙烷中的氯元素,水解后再用硫酸酸化 D. 为了增强KMnO4溶液的氧化能力,用浓盐酸酸化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com