
 3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。
3Na2S2O3+CO2。设计如下装置(夹持仪器省略)进行实验。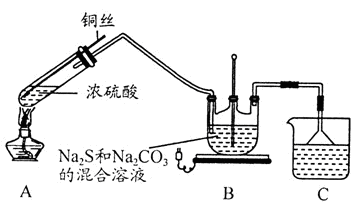
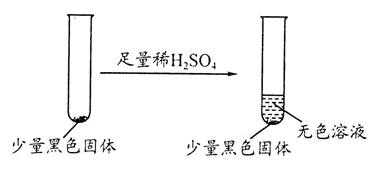

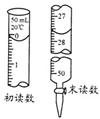
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O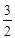 I2 -3 S2O32一;n(Ba2+)=
I2 -3 S2O32一;n(Ba2+)=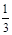 ×27.50×10-3L×0.0030mol·L-1=2.75×10-5mol,Ba2+的浓度为:
×27.50×10-3L×0.0030mol·L-1=2.75×10-5mol,Ba2+的浓度为: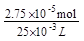 =1.1×10-3mol·L-1。
=1.1×10-3mol·L-1。

科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
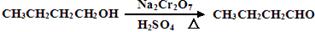 。反应物和产物的相关数据列表如下:
。反应物和产物的相关数据列表如下:| | 沸点/℃ | 密度/g·cm-3 | 水中溶解性 |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
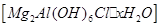 是一种新型离子交换材料,其在高温下完全分解为
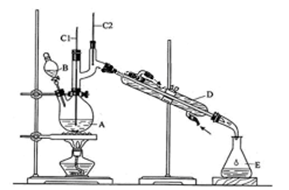
是一种新型离子交换材料,其在高温下完全分解为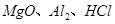 和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。
和水蒸气,现用题27图装置进行试验确定其化学式(固定装置略去)。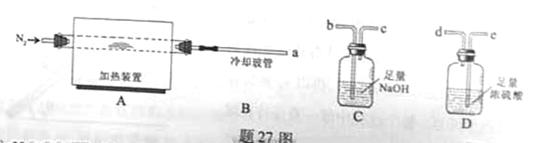
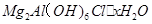 热分解的化学方程式为 。
热分解的化学方程式为 。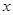 ,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。
,则装置的连接顺序为 (按气流方向,用接口字母表示),其中C的作用是 。装置连接后,首先要进行的操作名称是 。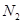 排尽装置中的空气,称取C、D的初始质量后,再持续通入
排尽装置中的空气,称取C、D的初始质量后,再持续通入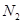 的作用是 、 等.
的作用是 、 等.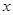 = .若取消冷却玻管B后进行试验,测定
= .若取消冷却玻管B后进行试验,测定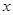 值将 (填“偏高”或“偏低”)
值将 (填“偏高”或“偏低”)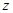 ,除测定D的增重外,至少还需测定 .
,除测定D的增重外,至少还需测定 .查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.0.5 mol·L-1氯化亚铁溶液 | B.0.5 mol·L-1氯化铜溶液 |
| C.0.5 mol·L-1盐酸 | D.0.5 mol·L-1氯化亚铁和0.5 mol·L-1氯化铜混合溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
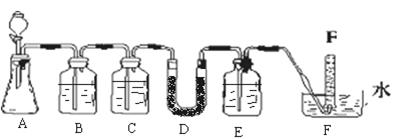
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | | 除去CO2中的水蒸气 |
| E | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
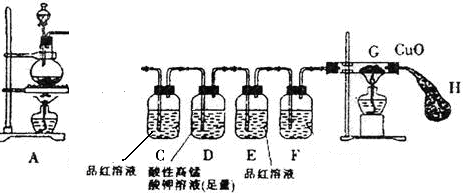
| 实验现象 | 结论及解释 | |
| ①将铁钉(足量)加入烧瓶中,再向其中滴加含amolH2SO4的浓硫酸溶液 | 未见明显现象 | 原因: 。 |
| ②点燃A、G处酒精灯 | 片刻后,烧瓶中溶液的颜色发生变化,并有气泡产生。C中溶液颜色 ,E中溶液未见明显变化。一段时间后,黑色的CuO变成了红色,此时E装置溶液颜色仍未有颜色变化 | 烧瓶中发生的所有反应 的化学方程式: 说明产生的SO2气体完全被D中溶液吸收 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com