
【题目】(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,

请写出N2和H2反应的热化学方程式:______________________________________________;
(2)若已知下列数据:
化学键 | H-H | N≡N |
键能/kJ mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能____________kJ mol-1
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后的变化是:E1_______,△H________ (填“增大”、“减小、” “不变”)。
(4)用NH3催化还原NO2还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H1=akJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=bkJ·mol-1
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=_________kJ/mol (用含a、b的式子表示)
【答案】 N2(g)+3H2(g)![]() 2NH3(g)△H=-92kJmol-1 390 减小 不变 (a-3b)/4
2NH3(g)△H=-92kJmol-1 390 减小 不变 (a-3b)/4
【解析】试题分析:本题考查反应热的计算,盖斯定律的应用。
(1)由图可见反应物的总能量大于生成物的总能量,该反应为放热反应,反应生成1molNH3(g)的ΔH=E1-E2=(254-300)kJ/mol=-46kJ/mol,N2和H2反应生成1molNH3(g)的热化学方程式为1/2N2(g)+3/2H2(g)![]() NH3(g)ΔH=-46kJmol-1。N2和H2反应的热化学方程式为N2(g)+3H2(g)
NH3(g)ΔH=-46kJmol-1。N2和H2反应的热化学方程式为N2(g)+3H2(g)![]() 2NH3(g)△H=-92kJmol-1。
2NH3(g)△H=-92kJmol-1。
(2)N2(g)+3H2(g)![]() 2NH3(g)ΔH=-92kJmol-1,ΔH=反应物的键能总和-生成物的键能总和=E(N
2NH3(g)ΔH=-92kJmol-1,ΔH=反应物的键能总和-生成物的键能总和=E(N![]() N)+3E(H-H)-6E(N-H)=943kJ/mol+3
N)+3E(H-H)-6E(N-H)=943kJ/mol+3![]() 435kJ/mol-6E(N-H)=-92kJ/mol,E(N-H)=390kJ/mol,N-H的键能为390kJ/mol。
435kJ/mol-6E(N-H)=-92kJ/mol,E(N-H)=390kJ/mol,N-H的键能为390kJ/mol。
(3)催化剂能降低反应的活化能,不改变ΔH;合成氨反应通常用铁触媒作催化剂,使用铁触媒后的变化是:E1减小,ΔH不变。
(4)将题中两个热化学方程式编号:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H1=akJ·mol-1(①式)
N2(g)+O2(g)=2NO(g) △H2=bkJ·mol-1(②式)
应用盖斯定律,将①式-②式![]() 3得4NH3(g)+6NO(g)=5N2(g)+6H2O(g)ΔH=ΔH1-3ΔH2=(a-3b)kJ/mol,则1mol NH3还原NO至N2,该反应过程中的反应热△H3=(a-3b)/4kJ/mol 。
3得4NH3(g)+6NO(g)=5N2(g)+6H2O(g)ΔH=ΔH1-3ΔH2=(a-3b)kJ/mol,则1mol NH3还原NO至N2,该反应过程中的反应热△H3=(a-3b)/4kJ/mol 。


科目:高中化学 来源: 题型:
【题目】向50 mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如下图所示,且每一段只对应一个反应。下列说法正确的

A. 开始时产生的气体为H2
B. AB段产生的反应为置换反应
C. 所用混合溶液中c(HNO3)=0.5mol·L-1
D. 参加反应铁粉的总质量m2=5.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中常用到许多化学知识,下列说法不正确的是( )
A. 热的纯碱(Na2CO3)水溶液(显碱性)可清洗油污
B. 将含有甲醇的工业酒精兑制成饮用白酒
C. 不能用苏丹红(色素)作食品的着色剂
D. 蚕丝和羊毛都属于动物纤维,又称蛋白纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法中,正确的是( )
A. 所有的有机化合物都很容易燃烧
B. 易溶于汽油、酒精、苯等有机溶剂的物质一定是有机化合物
C. 凡是含碳元素的化合物都属于有机化合物
D. 有机化合物的同分异构现象是有机化合物种类繁多的重要原因之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关组成细胞的元素和化合物的叙述中,不正确的是( )
A. 碳链是细胞内生物大分子的基本骨架
B. 无机盐对维持细胞形态和酸碱平衡有重要作用
C. 有些蛋白质能够调节机体的生命活动如:生长激素和性激素等
D. 脂质存在于所有细胞中,是构成细胞和生物体的重要化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置进行实验,并回答下列问题(提示:装置A为B的化学电源)
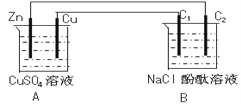
(1)锌极为__________极,电极反应式为__________________________________
(2)石墨棒C1为______极,电极反应式为__________________________________,石墨棒C2附近发生的实验现象为__________________________________
(3)当C2极析出224mL气体(标准状态)时,锌的质量减少_________g;
(4)此时装置B中OH-的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com