
【题目】联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为_____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的离子方程式为____________________。
(3)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4
上述反应热效应之间的关系式为△H4=_______________(用△H1、△H2、△H3表示)。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为
(已知:N2H4 + H+ ![]() N2H5+ K=8.5×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
N2H5+ K=8.5×107;Kw=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为 。
【答案】(1)![]() ; -2
; -2
(2)ClO- + 2NH3 = N2H4 + Cl- + H2O
(3)△H4 = 2△H3 - 2△H2 - △H1
(4)8.5×10-7;N2H6(HSO4)2
【解析】
试题分析:(1)肼的分子式为N2H4,是氮原子和氢原子形成四个共价键,氮原子和氮原子之间形成一个共价键形成的共价化合物,电子式为:![]() ,其中氢元素化合价为+1价,则氮元素化合价为-2价。
,其中氢元素化合价为+1价,则氮元素化合价为-2价。
(2)氨气被次氯酸钠溶液氧化生成肼,次氯酸钠被还原生成氯化钠,结合原子守恒配平书写反应的化学方程式为:2NH3+NaClO═N2H4+NaCl+H2O,离子方程式为:ClO-+2NH3 =N2H4+Cl-+H2O。
(3)已知①2O2(g)+N2(g)═N2O4(l)△H1,
②N2(g)+2H2(g)═N2H4(l)△H2,
③O2(g)+2H2(g)═2H2O(g)△H3。
依据热化学方程式和盖斯定律计算③×2-②×2-①得到
④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=2△H3-2△H2-△H1。
(4)联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离方程式为N2H4+H2ON2H5++OH-,平衡常数Kb=[c(N2H5+)c(OH)]/c(N2H4)= ![]() ×
×![]() =K × Kw = 8.7 × 107 × 1.0 × 10-14=8.7×10-7,第二步电离方程式为N2H5++H2ON2H62++OH-,因此联氨与硫酸形成的酸式盐为N2H6(HSO4)2。
=K × Kw = 8.7 × 107 × 1.0 × 10-14=8.7×10-7,第二步电离方程式为N2H5++H2ON2H62++OH-,因此联氨与硫酸形成的酸式盐为N2H6(HSO4)2。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,向密闭恒容容器中加入1.0 mol·L-1X,发生反应:2X(g) ![]() Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
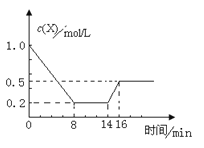
A.0~8min用Y表示该反应速率为0.1mol·L-1·min-1
B.8min时达到平衡,该反应的平衡常数为K= 0.5
C.14min时,改变的反应条是降低了温度
D.16min时的正反应速率比8min时的正反应速率大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种。
(1)用稀土等催化剂能将汽车尾气中的CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染。已知:
①N2(g)+ O2(g)=2NO(g)△H=180.5 kJ/mol
②2C(s)+ O2(g)=2CO(g)△H=—221kJ/mol
③C(s)+ O2(g)=CO2(g)△H=—393. 5 kJ/mol
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式__________________。
(2)①用甲烷催化还原氮的氧化物可消除氮氧化物的污染CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
②某温度下,密闭容器中CH4与NO的起始浓度分别为1mol/L、2mol/L,其中c(NO)随时间变化如图所示,t2时达到平衡,保持温度不变在t2时将容器容积压缩到一半,请画出t2-t3 c(CH4)随时间变化的曲线。_______

(3)①为提高反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g)中的转化率,可以采取在恒压条件下充入稀有气体,解释其原因______________。
N2(g)+CO2(g)+2H2O(g)中的转化率,可以采取在恒压条件下充入稀有气体,解释其原因______________。
②电解吸收法处理氮氧化物废气的基本原理是用硝酸吸收氮氧化物生成NO2-,同时用石墨电极电解将NO2-转化成NO3-,电解条件下循环利用NO3-来处理氮氧化物。写出该法处理NO2总反应的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,能生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和.
(1)A为__.(填元素符号)
(2)D的最高价氧化物的水化物的化学式是__,用电子式表示C与D构成的化合物的形成过程__
(3)写出由A、B组成的化合物与E反应的化学方程式:____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以N2和H2为反应物、溶有A的稀盐酸为电解质溶液,可制成能固氮的新型燃料电池,原理如下图所示。下列说法错误的是
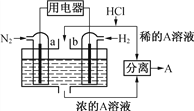
A. b电极为负极,发生氧化反应
B. a电极发生的反应为N2+8H++6e-=2NH4+
C. A溶液中所含溶质为NH4Cl
D. 当反应消耗1mol N2时,则消耗的H2为67.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物异搏定路线中某一步骤如下:

下列说法错误的是
A. 物质X中所有碳原子可能在同一平面内
B. 可用FeCl3溶液鉴别Z中是否含有X
C. 等物质的量的X、Z 分别与H2加成,最多消耗H2的物质的量之比为3:5
D. 等物质的量的X、Y分别与NaOH反应,最多消耗NaOH的物质的量之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质作用时,反应条件(反应温度和反应物用量)改变, 不会引起产物种类变化的是( )
A. Ca(OH)2和CO2 B. Fe和HCl
C. Na和O2 D. C和O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com