
����Ŀ��ijһ��Ӧ��ϵ�з�Ӧ��������ﹲ�������ʣ�O2��H2CrO4��Cr(OH)3��H2O��H2O2��
��֪�÷�Ӧ��H2O2ֻ�������¹��̣�H2O2��O2��
��1���÷�Ӧ�еĻ�ԭ����__________��
��2���÷�Ӧ�У�������ԭ��Ӧ�Ĺ�����_____________________��
��3��д���÷�Ӧ�Ļ�ѧ����ʽ�����õ����Ż�˫���ű������ת�Ƶķ������Ŀ________________________________________________________
��4������Ӧת����0.3mol���ӣ�������������ڱ�״�������Ϊ_______��
���𰸡� H2O2 H2CrO4�� Cr(OH)3  3.36L
3.36L
��������(1)����ϢH2O2-��O2�п�֪��OԪ�صĻ��ϼ���-1�����ߵ�0����H2O2Ϊ��ԭ�����ʴ�Ϊ��H2O2��
(2)��Ӧ��CrԪ�ػ��ϼ۽��ͣ�H2CrO4Ӧ����ԭ����Cr(OH)3���ʴ�Ϊ��H2CrO4��Cr(OH)3��
(3)�÷�Ӧ��OԪ��ʧ���ӣ�CrԪ�صõ����ӣ�2molH2CrO4��Ӧת�Ƶ���Ϊ2mol��(6-3)=6mol�����õ����ŷ��������ת�Ƶķ������ĿΪ =2Cr(OH)3��+3O2��+2H2O���ʴ�Ϊ��
=2Cr(OH)3��+3O2��+2H2O���ʴ�Ϊ�� =2Cr(OH)3��+3O2��+2H2O��
=2Cr(OH)3��+3O2��+2H2O��
(4)��2H2CrO4+3H2O2�T2Cr(OH)3��+3O2��+2H2O��֪������3mol����ת��6mol���ӣ���ת����0.3mol���ӣ����������������ʵ���Ϊ![]() mol=0.15mol�����ڱ�״�������Ϊ0.15mol��22.4L/mol=3.36L���ʴ�Ϊ��3.36L��
mol=0.15mol�����ڱ�״�������Ϊ0.15mol��22.4L/mol=3.36L���ʴ�Ϊ��3.36L��


 ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������鱦�е���Ҫ�ɷ֣�������Ȼ�߷������������ʵ���
A. ��ʯ B. ���� C. ˮ�� D. ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H��һ���������ϵ���Ҫ�ɷ�֮һ����ϳ�·�����£����ֲ���Ͳ��ַ�Ӧ������ȥ����

��֪��![]()
��ش��������⣺
��1��(CH3)2C=CH2��ͬ���칹���д���˳���칹���л��������Ϊ____________��
��2��A�ĺ˴Ź������׳������ϵ�H�⣬����ʾ____________��壬�������Ϊ____________��
��3��D�����к��еĺ���������������____________��E�Ľṹ��ʽΪ____________��
��4�� �����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ________________________________��
�����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ________________________________��
D��G��Ӧ����H�Ļ�ѧ����ʽΪ________________________________________��
��5��G��ͬ���칹���У�ͬʱ����������������____________��(�����������칹)��
�ٱ��Ķ�ȡ�������FeCl3��Һ������ʾ��Ӧ�ۺ���-COO-���ṹ
��6�����������ϳ�·�ߣ��Ա�ϩΪԭ�ϣ����Լ���ѡ��������Ʊ�2��3-�������ĺϳ�·��________________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA���������ӵ���������ֵ������˵����ȷ����
A. 1 molNa2O2���е����������ӵ���ĿΪ4NA
B. ���³�ѹ�£�0.1molC8H18�����еĹ��ۼ���ĿΪ2.5NA
C. ����0.2 mol H2SO4��Ũ����������ͭ��Ӧ��ת�Ƶĵ�����Ϊ0.2NA
D. 1 L 0.1mol/L������Һ�к��е���������Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�����������˵���д�����ǣ� ��
A. 1mol�������е�ԭ����Ϊ2NA
B. NA��ˮ�����к�����ԭ�ӵ����ʵ���Ϊ2 mol
C. 1 mol �����к��еķ�����Ϊ2NA
D. ����NA����ԭ�ӵ���������ʵ�����0.25 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E��F����Ԫ�أ�A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�B�ǵ縺������Ԫ�أ�C��2p�����������δ�ɶԵĵ����ӣ�Fԭ�Ӻ����������B��C���������֮�ͣ�D������Ԫ������Eͬ���ڣ�E��һ��������M�ܲ���Ӽ�������D��B���γ����ӻ������侧���ṹ��ͼ��ʾ����ش��������⣺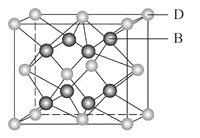
��1��EԪ��ԭ�ӻ�̬ʱ�ļ۵����Ų�ͼΪ___________��
��2��A2F������Fԭ�ӵ��ӻ�������_______��F��������FO3���ӿռ乹��Ϊ______��
��3��CA3��������ˮ����ԭ����Ҫ��________�����ж�CA3����ˮ���γ�CA3��H2O�ĺ����ṹ________(����ĸ����)����������γɽǶȻش����������ǣ�___________��
(a) (b)
(b)
��4��E�ľ�������ȡ________�ѻ���ʽ��
��5����ͼ�п��Կ�����D��B�γɵ����ӻ�����Ļ�ѧʽΪ_________���������˻����ᄃ����ܶ�Ϊag/cm3�����������_______cm3(д������ʽ���ɣ�NA��ʾ�����ӵ�������ֵ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǵؿ��й㷺�ֲ���Ԫ��֮һ���̶��������������dz���Ҫ���ǻ�ѧ�Լ���ҽҩ�����ӡ����ᡢ�ϳɹ�ҵ�ȵ���Ҫԭ�ϡ�
��1�������̵Ĺ�ҵ�Ʊ�����֪Al��ȼ����Ϊc kJ��mol��1����������Ȼ�ѧ����ʽΪ��
3MnO2(s)��Mn3O4(s)+O2(g) ��H1��a kJ��mol��1
3Mn3O4(s)+8Al(s)��9Mn(s)+4Al2O3(s) ��H2��b kJ��mol��1
��3MnO2(s)+4Al(s)��3Mn(s)+2Al2O3(s)��H��______kJ��mol��1���ú�a��b��c�Ĵ���ʽ��ʾ����
��2��MnCO3��һ�ֹ㷺����Ҫ������ԭ�ϡ�ͨ������MnCO3������ȡMnO2����Ӧ����ʽΪ��2MnCO3(s)��O2(g)![]() 2MnO2(s)��2CO2(g)����ͼΪװ��ʾ��ͼ��
2MnO2(s)��2CO2(g)����ͼΪװ��ʾ��ͼ��

�� 2MnCO3(s)��O2(g)![]() 2MnO2(s)��2CO2(g)�Ļ�ѧƽ�ⳣ������ʽK��_________��
2MnO2(s)��2CO2(g)�Ļ�ѧƽ�ⳣ������ʽK��_________��
�� �ڷ�Ӧ��������Ҫ����ճ����ò��ϳ�������Ŀ�ij���֤��Ӧ���������⣬����___________��
��3��MnO2��һ�ֳ��õĴ�����MnO2�������ȩ�ķ�Ӧ��������ͼ��ʾ��

ͼ��X��ʾ��������__________���÷�Ӧ���ܷ�Ӧ����ʽΪ___________��
��4��MnSO4����Ҫ��Ԫ�ط��ϡ��ö��Ե缫���MnSO4��Һ�����Ƶø��û��Ե�MnO2�����ʱ�ܷ�Ӧ�����ӷ���ʽΪ��_________��������������������pH__________��ѡ���������С�����䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����ȡClO2�Ļ�ѧ��Ӧ��2NaClO3 + SO2 + H2SO4 �� 2ClO2 + 2NaHSO4������˵����ȷ����
A. SO2�ڷ�Ӧ������ԭ�� B. NaClO3�ڷ�Ӧ�б�����
C. H2SO4 �ڷ�Ӧ���������� D. 1mol�������ڷ�Ӧ��ʧȥ1mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1molH��H��Br��Br��H��Br������ʱ��Ҫ���յ������ֱ���436kJ��200kJ��369kJ����������������������1mol�廯��ʱ�ų�������akJ����aΪ
A. -102 B. -51 C. 102 D. 51
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com