
����Ŀ����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷Ͼɵ�ص�ͭñ��Cu��Zn�ܺ���ԼΪ99%������Cu���Ʊ�ZnO�IJ���ʵ�������ͼ��
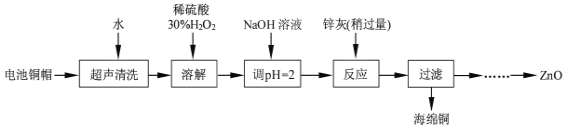
��1����д��ͭñ�ܽ�ʱͭ������ϡ���ᡢ30%H2O2��Ӧ�����ӷ�Ӧ����ʽ___��
��ͭñ�ܽ���ȫ���轫��Һ�й�����H2O2��ȥ����ȥH2O2�ļ�㷽����___��
��2��Ϊȷ������п��(��Ҫ�ɷ�ΪZn��ZnO������Ϊ������������)������ʵ������ⶨ��ȥH2O2����Һ��Cu2���ĺ�����
ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2������Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�������ҺpH=3��4�����������KI����Na2S2O3����Һ�ζ����յ㡣���������з�Ӧ�����ӷ���ʽ���£�2Cu2��+4I-=2CuI��(��ɫ)+I2��2S2O32-+I2=2I-+S4O62-
�ζ�ѡ�õ�ָʾ��Ϊ___���ﵽ�ζ��յ�۲쵽������Ϊ___��
��3�������£�����50mL0.0001mol/LCuSO4��Һ�м���50mL0.00022mol/LNaOH��Һ�������˳�������֪KSP[Cu(OH)2]=2.0��10-20(mol/L)3������������ɺ���Һ��c(Cu2+)=__mol/L��
��4����֪pH>11ʱZn(OH)2������NaOH��Һ����[Zn(OH)4]2-���±��г��˼������������������������pH(��ʼ������pH����������Ũ��Ϊ1.0mol��L-1����)��
��ʼ������pH | ������ȫ��pH | |
Fe3�� | 1.1 | 3.2 |
Fe2�� | 5.8 | 8.8 |
Zn2�� | 5.9 | 8.9 |
ʵ���п�ѡ�õ��Լ���30%H2O2��1.0mol��L-1HNO3��1.0mol��L-1NaOH���ɳ�ȥͭ����Һ�Ʊ�ZnO��ʵ�鲽������Ϊ��������Һ�м�������30%H2O2��ʹ���ַ�Ӧ��
��___���۹��ˣ���___���ݹ��ˡ�ϴ�ӡ������900�����ա�
���𰸡�Cu+H2O2+2H+=Cu2++2H2O �������� ������Һ ��ɫ��ȥ�Ұ���Ӳ��ָ�ԭ����Һ��ɫ 2��10-10 �μ�1.0mol��L-1NaOH������ҺpHԼΪ5(��3.2��pH<5.9)��ʹFe3��������ȫ ����Һ�еμ�1.0mol��L-1NaOH��������ҺpHԼΪ10(��8.9��pH��11)��ʹZn2��������ȫ
��������
��1������Ϊ˫��ˮ��������Һ���Ȱ�ͭ����������ͭ����Ȼ����һ�����ķ�Ӧ���γ�һ��ƽ�⣬�����γɵ�����ͭ���Ͼͻᱻϡ�����ܽ⣬ƽ�ⱻ���ƣ���Ӧ����������У��ʶ����ܽ⣬��Ӧ�Ļ�ѧ����ʽΪ��Cu+H2O2+H2SO4=CuSO4+2H2O��
�ڹ����������ʱȽ��ȶ������������¼������ҵķֽ�Ϊˮ������������Һ�й�����H2O2��ȥ�ɼ������У�
��2��������ҺΪָʾ���������һ��Na2S2O3��Һ����ʱ����Һ��ɫ��ȥ���������ɫ���䣬˵���ζ������յ㣻
��3�������£�����50mL0.0001mol/LCuSO4��Һ�м���50mL0.00022mol/LNaOH��Һ�������˳�������Ӧ���������ƹ�������Ӧ����Һ��������Ũ��Ϊ![]() =0.00001mol/L������Ksp[Cu(OH)2]=2.0��10-20(mol/L)3����֪�������ɺ���Һ��ͭ����Ũ��Ϊ
=0.00001mol/L������Ksp[Cu(OH)2]=2.0��10-20(mol/L)3����֪�������ɺ���Һ��ͭ����Ũ��Ϊ![]() = 2��10-10 mol/L;
= 2��10-10 mol/L;
��4������Һ�м���30%H2O2��ʹ���ַ�Ӧ��Ŀ��ʹFe2+ת����ȫΪFe3+���μ�NaOH��Һ��������ҺPHԼΪ5����3.2��pH��5.9����ʹFe3+������ȫ������Һ�еμ�1.0mol��L-1NaOH��������ҺPHԼΪ10����8.9��pH��11����ʹZn2+������ȫ��900�����գ��Ƶ�����п��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪����CH3OH(g)��H2O(g)===CO2(g)��3H2(g)����H����49.0 kJ/mol
��CH3OH(g)��![]() O2(g)===CO2(g)��2H2O(g)����H����192.9 kJ/mol
O2(g)===CO2(g)��2H2O(g)����H����192.9 kJ/mol
����������ʽ��֪��CH3OH��ȼ����________(����������������������С����)192.9 kJ/mol��
��֪ˮ��������Ϊ44 kJ/mol�����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ__________��
��2����CO2��NH3Ϊԭ�Ͽɺϳɻ�������[��ѧʽΪCO(NH2)2]��
��֪����2NH3(g)��CO2(g)===NH2CO2NH4(s)����H����159.5 kJ/mol
��NH2CO2NH4(s)===CO(NH2)2(s)��H2O(g)����H����116.5 kJ/mol
��H2O(l)===H2O(g)����H����44.0 kJ/mol
д��CO2��NH3�ϳ����غ�Һ̬ˮ���Ȼ�ѧ����ʽ��_____________________________��
��3����֪����Fe(s)��![]() O2(g)===FeO(s)����H1����272.0 kJ/mol
O2(g)===FeO(s)����H1����272.0 kJ/mol
��2Al(s)��![]() O2(g)===Al2O3(s)����H2����1675.7 kJ/mol
O2(g)===Al2O3(s)����H2����1675.7 kJ/mol
Al��FeO�������ȷ�Ӧ���Ȼ�ѧ����ʽ��_____________________________________���÷�Ӧ���Է������ƺܴ�ԭ����________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��V��W���ֶ�����Ԫ�أ�ԭ������������������Z��ԭ�Ӱ뾶���Z�ĵ�����W�ĵ�����ȼ�ղ�����ɫ���棻����Ԫ�ؿ������һ���л��Σ���ͼ��ʾ��������˵����ȷ���ǣ� ��
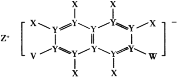
A.Y��W�γɵķ����и�ԭ������������8�����ȶ��ṹ
B.ԭ�Ӱ뾶�Ĵ�С��ϵΪ��V >Z > W
C.���ȶ��ԣ�X��V��ɵĶ�Ԫ������>X��W��ɵĶ�Ԫ������
D.Y��V��ɵĶ�Ԫ����������к�������Y��V��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)12.4 g Na2R��Na��0.4 mol����Na2R��Ħ������Ϊ________��R�����ԭ������Ϊ________����R������Ϊ1.6 g��Na2R�������ʵ���Ϊ________��
(2)86.4gA������4.80molCl2��ȫ��Ӧ������3.20molAClx,��x=___________��A��Ħ������Ϊ__________________g��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�ϵ��ȷ����( )
A. �е㣺���飾2��2-�������飾2��3-�������飾����
B. �ܶȣ�CCl4��CHCl3��H2O����
C. �����������������飾���飾��ϩ����Ȳ����
D. ������������ȼ�պ�O2�����������飾��ϩ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H3AsO3��һ�־綾��ɼ������SnCl2����ȥ����Ӧ����ʽΪ��2H3AsO3+3SnCl2+12X=2As��+3H2SnCl6+6H2O�����й��ڸ÷�Ӧ��˵������ȷ���ǣ� ��
A.��ԭ����H3AsO3
B.X�Ļ�ѧʽΪHCl���Ǹ÷�Ӧ��������
C.ÿ����0.2molAs����ԭ���õ�0.6mol����
D.�÷�Ӧת��2mol���ӣ����������SnCl2Ϊ1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���⡣
��.��������������������ţ�ǹܡ�����ƿ�����¶ȼơ��������ܡ�������װ�̶��õ�����̨���ƾ��ƺʹ������пף�������ƿ������ʯ�������������е�����̨��������þƾ���Һ����ȡ��ˮ�ƾ����Իش��������⣺
��1���������İ�װ�Ⱥ�˳�����������ṩ�ĸ�������������ţ�������__��__��__�������ڡ�
��2��������������ˮӦ���¿�__����������������������
��3������ʱ���¶ȼ�ˮ����Ӧ__��
��4����������ƿ��ע��Һ�������Ӧ�Ӽ�Ƭ���Ƭ����Ŀ����__��
��5����ʵ�ʵķ�������У�Ӧ�������м�����ʯ�ң���Ŀ����___������ϻ�ѧ����ʽ�ش𣩡�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����A��B��C�ֱ�Ϊ���塢����ɫ���塢��ɫ���壬�ں��ʵķ�Ӧ�����£����ǿɰ������ͼ���з�Ӧ����֪D��ҺΪ��ɫ��E��ҺΪ��ɫ����ش�
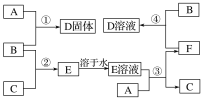
(1)A��__________��B��__________��C��_______________(��д��ѧʽ)��
(2)��Ӧ�ٵĻ�ѧ����ʽΪ_______________________________��
(3)��Ӧ�۵Ļ�ѧ����ʽΪ________________________________________��
(4)��Ӧ�ܵĻ�ѧ����ʽΪ____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С���������֪������Һ�����������ڵ������¿ɷ�Ӧ�����屽���廯�⣬�˷�ӦΪ���ȷ�Ӧ��������ͼװ����ȡ�屽�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A(��ʱA�¶˻����ر�)�С�
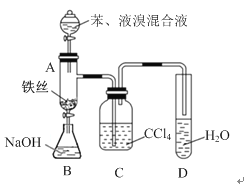
(1)д��A�з�Ӧ�Ļ�ѧ����ʽ__________________��
(2)ʵ�����ʱ����A�¶˵Ļ������÷�ӦҺ����B�У������Ŀ����_________��д���йص����ӷ���ʽ____________________�����ɵ��л�����λ����Һ______��(����������������)��
(3)C��ʢ��CCl4��������______________________��
(4)��֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ�������Թ�D�м���AgNO3��Һ��������________������֤������һ����֤�ķ��������Թ�D�μ�_____________����Һ���ɫ����֤����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com