
【题目】已知HA的酸性比HB弱,在物质的量浓度均为0.2 mol·L-1的NaA和NaB混合溶液中,下列排序正确的是( )
A. c(OH-)>c(A-)>c(B-)>c(H+) B. c(OH-)>c(B-)>c(A-)>c(H+)
C. c(OH-)>c(HA)>c(HB)>c(H+) D. c(OH-)>c(HB)>c(HA)>c(H+)
【答案】C
【解析】分析:根据盐的水解规律,弱酸的酸性越弱,其弱酸根离子水解程度越大,结合水解平衡和水的电离平衡分析解答。
详解:A、这两种盐水解的离子方程式为A-+H2O![]() HA+OH-、B-+H2O
HA+OH-、B-+H2O![]() HB+OH-。已知HA的酸性比HB的弱,所以A-水解程度大于B-,则水解生成的两种酸的浓度为c(HB)<c(HA);由于A-水解程度大于B-,则溶液中c(A-)<c(B-),但水解程度均是较弱的,则溶液中c(B-)>c(A-)>c(OH-)>c(H+),A错误;
HB+OH-。已知HA的酸性比HB的弱,所以A-水解程度大于B-,则水解生成的两种酸的浓度为c(HB)<c(HA);由于A-水解程度大于B-,则溶液中c(A-)<c(B-),但水解程度均是较弱的,则溶液中c(B-)>c(A-)>c(OH-)>c(H+),A错误;
B、根据A中分析可知B错误;
C、两种钠盐水解均呈碱性,则水解产生的OH—总浓度一定大于水解产生的HA、HB的浓度,即溶液中c(OH-)>c(HA)>c(HB)>c(H+),C正确;
D、根据C中分析可知D错误。答案选C。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】蒸馏是实验室制备蒸馏水的常用方法
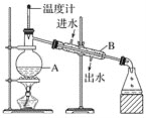
(1)如图是实验室制取蒸馏水的常用装置,图中明显的一个错误是____________________。
(2)仪器A的名称是______________,仪器B的名称是______________。
(3)实验时A中除加入少量自来水外,还需加入几粒____________,其作用是防止液体暴沸。
(4)从锥形瓶取少量收集到的液体于试管中,然后滴入____________和____________(填试剂的化学式),检验是否存在氯离子。
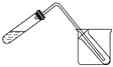
(5)如图装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与上图完全相同。该装置中使用的玻璃导管较长,其作用是______________;烧杯中最好盛有的物质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
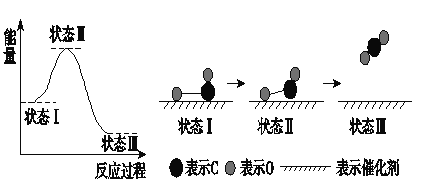
下列说法中正确的是( )
A. CO和O生成了具有共价键的CO2 B. 在该过程中,CO断键形成C和O
C. 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 D. CO和O生成CO2是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A+、B+、C-、D、E5种微粒(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①A++C-=D+E;②B++C-=2D。据此,回答下列问题:
(1)上述含10电子的四核阳离子为___________,含10电子的阴离子为_______。
(2)A+和B+的电子式A+____________、B+____________。
(3)C-、D、E3种粒子结合质子H+的能力由强到弱的顺序是(用粒子的化学式表示)____________________;这一顺序可用以下离子方程式加以说明:
①_____________________________________________;
②_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Na2CO3和NaHCO3的说法中,不正确的是
A. 均属于盐
B. 焰色反应均为黄色
C. 可以用加热的方法除去Na2CO3固体中的NaHCO3杂质
D. 物质的量相同的两种固体分别与足量盐酸反应,Na2CO3产生的二氧化碳多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行有关铜、硝酸、硫酸化学性质的实验,实验过程如图所示:
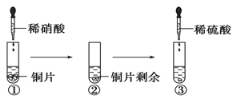
①、③均观察到实验现象:溶液呈蓝色,试管口有红棕色气体产生。下列说法正确的是
A. ①试管口有红棕色气体产生,原因是硝酸被还原为NO2
B. 由③的现象可得出结论:Cu可与稀硫酸反应
C. ③中反应的离子方程式:3Cu+2NO3-+8H+ === 3Cu2++2NO↑+4H2O
D. ③中可能产生SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲基丙烯酸甲酯是合成有机玻璃的单体,其合成方法之一如下:CH3OC≡CH+CH3OH+A ![]() CH2=C(CH3)COOCH3,下列说法正确的是
CH2=C(CH3)COOCH3,下列说法正确的是
A. 已知该反应的原子利用率为100%,则A为CO2
B. CH3OH和甘油互为同系物
C. CH3C≡CH与丙烯的性质相似,则该物质可以发生加成、氧化反应
D. 能与NaHCO3反应的CH2=C(CH3)COOCH3的同分异构体有9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1000mol/L的AgNO3溶液分别滴定体积均为V0mL的且浓度均为0.1000molL的KCl、KBr及KI溶液,其滴定曲线入下图,(已知25℃时,AgCl、AgBr及AgI溶度积常数依次为l.8×10-10、5.0×10-13、8.3×10-17),下列说法正确的是

A. V0= 45.00
B. 滴定曲线①表示KCl的滴定曲线
C. 滴定KCl时,可加入少量的KI作指示剂
D. 当AgNO3溶液滴定至60.00mL 时,溶液中 c(I-)-)-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关碱金属的叙述正确的是( )
A.随核电荷数的增加,密度逐渐增大
B.碱金属单质的金属性很强,均易与Cl2、O2、N2等发生反应
C.Cs2CO3加热时不能分解为CO2和Cs2O
D.无水硫酸铯的化学式为Cs2SO4,它不易溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com