
【题目】用VSEPR理论预测下列粒子的立体结构,其中正确的( )
A.NO3-为平面三角形B.SO2为直线形
C.BeCl2为V形D.BF3为三角锥形
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳足量,反应C(s)+H2O(g)![]() CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加碳的量且表面积保持不变 ②将容器的体积缩小一半 ③保持体积不变,充入He,使体系压强增大 ④保持压强不变,充入He使容器体积变大
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4 5H2O是铜的重要化合物,有着广泛的应用。
(一)CuSO4·5H2O制取
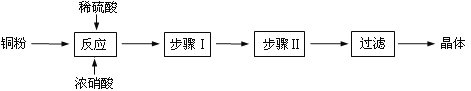
完成下列填空:
(1)向含铜粉的稀硫酸中滴加少量浓硝酸(可加热),铜粉溶解时可以观察到的实验现象:_____。
(2)根据反应原理,硝酸与硫酸的理论配比(物质的量之比)为______________________。
(3)步骤Ⅰ______________;步骤Ⅱ______________。
(二)胆矾中CuSO4·5H2O含量的测定
已知:CuSO4 + 2NaOH → Cu(OH)2 ↓+ Na2SO4
(1)实验方案如下,并将步骤④补全:
①将12.500g胆矾样品溶解,配成100mL溶液,取25mL于烧杯中;
②向溶液中加入100mL0.2500mol/L氢氧化钠溶液使Cu2+完全沉淀(不考虑其它副反应);
③过滤,多余的氢氧化钠溶液用0.5000mol/L盐酸滴定至终点,耗用10.00mL盐酸;
④___________________________
⑤数据处理。
(2)在滴定中,眼睛应注视__________;滴定终点时,准确读数应该是滴定管上________所对应的刻度。
(3)就方案中数据进行处理,则样品CuSO4·5H2O中质量分数为___________。步骤③中沉淀未洗涤,导致结果______(填偏大、偏小、无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 的相对原子质量为34.969,下列相关说法正确的是( )
的相对原子质量为34.969,下列相关说法正确的是( )
A.氯元素的近似相对原子质量为35
B.氯元素的某种同位素的质量数为35
C.氯元素的中子数为18
D.氯原子的质量为34.969
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸的结构如图所示。关于咖啡酸的描述不正确的是( )
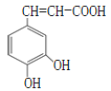
A.分子式为C9H8O4
B.1mol咖啡酸最多能与4mol氢气发生加成反应
C.遇溴水,既能发生取代反应又能发生加成反应
D.能还原酸性KMnO4溶液,说明其分子中含有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s,白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s,灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s,灰)![]() Sn(s,白) △H3=+2.1kJmol-1
Sn(s,白) △H3=+2.1kJmol-1
下列说法正确的是( )
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L恒容密闭容器中充入1mol PCl5,发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)反应过程中测定的部分数据见表(反应过程中条件不变);
PCl3(g)+Cl2(g)反应过程中测定的部分数据见表(反应过程中条件不变);
t/s | 0 | 60 | 150 | 250 | 350 | 450 |
n(PCl3)/mol | 0 | 0.12 | 0.19 | 0.2 | 0.2 | x |
请回答下列问题:
(1)x的值是___。
(2)0~60s内,用PCl3的浓度变化表示的化学反应速率是__。
(3)60s时,PCl5的转化率是__。
(4)达平衡时,容器中Cl2的体积分数是__(结果保留一位小数),由表中数据计算此条件下,该反应的平衡常数是__mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是( )
A.1L 1 mol·L-1的CH3COOH溶液中含有氢离子数约为6.02×1023
B.18g D2O(重水)完全电解,转移的电子数约为6.02×1023
C.34 g H2O2中含有的阴离子数为约为6.02×1023
D.STP下,14g乙烯和丙烯的混合物中,含有共用电子对数目约为3×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com