
【题目】某课外活动小组用如图装置进行实验,试回答下列问题:
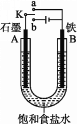
(1)若开始时开关K与a连接,则B极的电极反应为____________________。
(2)若开始时开关K与b连接,则B极的电极反应为____________________,总反应的离子方程式为____________________。
(3)有关上述实验,下列说法正确的是______。
A.溶液中Na+向A极移动
B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
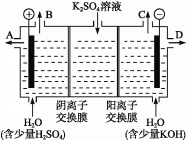
①该电解槽的阳极反应为______________。 此时通过阴离子交换膜的离子数_____(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)________导出。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因__________________________。
【答案】 Fe-2e- = Fe2+ 2H++2e- = H2↑ 2Cl-+2H2O![]() 2OH-+ H2↑+ Cl2↑ B 2H2O-4e- = 4H++ O2↑ 小于 D H2O
2OH-+ H2↑+ Cl2↑ B 2H2O-4e- = 4H++ O2↑ 小于 D H2O![]() H++ OH-,H+在阴极附近放电,引起水的电离平衡向右移动,使c(OH-)>c(H+)
H++ OH-,H+在阴极附近放电,引起水的电离平衡向右移动,使c(OH-)>c(H+)
【解析】试题分析:
(1) 开关K与a连接时,装置为原电池,铁为负极,发生吸氧腐蚀,即电极反应为Fe-2e-=Fe2+。
(2) 开关K与b连接时,装置为电解池,电解食盐水,此时阳极A发生2Cl--2e-=Cl2↑,阴极B发生2H++2e-H2↑,总反应的离子方程式为2Cl-+2H2O![]() 2OH-+ H2↑+ Cl2↑。
2OH-+ H2↑+ Cl2↑。
(3)阳离子向阴极移动,A错误;阳极A处产生的是Cl2,能使湿润的KI淀粉试纸变蓝,B正确;C应该通入HCl,不能加盐酸,因为盐酸是HCl的水溶液,错误;D电子不能在溶液中移动,错误。
(4))溶液中的OH-在阳极失电子产生O2:4OH--4e-=2H2O+O2↑,所以在B口放出O2,从A口导出H2SO4。溶液中的H+在阴极得到电子产生H2:2H++2e-=H2↑,则从C口放出H2,从D口导出KOH溶液。依据电荷守恒,通过阳离子交换膜的K+是通过阴离子交换膜的SO42-的2倍,所以通过阳离子交换膜的离子数大于通过阴离子交换膜的离子数。③电解过程中,H+在阴极附近放电,引起水的电离平衡向右移动,使c(OH-)>c(H+),故阴极区碱性明显增强。


科目:高中化学 来源: 题型:
【题目】深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根离子腐蚀,其电化学腐蚀原理如图所示。下列说法正确的是
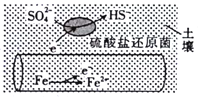
A. 铁管道发生的是吸氧腐蚀 B. 输送暖气的管道也易发生此类腐蚀
C. 这种情况下,土壤的pH增大 D. 管道上刷富铜油漆可以延缓管道的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A. 使酚酞变红色的溶液中:Na+、Cu2+、HCO3-、NO3-
B.  =1x10-13mol/L的溶液中:NH4+、Ca2+、Cl-、NO3-
=1x10-13mol/L的溶液中:NH4+、Ca2+、Cl-、NO3-
C. 与Al反应能放出H2的溶液中:Fe3+、K+、NO3- 、SO42-
D. 0.1mol/LNaAlO2溶液:H+、Na+、Cl-、SO42-、
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,我国北京等地出现严重雾霾天气,据研究,雾霾的形成与汽车排放的![]() 、
、![]() 等有毒气体有关,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体,反应方程式为
等有毒气体有关,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体,反应方程式为![]() 。对于该反应,温度不同(
。对于该反应,温度不同(![]() )其他条件相同时,下列图像正确的是
)其他条件相同时,下列图像正确的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中,不正确的是( )
A.氢氧化钡晶体与氯化铵晶体的反应属于放热反应
B.原电池工作时,通过外电路的电子和内电路的离子构成环路
C.元素的性质随着原子序数的递增而呈周期性变化的规律叫元素周期律
D.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,某溶液中由水电离产生的C(H+)和C(OH-)的乘积为1×10-20,该溶液中一定能大量存在的离子是
A. CO32- B. HCO3- C. Ba2+ D. NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】查阅资料:元素铬(Cr)在溶液中主要以Cr3+(蓝紫色) 、Cr(OH)4-(绿色) 、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)铬(24Cr)属于________(选填编号)。
a.主族元素 b.副族元素 c.Ⅶ族元素 d.过渡元素
(2)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol·L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
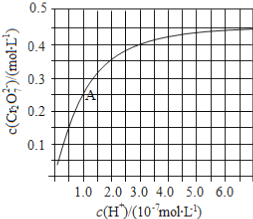
①用离子方程式表示Na2CrO4溶液中的转化反应____________。
②由图可知,溶液酸性增大,CrO42的平衡转化率__________(填“增大“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为__________。
③升高温度,溶液中CrO42的平衡转化率减小,则该反应的ΔH_________0(填“>”“<”或“=”)。
(3)欲降低废水中重金属元素铬的毒性,可将Cr2O72-转化为Cr(OH)3沉淀除去.已知:
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe2+ | 7.0 | 9.0 |
Fe3+ | 1.9 | 3.2 |
Cr3+ | 6.0 | 8.0 |
某含铬废水处理的主要流程如图所示:
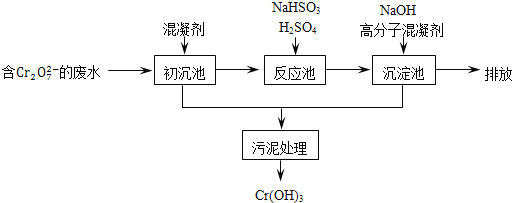
①初沉池中加入的混凝剂是K2SO4﹒Al2(SO4)3﹒24H2O,其作用为__________(用离子方程式表示).
②反应池中用NaHSO3将酸性废液中的Cr2O72-还原成Cr3+,该反应的离子方程式为________.根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子的先后顺序是____________.证明Cr3+沉淀完全的方法是__________.
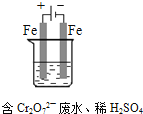
(4)工业可用电解法来处理含 Cr2O72-废水.实验室利用如图模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-═Fe2+,阴极反应式是2H++2e-═H2↑.Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是__________,得到的金属阳离子在阴极区可沉淀完全,用电解法处理该溶液中0.01mol Cr2O72-时,至少得到沉淀的质量是__________ g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com