
【题目】已知![]() 下,下列酸的电离常数如下:
下,下列酸的电离常数如下:
化学式 |
| HCN |
|
电离常数 |
|
|
|
下列各项不正确的是![]()
A.往NaCN溶液中通入少量![]() :
:![]()
B.往碳酸钠溶液中加足量醋酸:![]()
C.多元弱酸的酸性由第一步电离决定,因为第一步电离产生的氢离子对下一步电离起抑制作用
D.等物质的量浓度的![]() 和NaCN溶液,NaCN溶液的碱性更强
和NaCN溶液,NaCN溶液的碱性更强
【答案】A
【解析】
![]() 电离平衡常数越大,酸的酸性越强,则酸性:
电离平衡常数越大,酸的酸性越强,则酸性:![]() ,强酸能和弱酸盐反应生成弱酸,所以NaCN溶液中通入少量
,强酸能和弱酸盐反应生成弱酸,所以NaCN溶液中通入少量![]() :
:![]() ,故A错误;
,故A错误;
B.醋酸酸性大于碳酸,则碳酸钠和醋酸反应生成醋酸钠、二氧化碳和水,离子方程式为![]() ,故B正确;
,故B正确;
C.多元弱酸第一步电离程度远远大于第二步电离程度,因为第一步、第二步都电离生成氢离子而产生同离子效应,所以第一步电离产生的氢离子对下一步电离起抑制作用,故C正确;
D.相同物质的量浓度的钠盐,弱酸根离子水解程度越大其溶液碱性越强,酸的酸性越弱,其对应的酸根离子水解程度越大,则水解程度:![]() ,则等物质的量浓度的
,则等物质的量浓度的![]() 和NaCN溶液,NaCN溶液的碱性更强,故D正确;
和NaCN溶液,NaCN溶液的碱性更强,故D正确;
故选:A。


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】有机物Y(乙酰氧基胡椒酚乙酸酯)具有抗氧化、抗肿瘤作用,可由化合物X在一定条件下合成:
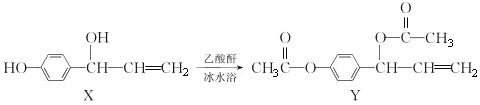
下列说法正确的是
A.可以用FeCl3溶液鉴别X与Y
B.X、Y分子中均含有1个手性碳原子
C.X分子中所有原子一定在同一平面上
D.1molX与溴水充分反应,最多消耗Br2的物质的量为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体 X 和气体 Y 各 0.16 mol 充入 10 L 恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A.该温度下,此反应的平衡常数 K=1.44
B.4min 时,ν(逆)>ν(正)
C.反应前 2min 的平均速率 ν(Z)=2.0×10-3mol/(L·min)
D.7min 时,反应还未达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气质量与我们的健康息息相关,目前我国通过监测 6 项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2 和 CO 是其中 3 项中的污染物。
(1)一定温度下,向固定体积为 2 L 的密闭容器中充入 SO2 和 NO2 各 1 mol,发生反应SO2(g)+NO2(g) ![]() SO3(g)+NO(g),测得上述反应 5 min 末到达平衡,此时容器中 NO 与 NO2的体积比为 3︰1,则这段时间内 SO2 的反应速率 v(SO2)=__________,此反应在该温度下的平衡常数 K=__________。
SO3(g)+NO(g),测得上述反应 5 min 末到达平衡,此时容器中 NO 与 NO2的体积比为 3︰1,则这段时间内 SO2 的反应速率 v(SO2)=__________,此反应在该温度下的平衡常数 K=__________。
(2)甲醇日趋成为重要的有机燃料,通常利用 CO 和 H2 合成甲醇,其反应的化学方程式为CO(g)+2H2(g) ![]() CH3OH(g)。今在一容积可变的密闭容器中,充有 10 mol CO 和 20 mol H2用于合成甲醇。CO 的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有 10 mol CO 和 20 mol H2用于合成甲醇。CO 的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:

①上述合成甲醇的反应为__________反应(填“放热”或“吸热”)。
②A、B、C 三点的平衡常数 KA、KB、KC 的大小关系为__________。A、B 两点对应的压强大小关系是 PA__________PB(填“大于”、 “小于”或“等于”)。
(3) 若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为____________,理论上通过外电路的电子最多为__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.某盐的水溶液呈酸性,该盐一定是强酸弱碱盐
B.中和相同体积相同pH的盐酸和醋酸溶液所需NaOH的物质的量相同
C.水的离子积常数![]() 随着温度的升高而增大,说明水的电离过程是吸热的
随着温度的升高而增大,说明水的电离过程是吸热的
D.弱电解质溶液稀释后,溶液中各种离子浓度一定都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在-定体积的某密闭容器中发生合成氨反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0。673K,30MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述不正确的是( )
2NH3(g) △H<0。673K,30MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述不正确的是( )
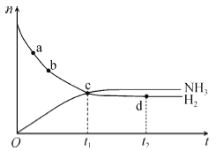
A.a点的正反应速率大于b点的
B.c点处,υ正(N2)=υ逆(N2)
C.d点处,υ正(N2):υ逆(H2)=1:3
D.升高温度,反应至t2时刻,n(H2)比图中d点的值大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.浓度相同的![]() 溶液和
溶液和![]() 溶液中
溶液中![]() 化学性质相同
化学性质相同
B.等质量的红磷和白磷完全燃烧生成![]() 放出热量相同
放出热量相同
C.可以通过化学反应将淀粉转化为乙酸
D.同温下,等体积pH相同的![]() 溶液和HCl溶液中由水电离出的
溶液和HCl溶液中由水电离出的![]() 数目相同
数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )
A.向100mL 0.1mol/L醋酸溶液中逐渐加入醋酸钠晶体过程中溶液pH的变化趋势图。CH3COOH![]() H++CH3COO-
H++CH3COO-

B.向FeCl3溶液和KSCN溶液混合后反应达平衡后, 向混合液中逐渐加入固体KCl过程中c(Fe3+)的变化趋势图。FeCl3+3KSCN![]() Fe(SCN)3+3KCl
Fe(SCN)3+3KCl

C.密闭容器中进行N2(g)+3H2(g) ![]() 2NH3(g)反应达到平衡后,保持恒温恒压条件下,逐渐通入稀有气体Ar的过程中H2的转化率变化趋势图。
2NH3(g)反应达到平衡后,保持恒温恒压条件下,逐渐通入稀有气体Ar的过程中H2的转化率变化趋势图。

D.密闭容器中进行CH3OCH3(g)+3H2O(g) ![]() 6H2(g)+2CO2(g) ΔH>0达到平衡后,保持恒压条件下,逐渐升高温度过程中CH3OCH3的转化率变化趋势图。
6H2(g)+2CO2(g) ΔH>0达到平衡后,保持恒压条件下,逐渐升高温度过程中CH3OCH3的转化率变化趋势图。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌元素对婴儿及青少年的智力和身体发育有重要的作用,被称为生命火花。利用恒电势电解NaBr溶液间接将葡萄糖[CH2OH(CHOH)4CHO]氧化为葡萄糖酸[CH2OH(CHOH)4COOH],进而制取葡萄糖酸锌,装置如图所示,下列说法错误的是( )
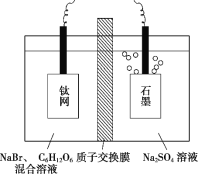
A.钛网与直流电源的正极相连,发生还原反应
B.石墨电极的反应为2H2O+2e-=H2↑+2OH-
C.电解过程中硫酸钠溶液浓度保持不变
D.生成葡萄糖酸的化学方程式为CH2OH(CHOH)4CHO+Br2+H2O=CH2OH(CHOH)4COOH+2HBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com