
【题目】绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:
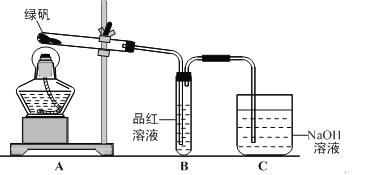
甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是___________,甲组由此得出绿矾的分解产物中含有SO2。装置C的作用是__________________。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中_____________。(填字母)
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解气态产物的装置:
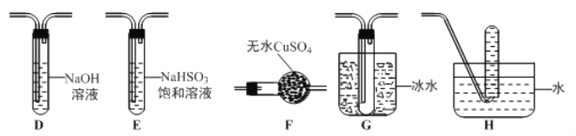
①丙组同学的实验装置中,依次连接的合理顺序为 _______________。
②能证明绿矾分解产物中有O2的实验操作及现象是_______________ 。
(4)为证明绿矾分解产物中含有三价铁,选用的实验仪器有试管、胶头滴管、_______________;选用的试剂为_______________。
【答案】品红溶液褪色吸收尾气,防止SO2(SO3)等气体扩散到空气中污染环境BCAFGBDH把H中的导管移出水面,撤走酒精灯,用姆指堵住试管口,取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气药匙盐酸,KSCN溶液
【解析】
本题考查实验方案设计的评价、离子的检验等知识。绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得各种铁的氧化物和硫的氧化物,硫的氧化物有二氧化硫、三氧化硫,铁的氧化物有氧化铁、氧化亚铁和四氧化三铁,根据题给信息结合氧化还原反应的理论分析。
(1)甲组得出绿矾的分解产物中含有二氧化硫,二氧化硫能使品红溶液褪色,所有装置B中观察到的现象是品红溶液褪色;二氧化硫有毒,因此装置C的作用是吸收尾气,防止SO2(SO3)等气体扩散到空气中污染环境。
(2)二氧化硫能使品红溶液褪色,受热恢复原来颜色,现在实验中不能恢复原来的颜色以及根据题意三氧化硫能漂白有机染料,因此可推出一定含有三氧化硫,可能含有二氧化硫,答案选BC。
(3)①首先加热绿矾,气态产物可能是三氧化硫、二氧化硫、水蒸气和氧气,因此先验证水蒸气,因此连接F装置,三氧化硫熔点较低,冰水中以固体形式存在,因此F装置后连接G,二氧化硫能使品红溶液褪色,因此G装置后连接B,需要吸收二氧化硫,B装置后连接D装置,最后连接H装置,因此顺序是AFGBDH。
②氧气能使带火星的木条复燃,因此具体操作是:把H中的导管移出水面,撤走酒精灯,用姆指堵住试管口,取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气 。
(4)验证Fe3+需要用KSCN溶液,需要把固体溶解成溶液,因此需要的试剂是盐酸和KSCN,取用固体需要药匙,则缺少的仪器是药匙。


科目:高中化学 来源: 题型:
【题目】人生病时要合理用药。下列药品与其作用相匹配的是
A. 氢氧化铝:中和过多胃酸 B. 阿司匹林:消炎抗菌
C. 氢氧化钡:胃部透视 D. 医用碘酒:人体补碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是进行化学研究的重要环节,下列有关化学实验的说法错误的是( )
A. 用酒精灯外焰加热铝箔,铝箔熔化但不滴落,说明Al2O3的熔点比Al的熔点高
B. 锅炉水垢CaSO4可用Na2CO3溶液浸泡,再用酸溶解去除,说明Ksp:CaCO3>CaSO4
C. 用酸性KMnO4溶液验证草酸的还原性
D. 向滴有KSCN的FeCl3溶液中加入NaOH溶液以研究反应物浓度对化学平衡的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】唐代中药学著作《新修本草》中,有关于“青矾”的记录为:“本来绿色,新出窟未见风者,正如琉璃,…,烧之赤色”.据此推测,“青矾”的主要成分为( )
A.CuSO45H2O
B.FeSO47H2O
C.KAl(SO4)212H2O
D.Fe2(SO4)39H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与乙酸乙酯(CH3COOCH2CH3)互为同分异构体的是
A. CH3CH2CH2CH2OHB. CH3COCH2CH3
C. CH3CH2CH2COOHD. CH3CH2OCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________与盐酸反应最剧烈,________与盐酸反应的速度最慢;________与盐酸反应产生的气体最多。
向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______________。
(3)资料显示:钠、镁、铝都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是________________。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应产生氢气的化学方程式为____________________。
Ⅱ.为验证氯、溴、碘三种元素的非金属性强弱,用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。

实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液由黄色变为棕红色时,关闭活塞a。
④……
(1)A中发生反应生成氯气,请写出该反应的离子方程式:___________________。
(2)验证氯气的氧化性强于碘的实验现象是________________________。
(3)B、C管口“浸有NaOH溶液的棉花”的作用是__________________________。
(4)为验证溴的氧化性强于碘,过程④的操作和现象是______________________。
(5)过程③实验的目的是____________________。
(6)请运用原子结构理论解释氯、溴、碘非金属性逐渐减弱的原因:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.硅太阳能电池、计算机芯片、光导纤维都用到硅单质
B.水晶镜片、石英钟表、玛瑙手镯含有SiO2
C.水泥路桥、门窗玻璃、砖瓦、陶瓷餐具所用材料为硅酸盐
D.熔融烧碱时不能使用普通玻璃坩埚、石英坩埚和陶瓷坩埚
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com