
【题目】(1)下列反应中,属于放热反应的是 ______ ,属于吸热反应的是 ______ (填序号)
①煅烧石灰石制生石灰 ②燃烧木炭取暖 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰 ⑥Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 ⑦灼热的木炭与CO2反应
写出Ba(OH)2·8H2O晶体与NH4Cl晶体反应的化学反应方程式: _________.
(2)已知下列各种共价键的键能:C—H:a kJ· mol-1、O—H:b kJ· mol-1、O=O:c kJ·mol-1、C=O:d kJ·mol-1。写出甲烷气体完全燃烧生成CO2气体和气体水的热化学方程式:________
(3)1L 1mol/L H 2SO 4溶液与 2L 1mol/L NaOH溶液完全反应,放出 114.6kJ的热量,该反应的中和热为 _______,表示其中和热的热化学方程式为____________。
【答案】②③④⑤ ①⑥⑦ Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=(4a+2c-2d—4b)] kJ· mol-1 57.3kJ/mol NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol
【解析】
(1)化学上把有热量放出的反应叫做放热反应,大多数化合反应、金属单质与水(或酸)的置换反应、燃烧反应、中和反应、铝热反应等都是放热反应;把吸收热量的反应叫做吸热反应,大多数分解反应、C与CO2的化合反应、氢氧化钡晶体与氯化铵晶体反应等是吸热反应;
(2)化学反应中旧键断裂需要吸收能量,新键形成需要放出能量,化学反应中的反应热△H=反应物总键能-生成物总键能;
(3)1L 1mol/L H2SO4溶液与2L 1mol/L NaOH溶液完全反应,放出114.6kJ的热量,则生成1mol水放出57.3kJ的热量。
(1)①煅烧石灰石制生石灰是分解反应,属于吸热反应;
②木炭燃烧是放热反应;
③炸药爆炸是放热反应;
④酸与碱的中和反应是放热反应;
⑤生石灰与水作用制熟石灰是化合反应,属于放热反应;
⑥Ba(OH)2·8H2O晶体与NH4Cl晶体的反应是吸热反应;
⑦灼热的木炭与CO2反应是吸热反应;
属于放热反应的是②③④⑤,属于吸热反应的是①⑥⑦,故答案为:②③④⑤;①⑥⑦;
Ba(OH)2·8H2O晶体与NH4Cl晶体研磨反应生成氯化钡、氨气和水,反应的化学方程式为Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,故答案为:Ba(OH)2·8H2O+2NH4Cl=BaCl2
+2NH3↑+10H2O;
(2)化学反应中旧键断裂需要吸收能量,新键形成需要放出能量,化学反应中的反应热△H=反应物总键能-生成物总键能。甲烷气体完全燃烧生成CO2气体和气体水的化学方程式为CH4(g)+2O2(g)═CO2(g)+2H2O(g)反应热△H=[4E(C-H)+2E(O=O)]-[2E(C=O)+4E(H-O)]
=[(4a+2c)-(2d+4b)] kJ· mol-1,故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=(4a+2c-2d—4b)] kJ· mol-1;
(3)1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,即生成2mol水放出114.6kJ的热量,反应的反应热△H为-114.6kJ/mol,所以中和热为生成1mol水所放出的热量57.3kJ/ mol,则中和热的热化学方程式:NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol,故答案为:57.3kJ/mol;NaOH(aq)+
Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol,故答案为:57.3kJ/mol;NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol。
Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol。


科目:高中化学 来源: 题型:
【题目】半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是硅,下列有关硅及其化合物叙述正确的是( )
A. 水玻璃可做防火材料 B. 光导纤维的主要成分是高纯硅
C. 可用石英钳埚加热熔融氢氧化钠固体 D. 二氧化硅不和任何酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是

A. 气态氢化物的稳定性:R>W
B. X与Y可以形成原子个数比为1:1和1:2的两种离子化合物
C. 由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2-
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN-
B. ![]() =106的溶液中:NH4+、K+、AlO2-、NO3-
=106的溶液中:NH4+、K+、AlO2-、NO3-
C. 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl-
D. 1.0mol·L-1的KNO3溶液中:Fe2+、H+、Cl-、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备,其原理如图所示:
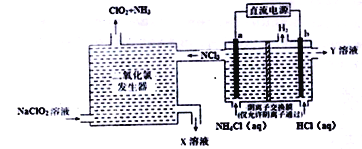
下列说法不正确的是
A. b电极接电源的负极,在b极区流出的Y溶液是稀盐酸
B. 二氧化氯发生器中排出的X溶液中溶质主要为NaCl和NaOH
C. 电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则b极产生0.6gH2
D. 电解池a极的电极反应式为NH4+-6e-+4OH-+3Cl-=NCl3+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知a、b、c、d四种短周期主族元素,在周期表中相对位置如下图所示,下列说法正确的是( )

A. a、c两元素的最高正价一定相等
B. d的原子序数不可能是b的原子序数的3倍
C. 若c元素最高价氧化物对应的水化物是强酸,则d元素的单质具有强氧化性
D. c的最高价氧化物对应的水化物可溶于d的最高价氧化物对应的水化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com