
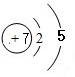
 ,
, ;
;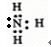 ,故答案为:
,故答案为: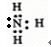 ;
;| 1 |
| 2 |
| 1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、常温常压下,8gO2含有4NA个电子 |
| B、1L 1mol/L 的NaClO 溶液中含有ClO-的数目为NA |
| C、标准状况下,22.4L盐酸含有NA个HCl分子 |
| D、1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
- 2 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| △ |
| △ |
| △ |
| △ |
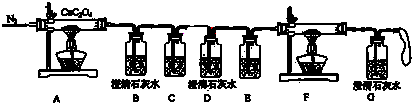
| 操作 | 预期实验现象和结论 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
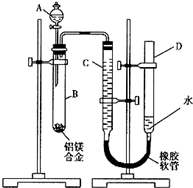 含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:| 足量的NaOH溶液 |
| 足量盐酸 |
| () |
| () |
查看答案和解析>>
科目:高中化学 来源: 题型:
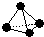 ,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.试判断相同条件下B4与B2的稳定性顺序是:
,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.试判断相同条件下B4与B2的稳定性顺序是:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用分液漏斗分离醋酸和水的混合物 |
| B、用酒精萃取碘水中的碘 |
| C、用10mL量筒量取7.5mL稀盐酸 |
| D、用容量瓶配置溶液过程中定容时发现蒸馏水稍微过量,可用胶头滴管吸出少许 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com