
【题目】

请回答下列问题:
(1)A是一种能与溴水反应使其褪色的芳香烃,其结构简式为 。
(2)在上述合成路线发生的反应中属于取代反应的是 (填反应编号)。
(3)反应①发生时若不加入H2O2,会生成较多的一种副产物。写出这种副产物的结构简式 。
(4)写出由C→D 、 E→F转化的化学反应方程式 、 。
(5)在化合物E多种同分异构体中,只含有一种含氧官能团,且能与FeCl3溶液发生显色反应的同分异构体有 种(不考虑羟基与碳碳双键直接连在一起的同分异构体),任写一种满足上述条件且核磁共振氢谱中有5个峰信号的同分异构体的结构简式 。
(6)按上述合成路线的表达形式,写出由![]() 制备
制备![]() 的合成路线。
的合成路线。
【答案】(1)![]() (1分)
(1分)
(2)②⑤(2分)(3)![]() (1分)
(1分)
(4)![]() (3分)
(3分)
![]() (3分)
(3分)
(5)6(2分)![]() 或
或![]() (任写一种,1分)
(任写一种,1分)
(6)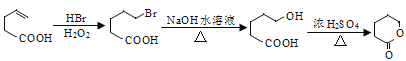 (2分)
(2分)
【解析】试题分析:(1)A是一种能与溴水反应使其褪色的芳香烃,说明含有碳碳双键,则其结构简式为![]() 。
。
(2)在上述合成路线中反应①是碳碳双键的加成反应,②是卤代烃的水解反应,③是羟基的催化氧化,④是醛基的氧化反应,⑤是酯化反应,因此发生的反应中属于取代反应的是②⑤。
(3)反应①发生时若不加入H2O2,会生成较多的一种副产物,该副产物的结构简式为![]() 。
。
(4)C→D是羟基的催化氧化,方程式为![]() ;E→F是酯化反应,转化的化学反应方程式为
;E→F是酯化反应,转化的化学反应方程式为
![]() 。
。
(5)在化合物E多种同分异构体中,只含有一种含氧官能团,且能与FeCl3溶液发生显色反应,说明含有酚羟基,即苯环上含有2个酚羟基和1个碳碳双键,因此符合条件的同分异构体有6种(不考虑羟基与碳碳双键直接连在一起的同分异构体),满足上述条件且核磁共振氢谱中有5个峰信号的同分异构体的结构简式为![]() 或
或![]() 。
。
(6)由![]() 制备
制备![]() 可以采用逆推法,即首先形成羟基,然后酯化,卤代烃水解形成羟基,碳碳双键据此引入卤素原子,则合成路线为
可以采用逆推法,即首先形成羟基,然后酯化,卤代烃水解形成羟基,碳碳双键据此引入卤素原子,则合成路线为
 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在体积都为1 L,pH 都等于2 的盐酸和醋酸溶液中,投入0.65 g 锌粒,则下图所示比较符合客观事实的是
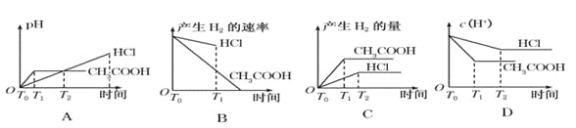
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表得第_____________族,其基态原子中未成对电子的个数为______。
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为____________________,所含非金属元素的电负性由大到小的顺序是____________________。
(3)尿素分子中、碳原子为________杂化,分子中σ键与π键的数目之比为____________________。
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需要知道的数据是______。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为____________________。
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示,则该物质的化学式为____________________。若晶体密度为dg·cm3,则晶胞中最近的两个碳原子的距离为____________________pm(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
请判断 X、Y、Z,并用相应的元素符号回答下列问题。
(1)X是_____,它的原子M层电子数是_______。
(2)表中元素原子半径最大的是________。
(3)Y在元素周期表中的位置是第____周期第_____族,用电子式表示Y的最简单氢化物的形成过程_____。
(4)氮气中氮原子之间的化学键属于_____键,由氮气与氢气反应生成1mol氨气时转移电子的数目是______NA。
(5)硫与Z两种元素相比,非金属性强的是______,请用化学方程式说明这一结论____________。
(6)碳、氮、Y三种元素的最简单气态氢化物的稳定性由强到弱的顺序是________。由最高价碳元素与最低价氮元素组成化合物的化学式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g H2完全燃烧生成水蒸气放出热量121 kJ,且O2中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中形成1 mol H—O键时放出热量463 kJ,则H2中1 mol H—H键断裂时吸收的热量为( )
A.920 kJ B.436 kJ C.557 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知五种元素原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1) 写出C元素的名称是___________________
(2) 用电子式表示离子化合物A2B的形成过程_____________________________;
(3)写出下列物质的电子式:E与B形成的化合物_______________;A、B、E形成的化合物
____________;D、E形成的化合物_____________。
(4) A、B两元素组成的化合物A2B2属于___________(离子或共价)化合物,存在的化学键 ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017届江西师大附中高三12月月考】一定条件下,在水溶液中1molCl-,ClOx(x=1,2,3,4)的能量(kJ)相对大小如图所示.下列有关说法正确的是( )
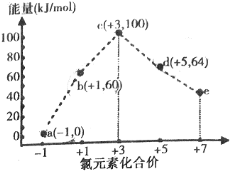
A.e是ClO3-
B.b→a+c反应的活化能为60kJmol-1
C.a,b,c,d,e中c最稳定
D.b→a+d反应的热化学方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-116kJmol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com