
����Ŀ����������һ����Ҫ�Ļ����м��壬������ҵ�о����ȵ㡣һ����ʯ�ͻ����еķ�����������Ҫ�ɷ�ΪNiCO3��SiO2������������Fe2O3��Cr2O3��Ϊԭ���Ʊ��������Ĺ�ҵ�������£�

��֪����. NiS��Ni(OH)2��Cr(OH)3��������ˮ��Cr(OH)3�������������
��. Fe(OH)3������NH4Cl����ˮ�Ļ��Һ��Ni(OH)2����NH4Cl����ˮ�Ļ��Һ����[Ni(NH3)6]2+��
��ش��������⣺
��1����������ʱӦ�Ƚ������������飬����20%������100���·�Ӧ2h���ò�����Ŀ��Ϊ____��
��2��������I����Ҫ�ɷ��ڹ�ҵ�ϵ���;Ϊ_______��ֻд1�ּ��ɣ���NH4Cl�ĵ���ʽΪ_______��
��3����һ�μ�����ʱ�������NaOH��Һ�������������������Ӧ�����ӷ���ʽΪ________��
��4������������Ŀ��Ϊ_____________________��
��5����������ʱ������Ӧ�����ӷ���ʽΪ___________________________��
��6�������μ����ʱ����ʹ��Һ�е�Ni2+������ȫ������ά��c(OH-)������__________��(��֪Ni(OH)2��Ksp=2��10-15��![]() ��1.4����
��1.4����
��7����ϵ�в�����������ָ____________�����ˡ�ϴ�ӡ����������NiSO4��7H2O���岻����Ӧ�������е��ᴿ��������Ϊ____________��
���𰸡��ӿ췴Ӧ���ʣ������Ԫ�صĽ����� �Ʋ��������ƹ��ά�� ![]() Cr3++4OH-=CrO2-+2H2O ʵ����Ԫ�غ���Ԫ�صķ��� 3NiS+8H++2NO3-=3Ni2++2NO��+3S��+4H2O 1.4��10-5mol��L-1 ����Ũ������ȴ�ᾧ �ؽᾧ
Cr3++4OH-=CrO2-+2H2O ʵ����Ԫ�غ���Ԫ�صķ��� 3NiS+8H++2NO3-=3Ni2++2NO��+3S��+4H2O 1.4��10-5mol��L-1 ����Ũ������ȴ�ᾧ �ؽᾧ
��������
������������Ҫ�ɷ�ΪNiCO3��SiO2������������Fe2O3��Cr2O3�������ܵõ������������������������Һ���������費������Ϊ����I����Ҫ�ɷ֣�����Һ�м���NaOH��Һ���õ�����������������������������ƫ��������Һ��ƫ������Ϊ��ҺI����Ҫ�ɷ֣�����������������NH4Cl����ˮ�Ļ��Һ�õ�[Ni(NH3)6]2+��Һ�������������ܣ������������Ҫ�ɷ֣�����Һ��ͨ�����⣬����NiS������������е���ϡ����õ������������������м���NaOH��Һ�õ���������������������м�������õ����������پ���ϵ�в����õ�NiSO4��7H2O��
��1����������ʱӦ�Ƚ������������飬����20%������100���·�Ӧ2h��������Ϊ������Ӵ���ӣ��ӿ췴Ӧ���ʣ���߸�Ԫ�صĽ����ʣ�
��2������I����Ҫ�ɷ�Ϊ�������裬��ҪӦ�����Ʋ������ƹ��ά�ȣ�NH4Cl�ĵ���ʽΪ![]() ��
��
��3��������Ŀ��֪��Cr(OH)3���������������������������������������������NaOH����������������������NaOHʹ�����������ƫ�����ƣ������ӷ���ʽΪCr3++4OH-=CrO2-+2H2O��
��4��������������Ԫ������һ�μ�����ʱת��Ϊ�����������������������������Ȼ��-��ˮ�����Һ���������������ڸ���Һ�����Ŀ����ʵ��NiԪ�غ�FeԪ�صķ��룻
��5������ʱ����ϡ������NiS�ķ�Ӧ��ϡ��������������NiS����ԭ����3NiS+8H++2NO3-=3Ni2++2NO��+3S��+4H2O��
��6�����������У�![]() ����������ȫ����ʱ��2��10-15=10-5��
����������ȫ����ʱ��2��10-15=10-5��![]() ����
����![]() ��
��
��7����ϵ�в�����������ָ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����������NiSO4��7H2O���岻����Ӧ�������е��ᴿ��������Ϊ�ؽᾧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ���о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬����������ʵ�飺
��ʵ��ԭ����2KMnO4 + 5H2C2O4 + 3H2SO4 �� K2SO4 + 2MnSO4 + 10CO2�� + 8H2O
��ʵ�����ݼ���¼��
ʵ���� | �����£��Թ��������Լ��������� / mL | ��������Һ��ɫ������ɫ����ʱ�� / min | |||
0.6 mol/L H2C2O4��Һ | H2O | 3 mol/L ϡ���� | 0.05mol/L KMnO4��Һ | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
��ش�
��1�������ϱ��е�ʵ�����ݣ����Եõ��Ľ�����___________________________________��
��2������ʵ��1�����ݼ��㣬����KMnO4��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ����(KMnO4)�� ________��
��3����С��ͬѧ���ݾ��������n(Mn2+) ��ʱ��仯���Ƶ�ʾ��ͼ����ͼ1��ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n(Mn2+) ��ʱ��仯������Ӧ��ͼ2��ʾ����С��ͬѧ����ͼ2��ʾ��Ϣ������µļ��裬����������ʵ��̽����
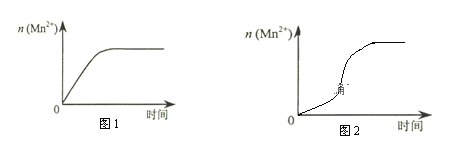
�ٸ�С��ͬѧ����ļ�����___________________________________________________��
�����������С��ͬѧ���ʵ�鷽��������д���пհס�
ʵ���� | �����£��Թ��������Լ��������� / mL | �����Թ��м����������� | ��������Һ��ɫ������ɫ����ʱ�� / min | |||
0.6mol/L H2C2O4��Һ | H2O | 3mol/Lϡ���� | 0.05mol/L KMnO4��Һ | |||
4 | 3.0 | 2.0 | 2.0 | 3.0 | _______ | t |
������С��ͬѧ����ļ��������Ӧ�۲쵽��������_____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ʱ�������й��������Ӧ��������ȷ����
ʱ�������й��������Ӧ��������ȷ����
A. ��ͼ�ɱ�ʾ�����Ϊ
��ͼ�ɱ�ʾ�����Ϊ![]() L��pH��Ϊ11�İ�ˮ��NaOH��Һ�ֱ���ˮϡ����VL�������b����Ϊ��ˮ
L��pH��Ϊ11�İ�ˮ��NaOH��Һ�ֱ���ˮϡ����VL�������b����Ϊ��ˮ
B. ��ͼ�ɱ�ʾˮ��Һ��
��ͼ�ɱ�ʾˮ��Һ��![]() ��
��![]() ��Ũ�ȱ仯���ߣ������{�¶ȿ�ʵ��
��Ũ�ȱ仯���ߣ������{�¶ȿ�ʵ��![]()
C. ��ͼ�ɱ�ʾ�����Ϊ100mL��pH��Ϊ3����������ᣬ�ֱ���
��ͼ�ɱ�ʾ�����Ϊ100mL��pH��Ϊ3����������ᣬ�ֱ���![]() gZn��Ӧ����a��ʾ����
gZn��Ӧ����a��ʾ����
D. ��ͼ�ɱ�ʾ���Ϊ
��ͼ�ɱ�ʾ���Ϊ![]() 1
1![]() ������ˮϡ����VL�������
������ˮϡ����VL�������![]() ��Χ�ڣ�
��Χ�ڣ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ�ĸ�����
�ٺ����Ļ�����һ����������
���ε������һ�����н���Ԫ��
��![]() һԪ����Һ��
һԪ����Һ��![]() Ũ��һ��Ϊ
Ũ��һ��Ϊ![]()
��ǿ����Һ�е�![]() Ũ��һ������������Һ�е�
Ũ��һ������������Һ�е�![]() Ũ��
Ũ��
�ݵ������Һ�����ԭ������Һ���������ƶ�����������
��![]() ˮ��Һ����ʱ���ɵ��������������ӣ���������
ˮ��Һ����ʱ���ɵ��������������ӣ���������
A.1��B.2��C.3��D.4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��Ԫ�����ڱ���һ���֣�
�� | X |
Y | Z |
��1
���ݱ�� | ����NaOH��Һ�����/mL | ��Һ��pH | |
HX | HZ | ||
�� | 0 | 3 | 1 |
�� | 20.00 | a | 7 |
��2
25��ʱ����Ũ��Ϊ0.1000mol/L������������Һ�ֱ�ζ�20.00 mLŨ�Ⱦ�Ϊ0.1000mol/ L��������HX��HZ��������Һ����仯����ʵ���������2�������ж���ȷ����
A. ������a<7
B. 25��ʱ��HX�ĵ��볣��Ka=1��10-6
C. Y��Z��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�߷ֽ��¶ȸ�
D. 0.1000mol/L Na2Y��ˮ��Һ����c(Y2-)+c(HY-)��c(H2Y)=0.1000mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�![]() ��
��![]() ��CO�ȴ�����Ⱦ�������������������Ҫ���壬Ŀǰ��������Ⱦ�ж��ַ�����
��CO�ȴ�����Ⱦ�������������������Ҫ���壬Ŀǰ��������Ⱦ�ж��ַ�����
(1)�û���̿��ԭ��������������йط�ӦΪ��![]() ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO������
ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO������![]() �����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
�����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
| NO |
|
|
0 |
| 0 | 0 |
10 |
|
|
|
20 |
|
|
|
30 |
|
|
|
40 |
|
|
|
50 |
|
|
|
��![]() ʱ���÷�Ӧ��ƽ�ⳣ��
ʱ���÷�Ӧ��ƽ�ⳣ��![]() ______
______ ![]() ������λС��
������λС��![]() ��
��
��![]() �ı�ijһ��������Ӧ���´ﵽƽ�⣬��ı������������ ______ ��
�ı�ijһ��������Ӧ���´ﵽƽ�⣬��ı������������ ______ ��
����30min�������¶���![]() ���ﵽƽ��ʱ��������NO��
���ﵽƽ��ʱ��������NO��![]() ��
��![]() ��Ũ��֮��Ϊ5��3��3����÷�Ӧ��
��Ũ��֮��Ϊ5��3��3����÷�Ӧ��![]() ______
______ ![]() ����
����![]() ������
������![]() ������
������![]() ��
��![]()
(2)��![]() ����ԭ��������������������������Ⱦ����֪��
����ԭ��������������������������Ⱦ����֪��
��![]()
��![]()
��![]()
�![]() ��
��![]() ��Ӧ����
��Ӧ����![]() ��
��![]() ��
��![]() ���Ȼ�ѧ����ʽ ______
���Ȼ�ѧ����ʽ ______
(3)���Ͱ���������������ѧԭ���Dz��ð�ˮ���������е�![]() ������һ�����������������ղ��ﷴӦ���ü����ŵ�����ܻ�������
������һ�����������������ղ��ﷴӦ���ü����ŵ�����ܻ�������![]() �⣬���ܵõ�һ�ָ��Ϸ��ϣ�
�⣬���ܵõ�һ�ָ��Ϸ��ϣ�
�ٸø��Ϸ��Ͽ��ܵĻ�ѧʽΪ ______ ![]() д��һ�ּ���
д��һ�ּ���![]() ��
��
������ˮ��![]() ǡ����ȫ��Ӧ�������Σ����ʱ��Һ�� ______ ��
ǡ����ȫ��Ӧ�������Σ����ʱ��Һ�� ______ ��![]() ����������������
����������������![]() ��
��![]() ��֪�����£���ˮ
��֪�����£���ˮ![]() ��
��![]()
![]() ��
��![]() ��
��![]()
(4)��ȼú�����Ķ�����̼�������ã��ɴﵽ��̼�ŷŵ�Ŀ�ģ���ͼ��ͨ���˹�������ã���![]() ��
��![]() Ϊԭ���Ʊ�HCOOH��
Ϊԭ���Ʊ�HCOOH��![]() ��ԭ��ʾ��ͼ������b���淢���ĵ缫��ӦʽΪ ______
��ԭ��ʾ��ͼ������b���淢���ĵ缫��ӦʽΪ ______ ![]() �����£�
�����£�![]() ��HCOONa��ҺpHΪ10����HCOOH�ĵ��볣��
��HCOONa��ҺpHΪ10����HCOOH�ĵ��볣��![]() ______ ��
______ ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������;�����UPOEM�����г�ɫ�����ȶ��ԡ���е�Ժ���ʴ�ԣ��㷺Ӧ���ڰ�װ��ҽ�÷���ߺ�ҩ���װ���������Ʊ��ĺ��ķ�Ӧ���£�

����˵����ȷ����
A.�÷�ӦΪ�Ӿ۷�Ӧ
B.�����в�����˳���칹
C.1mol III������3mol H2��Ӧ
D.����������Ӧ����������֪��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊȷ��ij���ȼ�(������������)����ɣ��ֱ��������ʵ�顣
(1) ��ȡa g��Ʒ�������м���������NaOH��Һ��������ɵ�����(��״������ͬ)���Ϊb L����Ʒ������������_____________g��
(2) ��ȡa g��Ʒ�����ȼ��ǡ����ȫ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�________����������������������________��
(3) ��(2)�з�Ӧ������ȴ�����������ᣬ������ɵ��������Ϊc L����������(1)����������������c��b=______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�������������(AG)����ʾ��Һ����ԣ���ȵļ��㹫ʽ��AG��lg[c(H+)/c(OH-)]������������ȷ����(����)
A.������Һ��AG��1
B.������Һ��AG��0
C.������0.1 mol��L��1NaOH��Һ��AG��12
D.������0.1 mol��L��1������Һ��AG��12
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com