
【题目】海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。其流程如图所示:
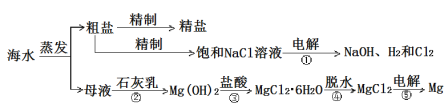
(1)写出镁原子的结构示意图:_______。在反应①→⑤中属于氧化还原反应的是______。(填序号)
(2)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、________溶液;③_________;④滤液中加适量盐酸;⑤__________。(请补全缺少的实验步骤或试剂)
(3)某同学利用反应①原理制备氯气,将400 mL 5.0 mol·L-1NaCl溶液进行电解,则理论上最多可制得标准状况下氯气的体积为_____L。
(4)实验室模拟Mg的制取流程时,用11.3 mol·L-1的浓盐酸配置反应③所需要的0.5 mol·L-1稀盐酸100 ml,需要用量筒量取浓盐酸________ml,接下来的配置过程除了玻璃棒和烧杯外,还需要用到的玻璃仪器有_______。
【答案】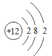 ①⑤ Na2CO3 过滤 蒸发结晶 22.4 4.4 胶头滴管、100ml容量瓶
①⑤ Na2CO3 过滤 蒸发结晶 22.4 4.4 胶头滴管、100ml容量瓶
【解析】
(1)镁离子质子数为12,核外电子数为10,有2个电子层,各层电子数为2、8;有元素化合价发生变化的反应属于氧化还原反应,结合具体反应判断;
(2)镁离子与氢氧根离子生成氢氧化镁沉淀;钙离子与碳酸根反应生成碳酸钙沉淀;
(3)根据n=cV计算NaCl的物质的量,结合方程式计算生成氯气的体积;
(4)根据配制一定物质的量浓度溶液需要仪器分析。
(1)镁的质子数为12,镁原子结构示意图为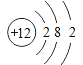 ;反应①是电解食盐水生成氢氧化钠、氯气与氢气,属于氧化还原反应,反应②是溶液中镁离子与石灰乳反应生成氢氧化镁沉淀,属于非氧化还原反应,反应③是氢氧化镁与盐酸反应,属于非氧化还原反应,反应④是氯化镁晶体失去结晶水得到氯化镁,属于非氧化还原反应,反应⑤是电解熔融氯化镁生成镁与氯气,属于氧化还原反应,
;反应①是电解食盐水生成氢氧化钠、氯气与氢气,属于氧化还原反应,反应②是溶液中镁离子与石灰乳反应生成氢氧化镁沉淀,属于非氧化还原反应,反应③是氢氧化镁与盐酸反应,属于非氧化还原反应,反应④是氯化镁晶体失去结晶水得到氯化镁,属于非氧化还原反应,反应⑤是电解熔融氯化镁生成镁与氯气,属于氧化还原反应,
故答案为: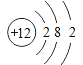 ;①⑤;
;①⑤;
(2)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,最后过滤,向滤液加入盐酸酸化。但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,因此为制得纯净的NaCl晶体,操作如下:①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③过滤;④滤液中加适量盐酸;⑤蒸发结晶,故答案为:Na2CO3;过滤;蒸发结晶;
(3)400mL5molL-1NaCl溶液中NaCl的物质的量=0.4L×5mol/L=2mol,由2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑可知生成氯气为2mol×1/2=1mol,标况下,生成氯气的体积=1mol×22.4L/mol=22.4L,
2NaOH+Cl2↑+H2↑可知生成氯气为2mol×1/2=1mol,标况下,生成氯气的体积=1mol×22.4L/mol=22.4L,
故答案为:22.4;
(4)由于稀释过程中溶质的物质的量不变,则需要用量筒量取浓盐酸的体积为![]() ≈4.4mL;用浓盐酸配制稀盐酸的一般步骤分别是计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,需要的仪器除了量筒、玻璃棒和烧杯外,还需要用到的玻璃仪器有胶头滴管、100mL容量瓶,
≈4.4mL;用浓盐酸配制稀盐酸的一般步骤分别是计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,需要的仪器除了量筒、玻璃棒和烧杯外,还需要用到的玻璃仪器有胶头滴管、100mL容量瓶,
故答案为:4.4;胶头滴管、100mL容量瓶。


科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是_____,D是_____,G是_____,H是_____(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:__________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为_________。
(3)A中元素的原子结构示意图为________。
(4)F在溶液中的电离方程式为_________。
(5)上述反应中属于氧化还原反应的是_______(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种无色无味的气体,微溶于水,易溶于有机溶剂。实验室常用如图所示装置制取乙炔,并验证乙炔的性质。完成实验,观察实验现象,回答下列问题:

(1)写出电石(碳化钙CaC2)与水反应,制取乙炔的化学方程式_________
(2)用饱和食盐水代替蒸馏水的目的是____________
(3)装置A的作用是_________,装置B中的现象是___________
(4)若称取a g CaC2,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中溶液增重b g,则CaC2的纯度为____________(用百分数表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+B(g)![]() 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
A. v(A)=0.15mol·(L·min) -1B. v (B)=0.2 mol·(L·min) -1
C. v (C)=0.3 mol·(L·min) -1D. v (D)=0.1 mol·(L·min) -1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋酸钠(NaBiO3)常用作Mn2+鉴定的强氧化剂,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量Bi2O3、SiO2等杂质)制备铋酸钠,其流程如图:
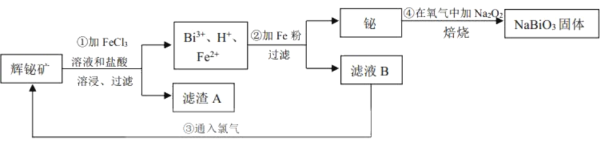
己知:①NaBiO3是一种难溶于水的物质
②BiCl3极易水解生成不溶性的BiOCl沉淀
请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有___(填标号)。
a.加入足量的蒸馏水 b.搅拌 c.粉碎矿石 d.降低温度
(2)溶浸时通常加入FeCl3溶液和浓盐酸,加入的浓盐酸需过量的目的是___,滤渣A的主要成分为___(填化学式)。
(3)反应④的化学方程式为___。
(4)NaBiO3可在酸性介质中将Mn2+氧化为MnO![]() ,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为___。
,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为___。
(5)实验室为了测定NaBiO3样品的纯度,需要配制250mL0.500mol/LFeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒外,还需要___。
(6)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,稀释至100mL,取出20.00mL溶液,然后用新配制的0.500mol/LFeSO4溶液进行滴定,滴定完成后消耗24.80mLFeSO4溶液。则该样品中NaBiO3纯度为___%(结果保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿巴卡韦(Abacavir)是一种核苷类逆转录酶抑制剂,存在抗病毒功效。关于其合成中间体M(![]() ),下列说法正确的是( )
),下列说法正确的是( )
A.与环戊醇互为同系物
B.分子中所有碳原子共平面
C.能使酸性高锰酸钾溶液和溴水褪色,且反应类型相同
D.可用碳酸钠溶液鉴别乙酸和M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,2.8g 由CO与CO2组成的混合物中含有的质子总数为1.4NA
B.标准状况下,22.4 L H2O中含有的分子数为NA
C.2.3g Na与100 mL 0.1mol·L-1盐酸反应,转移的电子数为0.01NA
D.1L 1 mol·L-1 CaCl2溶液中含有的氯离子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2 mol·L-1的CH3COOH溶液中,当CH3COOH![]() H++CH3COO-已达平衡时,若要使CH3COOH的电离程度减小,溶液中的c(H+)增大,应加入( )
H++CH3COO-已达平衡时,若要使CH3COOH的电离程度减小,溶液中的c(H+)增大,应加入( )
A.CH3COONa固体B.氨水C.HClD.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在科学研究和工业生产中具有许多用途。请回答下列问题:
(1)画出基态Cu原子的价电子排布图__________________;
(2)已知高温下Cu2O比CuO稳定,从核外电子排布角度解释高温下Cu2O更稳定的原因_________________________________________________________________________。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是____________,配体中提供孤对电子的原子是____________。C、N、O三元素的第一电离能由大到小的顺序是__________(用元素符号表示)。
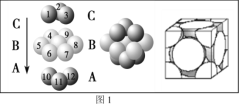
(4)铜晶体中铜原子的堆积方式如图1所示,则晶体铜原子的堆积方式为________________。
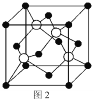
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(白球代表铜原子)。
①该晶体的化学式为_________________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于_________化合物(填“离子”、“共价”)
③已知该晶体的密度为![]() g/cm3,阿伏加德罗常数的值为NA,则该晶体中Cu原子和M原子之间的最短距离为_________pm(写出计算式)。
g/cm3,阿伏加德罗常数的值为NA,则该晶体中Cu原子和M原子之间的最短距离为_________pm(写出计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com