
【题目】工业上可通过煤的液化合成甲醇,主反应为:CO(g)+2H2(g)=CH3OH(l) △H=x
(1)己知常温下CH3OH、H2和CO的燃烧热分別为726.5kl/mo1、285.5kJ/mol、283.0kJ/mol,則x=_______;为提高合成甲醇反应的选择性,关键因素是___________。
(2)TK下,在容积为1.00 L的某密闭容器中进行上述反应(CH3OH为气体),相关数据如图。

①该反应0-10min的平均速率v(H2)=_______;M和N点的逆反应速率较大的是______(填“v逆(M)”、“v逆(N)”或“不能确定”)。
②10min时容器内CO的体积分数为_______。相同条件下,若起始投料加倍,达平衡时,CO的体积分数将________(填“增大”、“减小”或“不变”)
③对于气相反应,常用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)表示平衡常数(以Kp表示),其中,PB=P总×B的体积分数;若在TK下平衡气体总压强xatm,则该反应Kp=____(计算表达式)。实验测得不同温度下的lnK(化学平衡常数K的自然对数)如图,请分析lnK随T呈现上述变化趋势的原因是:____________。

【答案】-127.5kJ/mol 催化剂(或提高催化剂的选择性) 0.12mol/(L·min) 不能确定 2/9(或22.22%) 减小 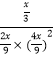 该反应正反应为放热反应,当温度升高平衡逆向移动,平衡常数(Kp或lnKp)减小
该反应正反应为放热反应,当温度升高平衡逆向移动,平衡常数(Kp或lnKp)减小
【解析】
(1)CH3OH、H2和CO的燃烧热分別为726.5kl/mo1、285.5kJ/mol、283.0kJ/mol,则CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l);△H=-726.5 kJ/mol①;H2(g)+
O2(g)=CO2(g)+2H2O(l);△H=-726.5 kJ/mol①;H2(g)+![]() O2(g)═H2O;△H=-285.5kJ/mol②;CO(g)+
O2(g)═H2O;△H=-285.5kJ/mol②;CO(g)+![]() O2(g)═CO2(g);△H=-283kJ/mol③,根据盖斯定律计算CO(g)+2H2(g)=CH3OH(l)的△H;选择合适的催化剂可以提高合成甲醇反应的选择性;(2) ①根据
O2(g)═CO2(g);△H=-283kJ/mol③,根据盖斯定律计算CO(g)+2H2(g)=CH3OH(l)的△H;选择合适的催化剂可以提高合成甲醇反应的选择性;(2) ①根据![]() 计算;10min时氢气浓度逐渐减小,平衡正向移动,改变的条件可能是加入CO(g)或分离出甲醇或降低温度;②根据图示10min时容器内CO的物质的量是0.4mol、氢气的物质的量是0.8mol、甲醇的物质的量是0.6mol;相同条件下,若起始投料加倍,相当于加压,平衡正向移动;③
计算;10min时氢气浓度逐渐减小,平衡正向移动,改变的条件可能是加入CO(g)或分离出甲醇或降低温度;②根据图示10min时容器内CO的物质的量是0.4mol、氢气的物质的量是0.8mol、甲醇的物质的量是0.6mol;相同条件下,若起始投料加倍,相当于加压,平衡正向移动;③![]() ,带入压强计算Kp;该反应正反应为放热反应,当温度升高平衡逆向移动。
,带入压强计算Kp;该反应正反应为放热反应,当温度升高平衡逆向移动。
(1)CH3OH、H2和CO的燃烧热分別为726.5kl/mo1、285.5kJ/mol、283.0kJ/mol,则CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l)△H=-726.5 kJ/mol ①;H2(g)+
O2(g)=CO2(g)+2H2O(l)△H=-726.5 kJ/mol ①;H2(g)+![]() O2(g)═H2O;△H=-285.5kJ/mol②;CO(g)+
O2(g)═H2O;△H=-285.5kJ/mol②;CO(g)+![]() O2(g)═CO2(g);△H=-283kJ/mol③,根据盖斯定律③+②×2-①得 CO(g)+2H2(g)=CH3OH(l) △H=-283kJ/mol-285.5kJ/mol×2+726.5 kJ/mol =-127.5 kJ/mol;选择合适的催化剂可以提高合成甲醇反应的选择性,所以关键因素是催化剂;(2) ①
O2(g)═CO2(g);△H=-283kJ/mol③,根据盖斯定律③+②×2-①得 CO(g)+2H2(g)=CH3OH(l) △H=-283kJ/mol-285.5kJ/mol×2+726.5 kJ/mol =-127.5 kJ/mol;选择合适的催化剂可以提高合成甲醇反应的选择性,所以关键因素是催化剂;(2) ①![]() mol/(L·min);10min时氢气浓度逐渐减小,平衡正向移动,改变的条件可能是加入CO(g)或分离出甲醇或降低温度。若加入CO(g)反应速率加快;若分离出甲醇或降低温度,反应速率减慢,所以不能确定M和N点的逆反应速率的大小;②根据图示10min时容器内CO的物质的量是0.4mol、氢气的物质的量是0.8mol、甲醇的物质的量是0.6mol,CO的体积分数为
mol/(L·min);10min时氢气浓度逐渐减小,平衡正向移动,改变的条件可能是加入CO(g)或分离出甲醇或降低温度。若加入CO(g)反应速率加快;若分离出甲醇或降低温度,反应速率减慢,所以不能确定M和N点的逆反应速率的大小;②根据图示10min时容器内CO的物质的量是0.4mol、氢气的物质的量是0.8mol、甲醇的物质的量是0.6mol,CO的体积分数为![]() 22.22% ;相同条件下,若起始投料加倍,相当于加压,平衡正向移动,所以CO的体积分数将减小;③ Kp=
22.22% ;相同条件下,若起始投料加倍,相当于加压,平衡正向移动,所以CO的体积分数将减小;③ Kp=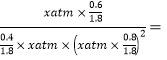
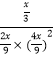 ;该反应正反应为放热反应,当温度升高平衡逆向移动,平衡常数(Kp或lnKp)减小。
;该反应正反应为放热反应,当温度升高平衡逆向移动,平衡常数(Kp或lnKp)减小。


科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)写出二氧化碳的电子式________________。
(2)写出有机物CH3CH2CH2CH(CH3)2的名称__________________。
(3)铁片、铜片连接后浸入稀硫酸形成原电池,正极反应式是_________________。
(4)乙醇的热值为Q kJ·g-1,写出乙醇完全燃烧生成CO2气体和液态水的热化学方程式______________。
(5)写出苯与浓硫酸、浓硝酸在55℃下反应的化学方程式____________________。
(6)烃X分子中碳与氢的质量比为36∶7,化学性质与甲烷相似,则烃X的同分异构体共有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 同主族非金属元素的简单阴离子的还原性越强,其元素非金属性越强
B. ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
C. 元素原子的最外层电子数等于元素的最高化合价
D. 全部由非金属元素组成的化合物中只含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如图所示:
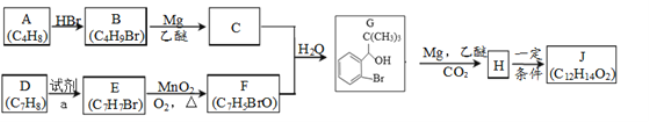
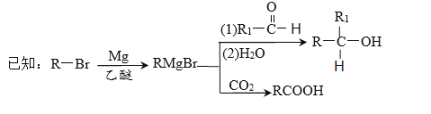
(1)A的名称是_______,E到F的反应类型是___________。
(2)试剂a是________,F中官能团名称是_______。
(3)M组成比F多1个CH2,M的分子式为C8H7BrO,M的同分异构体中:①能发生银镜反应;②含有苯环;③不含甲基。满足上述条件的M的同分异构体共有______种。
(4)J是一种酯,分子中除苯环外还含有一个五元环,J的结构简式为__________。H在一定条件下还能生成高分子化合物K,H生成K的化学方程式为________。
(5)利用题中信息写出以乙醛和苯为原料,合成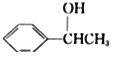 的路线流程图(其它试剂自选)。________。
的路线流程图(其它试剂自选)。________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质的说法中正确的是( )
A.氢氧化钠固体溶于水后能导电,所以氢氧化钠是电解质
B.二氧化碳水溶液能够导电,所以二氧化碳是电解质
C.铁、铜能导电,所以铁、铜为电解质
D.氯化铁溶液能够导电,所以氯化铁溶液是电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com