
【题目】短周期主族元素 W、X、Y、Z 的原子序数依次增大,W、X 原子的最外层电子数之比为 4:3,Z 原子比 X 原子的核外电子数多 4。下列说法正确的是
A.W、Y、Z 的电负性大小顺序一定是 Z>Y>W
B.W、X、Y、Z 的原子半径大小顺序可能是 W>X>Y>Z
C.Y、Z 形成的分子空间构型可能是正四面体
D.WY2 分子中![]() 键与π键的数目之比是 2:1
键与π键的数目之比是 2:1
【答案】C
【解析】
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,由于最外层电子数不超过8,故W的最外层电子数为4,处于第ⅣA族,X的最外层电子数为3,处于第ⅢA族,原子序数X大于W,故W为C元素,X为Al元素,Z原子比X原子的核外电子数多4,故Z的核外电子数为17,则Z为Cl元素,Y的原子序数大于铝元素,小于氯元素,故Y为Si或P或S元素,据此解答。
A.同主族自上而下电负性逐渐减弱,Y若为Si元素,则电负性C>Si,A错误;
B.同周期自左而右原子半径逐渐减小,电子层越多原子半径越大,故原子半径Al>Y>Cl>C,B错误;
C.若Y、Z形成的分子为SiCl4,中心原子Si形成4个![]() 键,无孤电子对,为sp3杂化,正四面体构型,C正确;
键,无孤电子对,为sp3杂化,正四面体构型,C正确;
D.WY2分子为CS2,分子结构式为S=C=S,每个双键中含有1个![]() 键、1个π键,故δ键与π键的数目之比1:1,D错误。
键、1个π键,故δ键与π键的数目之比1:1,D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】有一含Ni的单核六配位配合物,其阳离子空间结构为八面体。1mol该配合物的稀水溶液与足量![]() 混合生成
混合生成![]() 沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为
沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为![]() 。
。
(1)请画出Ni的价电子排布图:______________________,H、N、O的电负性由大到小的顺序为______________________。
(2)滤液与硝酸银溶液混合不生成沉淀的原因是___________________________________。
(3)该配合物阴离子的中心原子杂化方式为____________,请写出该配合物的化学式:________________。
(4)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可以在多个原子间运动,形成“离域![]() 键”。下列微粒中存在“离域
键”。下列微粒中存在“离域![]() 键”的是_________
键”的是_________![]() 填序号
填序号![]() 。
。
A.![]()
![]()
![]()
![]() 苯
苯
(5)如图是六方NiAs晶胞的晶胞图及坐标参数,其中![]() ,
,![]() ,
,![]() 。晶胞顶点、棱上小球为Ni,As在体内。
。晶胞顶点、棱上小球为Ni,As在体内。

①写出As的配位数为_________,Ni的配位数为_________。
②已知晶胞参数为![]() ,
,![]() ,则晶胞的密度为____________
,则晶胞的密度为____________![]() 写表达式
写表达式![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
A. 0.4mol
B. 0.2mol
C. 小于0.2mol
D. 大于0.2mol,小于0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化碳结构如下图所示,其硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法不正确的是 ( )
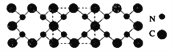
A. 氮化碳属于原子晶体
B. 氮化碳中碳显-4价,氮显+3价
C. 氮化碳的化学式为C3N4
D. 每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把含有某一氯化物杂质的氯化钙5.55克溶于水后,与足量的硝酸银溶液反应,生成的氯化银沉淀15克,则该杂质可能是
A.氯化钠B.氯化钾
C.氯化铜D.氯化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:①乙醇蒸气通过红色粉末(CrO3),红色粉末变成绿色粉末(Cr2O3),生成乙醛。②乙醛能还原酸性高锰酸钾溶液。某小组设计如下装置制备少量乙醛。下列说法错误的是( )
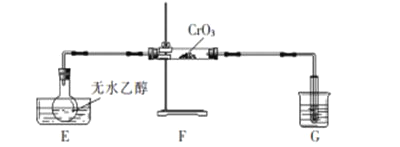
A.水槽E中装热水,烧杯G中装冷水
B.检验乙醛的方法是向反应后的溶液中滴加酸性高锰酸钾溶液
C.E中增加一支温度计,有利于提高乙醇的利用率
D.常采用蒸馏操作分离、纯化粗产品中的乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素组成的单质X2、Y,标准状况下X2的密度为3.17gL-1,常温下,Y为浅黄色固体。Z是一种化合物,焰色反应呈浅紫色![]() 透过钴玻璃
透过钴玻璃![]() ;0.1molL-1Z的水溶液pH=13。X2、Y和Z之间有如下转化关系
;0.1molL-1Z的水溶液pH=13。X2、Y和Z之间有如下转化关系![]() 其他无关物质已略去
其他无关物质已略去![]() :
:
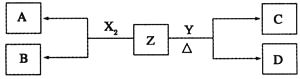
(1)写出单质X2与Z反应的离子方程式:______________________________________。
(2)已知16g单质Y完全燃烧放出148kJ热量。写出热化学方程式:________________。
(3)已知C能与较浓盐酸反应生成能使品红溶液褪色的气体
①D的化学式是:_________;D的水溶液pH>7,原因是![]() 用离子方程式表示
用离子方程式表示![]() :_____________。
:_____________。
②0.1molL-1的D溶液中各离子浓度由大到小的顺序为_______________________。
③将20mL0.5molL-1溶液逐滴加入到20mL0.2molL-1 KMnO4溶液![]() 硫酸酸化
硫酸酸化![]() 中,溶液恰好褪为无色。写出反应的离子方程式:_________________________________。
中,溶液恰好褪为无色。写出反应的离子方程式:_________________________________。
(4)①石墨和铁做电极,用隔膜电解槽电解A的溶液,阳极可产生X2。则铁做_________极。
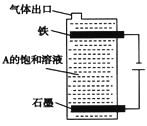
②按下图电解A的饱和溶液,写出该电解池中较长时间内发生反应的总反应方程式: ________。将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的现象是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学配置450毫升 1mol/L的硫酸溶液
(1)应该选择________的容量瓶 A 250毫升 B 500毫升 C 1000毫升
(2)需要量取98%,ρ=1.84g/cm3浓硫酸__________毫升
(3)将所取浓硫酸逐滴加入盛有水的烧杯中,边加边搅拌
(4)将该溶液注入容量瓶
(5)在容量瓶中加水至___________处,改用__________加水至_______与刻度线相切
(6)塞好瓶塞,反复摇匀
(7)摇匀后发现,溶液体积缩小,继续加水至刻度线
(8)该同学的操作是否有不当之处,请指出(不必全部填满)
a__________________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
b____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
c_______________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
d____________该错误操作将使所配溶液的浓度_______(“变大”或“变小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2A+B![]() 3C+4D,表示反应速率最快的是
3C+4D,表示反应速率最快的是
A.VA=0.75mol/(L·s)B.VB=0.5mol/(L·s)C.VC=1.0mol/(L·s)D.VD=1.5mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com