
【题目】(题文)(题文)在恒温、恒容条件下,能说明可逆反应:H2(g)+I2(g) 2HI(g)达到平衡状态的是
A. 气体的压强保持不变 B. v(H2)正=2v(HI)逆
C. 气体的密度保持不变 D. 气体的颜色保持不变
【答案】D
【解析】
化学平衡状态是可逆反应在一定条件下正逆反应速率达到相等、各物质的浓度保持不变的状态,故判断一个可逆反应是否达到平衡状态可抓住这两个标准来进行分析。
A.因为反应H2(g)+I2(g)![]() 2HI(g)是一个反应前后分子数目不变的反应,在反应的过程中气体的压强始终不变,则气体的压强不变不能说明反应达到平衡状态,故A项错误;B.根据方程式的计量数可得当达到平衡状态时应有2v(H2)正=v(HI)逆,故B项错误;C.在恒容条件下,由反应的质量守恒可知反应混合物的密度始终不会改变,所以气体的密度不变不能说明可逆达到平衡状态,故C项错误;D.气体的颜色不变即碘蒸气的浓度不变,反应处于平衡状态,故D项正确;答案选D。
2HI(g)是一个反应前后分子数目不变的反应,在反应的过程中气体的压强始终不变,则气体的压强不变不能说明反应达到平衡状态,故A项错误;B.根据方程式的计量数可得当达到平衡状态时应有2v(H2)正=v(HI)逆,故B项错误;C.在恒容条件下,由反应的质量守恒可知反应混合物的密度始终不会改变,所以气体的密度不变不能说明可逆达到平衡状态,故C项错误;D.气体的颜色不变即碘蒸气的浓度不变,反应处于平衡状态,故D项正确;答案选D。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】过氧化氢H2O2(氧的化合价为﹣1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl===2NaCl+H2O2
B.Ag2O+H2O2===2Ag+O2+H2O
C.2H2O2===2H2O+O2
D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是_________(填代号)。
(2)H2O2既体现氧化性又体现还原性的反应是_________(填代号)。
(3)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2﹣2e﹣===2H++O2↑
还原反应:MnO![]() +5e﹣+8H+===Mn2++4H2O
+5e﹣+8H+===Mn2++4H2O
写出该氧化还原反应的离子方程式:___________________。
(4)在K2Cr2O7+14HCl===2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3 mol电子转移时生成Cl2的体积为______(标准状况),被氧化的HCl的物质的量为____。
(5)除去镁粉中混入的铝粉杂质用溶解、_______方法,化学反应方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知20℃时,饱和NaCl溶液的密度为ρg/cm3,物质的量浓度为c mol/L,则下列说法中不正确的是
A. 温度低于20℃时,饱和NaCl溶液的浓度小于c mol/L
B. 此溶液中NaCl的质量分数为![]()
C. 20℃时,密度小于ρg/cm3的NaCl溶液是不饱和溶液
D. 20℃时,饱和NaCl溶液的溶解度![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(l)天然气和CO2通入聚焦太阳能反应器,发生反应CH4(g)+ CO2(g)![]() 2CO(g)+2H2(g) ΔH。已知:CH4、H2、CO的燃烧热ΔH分别为-akJ/mol、-bkJ/mol、-ckJ/mol。则上述反应中,ΔH=_______________(用含a、b、c的代数式表示)kJ/mol。
2CO(g)+2H2(g) ΔH。已知:CH4、H2、CO的燃烧热ΔH分别为-akJ/mol、-bkJ/mol、-ckJ/mol。则上述反应中,ΔH=_______________(用含a、b、c的代数式表示)kJ/mol。
(2)CO2和H2可以合成二甲醚(CH3OCH3)。二甲醚是一种绿色环保型能源,以稀硫酸为电解质溶液,若某二甲醚空气燃料电池每消耗l mol CH3OCH3,电路中通过9 mol电子,则该电池效率η为___________。(提示:电池效率等于电路中通过的电子数与电池反应中转移电子总数之比)
(3)325K时,在恒容密闭容器中充入一定量NO2 ,发生反应:2NO2(g)![]() N2 O4(g)。
N2 O4(g)。
①NO2与N2O4的消耗速率与其浓度的关系如图所示,图中交点A表示该反应所处的状态为:____________;
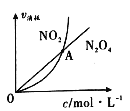
A.平衡状态 B.朝正反应方向移动 C.朝逆反应方向移动 D.无法判断
② 能够说明上述反应已经达到平衡状态的有__________________;
a.NO2和N2 O4的物质的量相等 b.体系颜色不再变化
c.容器内混合气体的密度不再改变 d.容器内气体压强不发生变化
③若达到平衡后容器内混合气体的平均相对分子质量为57.5。平衡时NO2的转化率为_____。
(4)实验中多余的SO2可以用氢氧化钠溶液吸收。常温下H2SO3的Ka1=1.3×10-2、Ka2=6.6×10-8。
①室温下pH=3的亚硫酸溶液,下列判断正确的是_______________。
a.溶液中c(H2SO3)>c(SO32—) b.溶液中c(SO32—):c(HSO3—)=6.6×10-5
c.溶液中氢离子数目为6.02×1020个 d.加入等体积pH=3的硫酸溶液,亚硫酸的电离平衡不移动
②常温下,用含1mol氢氧化钠的稀溶液吸收足量SO2气体,放出热量为QkJ,该反应的热化学方程式为_______
③若吸收液中c(HSO3—)=c(SO32—),则溶液中c(H+)=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:
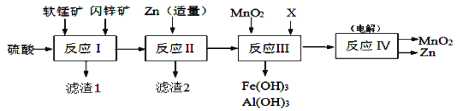
已知:反应Ⅰ中所有金属元素均以离子形式存在。有关常数:Ksp[Al(OH)3]=1.0×10-33、Ksp[Fe(OH)3]=3.0×10-39、Ksp[Mn(OH)2]=2.0×10-13、Ksp[Zn(OH)2]=1.0×10-17、Ksp(MnCO3)=2.0×10-11、Ka1(H2CO3)=4.0×10-7、Ka2(H2CO3)=5.6×10-11。回答下列问题:
(1)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应的离子方程式____________________________。
(2)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,滤渣2的主要成分是___________。
(3)反应Ⅲ中MnO2的作用是_______________________,若反应后溶液中Mn2+、Zn2+均为0.1mol·L-1,需调节溶液pH范围为_______________(溶液中,当一种离子的浓度小于10-6mol/L时可认为已不存在),X可以是_________。(填字母代号)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反应Ⅳ中电极均是惰性电极,写出阳极电极反应式________________________。本工艺可以循环利用的物质有MnO2、Zn和_________。
(5)MnCO3有多种用途。废水处理领域中常用NH4HCO3溶液将Mn2+转化为MnCO3,该反应的离子方程式为______。试通过题述有关数据简要计算说明该反应能进行的原因:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关溶液的说法正确的是( )
A. pH相等的①NH4Cl、②NH4Al(SO4)2、③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×1010,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F) >c(K+ ) c(CH3COO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2s后测得C的浓度为0.6mol/L,现有几种说法:
①用物质A表示的反应的平均速率为0.3 mol/Ls
②用物质B表示的反应的平均速率为0.6 mol/Ls
③2s时物质A的转化率为70%
④2s时B物质的浓度为0.7 mol/L
其中正确的是( )
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列判断正确的是
A. 0.1 mol Na2O2含有的离子总数为0.4NA
B. 常温常压下,18g H2O 所含的中子数为8NA
C. 5.6 g铁与足量盐酸反应转移的电子数为0.3NA
D. 将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将以下4份溶液分别置于如图的装置中,其它条件相同时,灯泡最亮的是
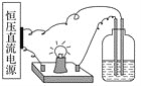
A. 100 mL 1 mol·L-1的盐酸
B. 100 mL 2 mol·L-1的蔗糖溶液
C. 100 mL 1 mol·L-1的醋酸溶液
D. 30 mL 1 mol·L-1的氯化铝溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com