
����Ŀ����������2017�쿼ǰģ���̴�о�����3�ֲ�ͬ�����£��ֱ����ݻ�Ϊ2L�ĺ����ܱ������г���2 mol A��1 mol B��������Ӧ��2A(g) + B(g)![]() 2D(g) ��H=Q kJ��mol�C1��������������ݼ��±���
2D(g) ��H=Q kJ��mol�C1��������������ݼ��±���
ʵ���� | ʵ��� | ʵ��� | ʵ��� |
��Ӧ�¶�/�� | 700 | 700 | 750 |
��ƽ��ʱ��/min | 40 | 5 | 30 |
n(D)ƽ��/ mol | 1.5 | 1.5 | 1 |
��ѧƽ�ⳣ�� | K1 | K 2 | K 3 |
����˵����ȷ����
A��K 3��K 2��K 1
B��ʵ������ʹ���˴���
C��ʵ����ƽ��������ڵ�ѹǿ��ʵ����![]() ��
��
D��ʵ����ƽ�����������������ͨ��1 mol A��1 mol D��ƽ�ⲻ�ƶ�
���𰸡�BD
�����������ݱ������ݣ������¶ȵ�750�棬n(D)��С��ƽ�������ƶ���K 3<K 2��K 1����A����ʵ�����ʵ�����ȣ�ƽ��û�ƶ�������Ӧ���ʼӿ죬����ʵ������ʹ���˴�������B��ȷ��ʵ�����ʵ����¶Ȳ�ͬ������ѹǿ�������ʵ����ȣ���C����ʵ����ƽ�ⳣ����
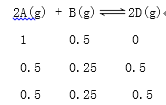
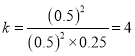 ������������������ͨ��1 mol A��1 mol D��A��Ũ�ȱ�Ϊ1��D��Ũ�ȱ�Ϊ1��
������������������ͨ��1 mol A��1 mol D��A��Ũ�ȱ�Ϊ1��D��Ũ�ȱ�Ϊ1�� ![]() ��
�� ![]() ������ƽ�ⲻ�ƶ�����D��ȷ��
������ƽ�ⲻ�ƶ�����D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��ȷ������������
A. ����ϡ���2Fe +6H+=2Fe3��+3H2��
B. ʯ������Na2CO3��Һ��ϣ�Ca��OH��2 +CO32��= CaCO3��+2OH��
C. ����ʯ���ڴ�����Һ�ķ�Ӧ��CaCO3+ 2H+��Ca2++CO2��+H2O
D. ���ˮ�еμ�FeCl3��Һ�Ʊ�Fe��OH��3���壺Fe3+��3H2O![]() Fe��OH��3����3H+
Fe��OH��3����3H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ��е�VIIA��Ԫ�صĵ��ʼ��仯�������;�㷺��
(1)��Ԫ��ͬ�����һ����Ԫ�ص�ԭ�ӽṹʾ��ͼΪ_______������______ (����ɫ)�������ʡ�
(2)���ݵ���ʵ�������������ǻ���ʯ[Ca5(PO4)3OH]�ܽ�Ľ������մ���������ϣ���ø�������²����������ʣ������ȣ�ݡ�ʹ�ú�������ᱣ�����ݣ���Ϊ�����ӻ���ǻ���ʯ[Ca5(PO4)3OH]������Ӧ���ɷ���ʯ������ʯ���ǻ���ʯ���ֿܵ������ʴ���������ӷ���ʽ��ʾ��һ����___________�����������ӻ������ƿ�ǻϸ�������ᣬ�������༺���ձ�ʹ�á�
(3)�ⱻ��Ϊ������Ԫ�ء��������(KIO3)�ǹ��ҹ涨��ʳ�μӵ�������ľ���Ϊ��ɫ��������ˮ������������Խ�������⻯�����ɵ��ʵ⡣д���÷�Ӧ�����ӷ���ʽ_____________��
(4)������װ��KI��������Һ���м��������ӽ���Ĥ�������ڡ����ĵ�ѹ��ͨ�磬���������Һ����ɫ��һ��ʱ�����ɫ��dz�������ϣ��ӵ��Һ�еõ�����ؾ����ʵ��������£�
![]()
����ݵIJ�������____________________��
(5)��֪��I2+2S2O32-=S4O62-+2I-��
�á���ӵ��������ⶨ����CuCl2��2H2O�������������������I-������Ӧ�����������ʣ��Ĵ��ȣ��������£�ȡag��������ˮ���������KI���壬��ַ�Ӧ�����ɰ�ɫ������I-������ΪI2��Ȼ����cmol/L Na2S2O3����Һ�ζ�������ζ��յ�ʱ������Na2S2O5����ҺbmL����ѡ��______���ζ�ָʾ�����ζ��յ��������_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ͻ�ѧʽ���Ǻϵ���
A. ���� KAl��SO4��2��12H2O B. �ؾ�ʯ BaSO4
C. ��ʯ�� 2CaSO4��H2O D. �̷� CuSO4��5H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ÿ���n(H2S):n(FeCl3)=1:2��Ӧ�õ��IJ������õ�ⷨ���⣬�乤��ԭ����ͼ��ʾ�������йص�˵���������ǣ� ��
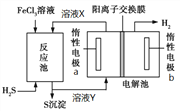
A. ���Ե缫aΪ����������Ӧ
B. Fe(OH)3�����еμ���ҺX�����г���������ܽ�
C. ��ҺY���������������յõ�Fe2O3
D. �����ܷ�Ӧ�����ӷ���ʽΪ2Fe2����2H��![]() 2Fe3����H2��
2Fe3����H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������������ء�����˵���������
A. �ð�������װʳƷ�������� B. ʳƷ����Ĥ�ܼ���ʳƷ��ˮ�ֵ�����
C. ��Һ��������������Ʒ D. �ó�����ҽ����е��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ������ ��
A. ��0.1 molL��1CH3COOH��Һ�м�������ˮ����Һ��![]() ��С
��С
B. ��CH3COONa��Һ��20��������60������Һ��![]() ����
����
C. �������м��백ˮ�����ԣ���Һ��![]()
D. ��AgCl��AgBr�ı�����Һ�м�������AgNO3����Һ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ֳ��á�����λ��NOx����������⻯�����ĵ������������Ƿ�ﵽ�ŷű����乤��ԭ����ͼ��ʾ������˵������ȷ���ǣ�������

A. ���Ե缫���Ǹ���
B. �������缫���Ϸ����ĵ缫��ӦΪNO2+2e-+2H+�TNO+H2O
C. ����������ʱH+�ɹ����缫����Ե缫
D. �Ե缫�IJ��Ͽ���Ϊ���ý���п
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.�Ӻ�ˮ�õ��Ĵ�ʳ��ˮ�г���Ca2����Mg2����SO![]() ����Ҫ�����ᴿ�����к�����CaCl2��MgSO4�Ĵ�ʳ��ˮ���ڳ�ȥ���������ɳ֮��Ҫ��4���Լ������ᡢ��Na2CO3����NaOH����BaCl2����ȥʳ��ˮ��Ca2����Mg2����SO
����Ҫ�����ᴿ�����к�����CaCl2��MgSO4�Ĵ�ʳ��ˮ���ڳ�ȥ���������ɳ֮��Ҫ��4���Լ������ᡢ��Na2CO3����NaOH����BaCl2����ȥʳ��ˮ��Ca2����Mg2����SO![]() ���ᴿʱ�IJ�������ͼ����Լ��������ͼ��
���ᴿʱ�IJ�������ͼ����Լ��������ͼ��

ͼ��a��b��c��d�ֱ��ʾ����4���Լ��е�һ�֣��Իش�
(1)����A��������________��
(2)�Լ�d��________���ж��Լ�d�Ѿ������ķ�����
________________________________________________________________________��
(3)����b��c����Һ�з����Ļ�ѧ��Ӧ�Ļ�ѧ����ʽΪ
________________________________________________________________________��
(4)�����������������˳�����A��B��Cʱ�����õ�����____(�����)�������۵�������________��

��.�������������ʾ����������Եõ���ˮ�����ӵ�ˮ����ȡ�⣬��Ҫ���������е� ________(�����)������������Ϊ________����õ�ˮ�м������Ȼ�̼����ȡ�ⵥ�ʵ�ʵ���������________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com