
【题目】无水氯化铁加热易升华,遇潮湿空气易变质。在实验室中,可以采用如下装置和药品制取较纯的无水氯化铁固体。
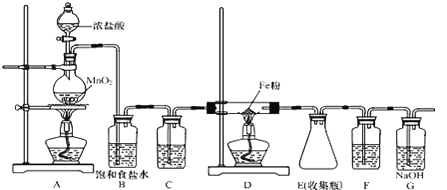
(1)制取氯化铁时,应先点燃_____(填“A”或“D”)处的酒精灯,制取氯化铁的化学方程式为_____。
(2)C、F装置中所装试剂相同,试剂均为________。
(3)下列收集Cl2的正确装置是______。
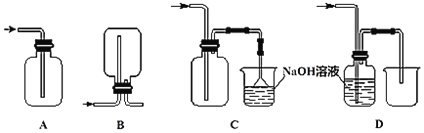
(4)G装置中反应的离子方程式为________________________________。
(5)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血红色,推断固体物质的成分为______(选填序号,下同);写出溶液变血红色的离子方程式:_____________,若溶液未变血红色,推断固体物质的成分为______。
A.只有 FeCl3 B.只有Fe C.一定有FeCl3 D.一定有Fe
【答案】A ![]() 浓硫酸 C Cl2+ 2OH-= Cl-+ ClO-+ H2O C Fe3++3SCN-= Fe (SCN)3 D
浓硫酸 C Cl2+ 2OH-= Cl-+ ClO-+ H2O C Fe3++3SCN-= Fe (SCN)3 D
【解析】
⑴为排尽装置中的氧气,实验开始时,先点燃A处的酒精灯,反应生成的氯气充满D装置后再加热D处的酒精灯,铁与氯气反应![]() ,故答案为:A,
,故答案为:A,![]() ;
;
⑵C、F装置为了防止水蒸气进入E中,加入的干燥剂应为浓硫酸,故答案为:浓硫酸;
⑶A.收集气体时,集气瓶不能用橡胶塞堵住,应用双孔橡胶塞,故A错误;
B.该装置收集的是密度小于空气的气体,而氯气密度大于空气,且氯气有毒不能直接排放,故B错误;
C.该装置收集比空气密度大的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,故C正确;
D.氯气与氢氧化钠反应,得不到氯气,故D错误;
故答案为:C;
⑷G中氢氧化钠溶液吸收多余氯气,发生的反应为![]() ,离子方程式为
,离子方程式为![]() ,故答案为:
,故答案为:![]() ;
;
⑸滴加几滴KSCN溶液,溶液变血红色,说明溶液中有![]() ,即含有
,即含有![]() ,
,![]() 与
与![]() 反应的离子方程式
反应的离子方程式![]() ,若溶液未变血红色,说明铁粉未完全反应,铁把铁离子还原为亚铁离子。故答案为:C,
,若溶液未变血红色,说明铁粉未完全反应,铁把铁离子还原为亚铁离子。故答案为:C,![]() ,D。
,D。


 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:
【题目】实验小组制备NaNO2,并探究其性质。
I.制备NaNO2
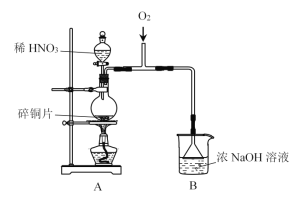
(1)A中发生反应的化学方程式是__________。
(2)B中选用漏斗替代长直导管的优点是________。
(3)为检验B中制得NaNO2,甲进行以下实验:
序号 | 试管 | 操作 | 现象 |
① | 2 mLB中溶液 | 加2 mL 0.1 mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
② | 2 mLB中溶液 | 滴加几滴H2SO4至pH=5,加2 mL 0.1 mol/LKI溶液,滴加几滴淀粉溶液 | 变蓝 |
③ | 2 mLH2O | 滴加几滴H2SO4至pH=5,加2 mL 0.1 mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
实验③的目的是________。
(4)乙认为上述3组实验无法证明B中一定含NaNO2,还需补充实验,理由是_________。
II.探究NaNO2的性质
装置 | 操作 | 现象 |
| 取10 mL1 mol/LNaNO2溶液于试剂瓶中,加入几滴H2SO4酸化,再加入10 mL1 mol/LFeSO4溶液,迅速塞上橡胶塞,缓缓通入足量O2。 | i.溶液迅速变为棕色; ii.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色。 iii.最终形成棕褐色溶液。 |
资料:i.[Fe(NO)]2+在溶液中呈棕色。
ii.HNO2在溶液中不稳定,易分解产生NO和NO2气体。
(5)溶液迅速变为棕色的原因是_________。
(6)已知棕色溶液变浅是由于生成了Fe3+,反应的离子方程式是_________。
(7)最终棕褐色溶液的成分是Fe(OH)x(SO4)y,测得装置中混合溶液体积为20 mL,设计如下实验测定其组成。
资料:充分反应后,Fe2+全部转化为Fe(OH)x(SO4)y。
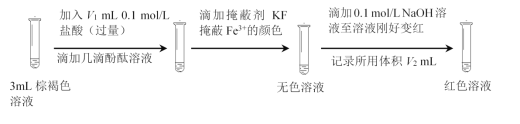
Fe(OH)x(SO4)y中x=_______(用含V1、V2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯乙烯的结构为![]() 。有关该物质的下列说法正确的是( )
。有关该物质的下列说法正确的是( )
A. 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物 6 种
B. 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同
C. 苯乙烯分子的所有原子不可能在同一平面上
D. 除去乙苯中混有的苯乙烯可以通入等量氢气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
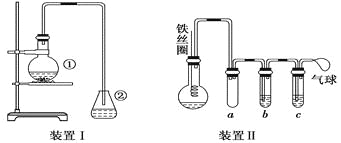
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5 min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应.
(1)装置I中①的化学方程式为__________________________________________.
②中离子方程式为__________________________________________________.
(2)①中长导管的作用是________________________________________________.
(3)烧瓶中生成的红褐色油状液滴的成分是__________________________,要想得到纯净的产物,可用__________________________试剂洗涤.洗涤后分离粗产品应使用的仪器是____________________.
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验.可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳.
a的作用是__________________________________________________________.
b中的试剂是__________________________________________________________.
比较两套装置,装置Ⅱ的主要优点是______________________________________
________________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和CH4催化重整可制备合成气,其反应历程示意图如下:
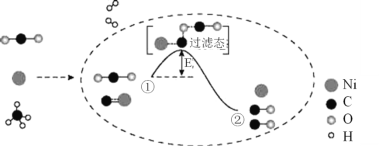
下列说法中不正确的是( )。
A.Ni是该反应的催化剂
B.过程①→②既有碳氧键的断裂,又有碳氧键的形成
C.过程①→②是吸热反应
D.反应的总化学方程式可表示为:CH4 +CO2![]() 2CO+2H2
2CO+2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体 ,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现红色。
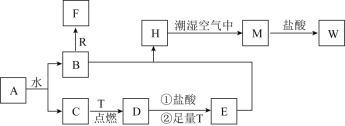
(1)物质D的化学式为___________,H的名称___________。
(2)![]() 在潮湿空气中变成M的实验现象是______________,化学方程式为___________。
在潮湿空气中变成M的实验现象是______________,化学方程式为___________。
(3)![]() 与W溶液也能发生反应,其反应的类型为______(填序号)。
与W溶液也能发生反应,其反应的类型为______(填序号)。
![]() 化合反应
化合反应 ![]() 置换反应
置换反应 ![]() 复分解反应
复分解反应 ![]() 氧化还原反应
氧化还原反应
(4)![]() 和R在溶液中反应生成F的离子方程式为____________________。
和R在溶液中反应生成F的离子方程式为____________________。
(5)将![]() 投入到E溶液中,可以观察到的现象是:___________________。
投入到E溶液中,可以观察到的现象是:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为短周期元素,表中所列序号分别代表一种元素。(除说明外都用化学用语填空)
① | ② | |||||||
③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
(1)上述元素中金属性最强和非金属性最强的元素名称分别是______,_______;
(2)①和②的气态氢化物稳定性比较(写化学式):______________;
(3)在上述元素中其最高价氧化物对应水化物酸性最强的酸为_________;写出⑤单质与③的最高价氧化物对应水化物反应的化学方程式为____________ 。描述H2在⑧单质中燃烧的现象___________________;
(4)现有上表中某一种元素,其单质通入到紫色石蕊溶液中的现象为先变红后褪色,该元素在周期表中的位置是_________________;
(5)比较②和③对应简单离子的离子半径大小(用相应离子符号表示)________;
(6)写出③的最高价氧化物对应水化物的电子式___________;其含有的化学键类型是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 。将一定量的硫酸酸化的KMnO4溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示。下列说法错误的是
。将一定量的硫酸酸化的KMnO4溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示。下列说法错误的是
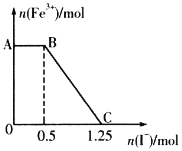
A.AB段发生I-被![]() 氧化的反应
氧化的反应
B.BC段发生的反应为![]()
C.开始时加入KMnO4的物质的量为0.15mol
D.开始时加入FeSO4的物质的量为1.25mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)实验室用图甲装置制备SO3并测定SO2催化氧化为SO3的转化率。
已知:SO3熔点为16.8℃,沸点为44.8℃,假设气体进入装置可以被完全吸收,不考虑空气的影响。

(1)A中使用浓硫酸的质量分数为70%的原因是___,B中浓H2SO4的作用是___。
(2)当实验停止通入SO2,熄灭酒精灯后,还需要继续通一段时间的氧气,其目的是___。
(3)实验结束后测得装置D增加了ag,装置E中的沉淀洗涤烘干后其质量为bg。则E中的沉淀的化学成分是___(填写化学式),本实验中SO2转化率为___(用代数式表示,不用化简)。
(二)SO3溶于浓硫酸后可得到发烟硫酸,工业上把干燥的氯化氢气体通入到发烟硫酸中可以得到HSO3Cl。HSO3Cl是一种无色液体,沸点为152℃,有强腐蚀性,遇湿空气产生强烈的白雾。现用图乙所示的装置制取HSO3Cl(夹持及加热装置略去)。

(1)HSO3Cl遇湿空气产生强烈的白雾,请结合用化学方程式解释其原因___。
(2)分液漏斗下方接的毛细管,其作用是___;若不用毛细管而直接用分液漏斗注入浓盐酸,可能发生的现象是___。
(3)装置F的作用是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com