
【题目】下列说法正确的是
A. 催化剂能够降低化学反应的反应热
B. 己知C(s)+O2(g)=CO2(g) △H1;C(s)+ 1/2O2(g)=CO(g) △H2。则△H1>△H2
C. 已知中和热为ΔH=-57.3 kJ·mol-1,则H2SO4(aq)与Ba(OH)2(aq)反应生成2moIH2O(l) ΔH=-114.6 kJ·mol-1
D. 甲烷的燃烧热为ΔH=-890.3 kJ·mol-1,1g 水蒸气转化为液态水放热2.4444kJ, 则lgCH4完全燃烧生成气态水放出的热量为50.14kJ
【答案】D
【解析】A.使用催化剂不能改变化学反应的反应热(△H),选项A错误;B、ΔH大小比较注意要带“+”、“—”比较。选项所给反应均为放热反应,碳的完全燃烧放出的热量大于不完全燃烧放出的热量即ΔH1<ΔH2,选项B错误;C、H2SO4和Ba(OH)2发生中和反应放热,生成硫酸钡沉淀也放热;已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1,则H2SO4和Ba(OH)2反应的反应热△H<-114.6kJ/mol;选项C错误;D. ①CH4(g)+2O2(g)=CO2(g)+ 2H2O(l) △H1=-890.3 kJ·mol-1, 1g 水蒸气转化为液态水放热2.4444kJ,②H2O(g)= H2O(l) △H2=-18![]() 2.4444 kJ·mol-1=-44.0 kJ·mol-1;故由①-2
2.4444 kJ·mol-1=-44.0 kJ·mol-1;故由①-2![]() ②得反应CH4(g)+2O2(g)=CO2(g)+ 2H2O(g) △H=-890.3 kJ·mol-1-2
②得反应CH4(g)+2O2(g)=CO2(g)+ 2H2O(g) △H=-890.3 kJ·mol-1-2![]() (-44.0 kJ·mol-1)= -802.3 kJ·mol-1,则lgCH4完全燃烧生成气态水放出的热量为
(-44.0 kJ·mol-1)= -802.3 kJ·mol-1,则lgCH4完全燃烧生成气态水放出的热量为![]() kJ=50.14 kJ,选项D正确。答案选D。
kJ=50.14 kJ,选项D正确。答案选D。


科目:高中化学 来源: 题型:
【题目】白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体黑磷,其转化过程中能量变化如图所示.下列叙述中正确的是( ) 
A.黑磷比白磷稳定
B.黑磷与白磷互为同分异构体
C.白磷转化为黑磷是氧化还原反应
D.白磷转化为黑磷是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W 在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍。下列说法不正确的是
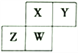
A. 原子半径:Z>W>X>Y
B. 最简单气态氢化物的热稳定性:X>Y>W>Z
C. 最高价氧化物对应水化物的酸性;X>W>Z
D. Y 与X、Y 与Z形成的化合物的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马日夫盐是一种白色晶体,易溶于水,常用于机械设备的磷化处理.以软锰矿(主要成分为MnO2 , 还含有少量的Fe2O3、FeO和Al2O3)为原料制备马日夫盐的流程如图: 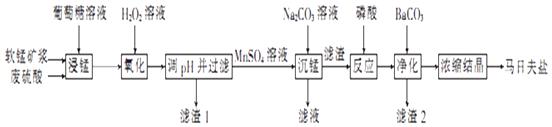
(1)软锰矿要先制成矿浆的目的是 , 葡萄糖(C6H12O6)与MnO2反应时,产物为MnSO4、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为 .
(2)用H2O2溶液“氧化”时发生反应的列子方程式为 .
(3)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如表所示、“调pH并过滤”时,应调整的pH范围为 , 滤渣1的主要成分为(填化学式).
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.8 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
Mn2+ | 7.8 | 9.8 |
(4)加入磷酸后发生反应的化学方程式为 .
(5)某工厂用上述流程制备马日夫盐,已知软锰矿中MnO2的含量为87%,整个流程中锰元素的损耗率为9%,则1t该软锰矿可制得马日夫盐t.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在容积不变的密闭容器中,进行如下可逆反应:C(s)+CO2(g)![]() 2CO(g)下列能表明该反应已达到平衡状态的是
2CO(g)下列能表明该反应已达到平衡状态的是
①2v(CO2)=v(CO) ②2n(CO2)=n(CO)
③2v正(C)=v逆(CO) ④混合气体的密度保持不变
⑤混合气体的平均摩尔质量
A. ④ B. ④⑤ C. ①④ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用食用白醋(醋酸浓度约1 mol/L)进行下列实验,能证明醋酸为弱电解质的是( )
A. 白醋中滴入石蕊试液呈红色 B. 白醋加入豆浆中有沉淀产生
C. 蛋壳浸泡在白醋中有气体放出 D. pH试纸显示白醋的pH为2~3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com