
【题目】下列水溶液一定呈中性的是( )
A. pH=7的溶液 B. c(H+)=1.0×10-7mol·L-1的溶液
C. c(H+)=c(OH-)的溶液 D. pH=3的酸与pH=11的碱等体积混合后的溶液
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A. 常温常压下,11.2L氧气所含的原子数为NA
B. 1.8g的NH4+离子中含有的电子数为0.1NA
C. 常温常压下,48gO3含有的氧原子数为3NA
D. 2.4g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2。该反应的还原产物为______。
(2)已知反应2HI(g)![]() H2(g)+I2(g)的△H = +11 kJ·mol-1,l molH2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(s)分子中化学键断裂时需吸收的能量为______kJ。
H2(g)+I2(g)的△H = +11 kJ·mol-1,l molH2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(s)分子中化学键断裂时需吸收的能量为______kJ。
(3)Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g)。在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)。在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为__________________。
②上述反应中,正反应速率为![]() 正=k正x2(HI),逆反应速率为
正=k正x2(HI),逆反应速率为![]() 逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为____________________(以K和k正表示)。若k正=0.0027 min-1,在t = 40 min时,
逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为____________________(以K和k正表示)。若k正=0.0027 min-1,在t = 40 min时, ![]() 正 = _______________min-1。
正 = _______________min-1。
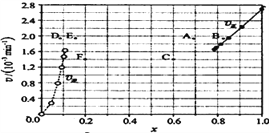
③由上述实验数据计算得到![]() 正~x(HI)和
正~x(HI)和![]() 逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为______________(填字母)。
逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为______________(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3 . 请回答下列问题:
(1)Na3N的电子式是 , 该化合物由键形成.
(2)Na3N与盐酸反应生成种盐,其电子式分别是 , .
(3)Na3N与水的反应属于(填基本反应类型)反应.
(4)比较Na3N中两种粒子的半径:r(Na+)(填“>”“=”“<”) r(N3﹣).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①烧杯、②坩埚、③锥形瓶、④蒸发皿、⑤试管、⑥烧瓶、⑦表面皿,用酒精灯加热时,需要垫石棉网的是
A. ②④⑤ B. ①⑥⑦
C. ③④⑥ D. ①③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com