
【题目】几种短周期元素的原子半径和主要化合价如表所示,下列说法正确的是( )
元素代号 | 原子半径/nm | 主要化合价 |
X | 0.160 | +2 |
Y | 0.143 | +3 |
Z | 0.102 | +6、﹣2 |
L | 0.099 | +7、﹣1 |
M | 0.077 | +4、﹣4 |
Q | 0.074 | ﹣2 |
A.等物质的量的X、Y的单质与足量的盐酸反应,生成![]() 的物质的量相等
的物质的量相等
B.Y与Q形成的化合物不能跟氢氧化钠溶液反应
C.在化学反应中,M原子与其他原子易形成共价键而不易形成离子键
D.Z的简单氢化物的稳定性强于L的简单氢化物的稳定性
【答案】C
【解析】
这几种元素均为短周期元素,由元素的主要化合价可知,Q为O元素,Z有+6、﹣2价,可知Z为S元素;L有+7、﹣1 价,则L为C1元素;M有+4、﹣4价,且原子半径L>M,则M为C元素;X有+2价,Y有+3价,原子半径:X>Y>Z,所以X为Ma元素,Y为Al元素。
A.X为Mg元素,Y为Al元素,等物质的量的X、Y的单质与足量盐酸反应,生成![]() 的物质的量之比为2:3,选项A错误;
的物质的量之比为2:3,选项A错误;
B.Y与Q形成的化合物为![]() ,
,![]() 是两性氧化物,能与氢氧化钠溶液反应生成偏铝酸钠和水,选项B错误;
是两性氧化物,能与氢氧化钠溶液反应生成偏铝酸钠和水,选项B错误;
C.M为C元素,其原子最外层电子数为4,与其他原子易形成共价键而不易形成离子键,选项C正确;
D.非金属性:![]() ,所以简单氢化物的稳定性:
,所以简单氢化物的稳定性:![]() ,选项D错误。
,选项D错误。
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】AG表示溶液酸度:![]() 。常温下,用0.1mol/L的NaOH溶液滴定25 ml 0.1mol/L的CH3COOH滴定结果如图所示,下列分析正确的是()
。常温下,用0.1mol/L的NaOH溶液滴定25 ml 0.1mol/L的CH3COOH滴定结果如图所示,下列分析正确的是()
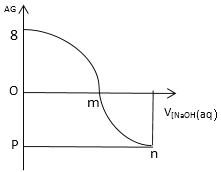
A.0.1mol/L的 CH3COOH溶液的pH=3
B.m点加入NaOH的体积为25mL
C.若pH=7,则溶液中水电离的c(OH-)=1.0×10-3.5 mol/L
D.随着NaOH溶液滴入,溶液中水的电离程度逐渐增大,m点最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有下列6种离子中的某几种:Cl-、SO42-、CO32-、NH4+、Na+、K+。为确认溶液组成进行如下实验:(1) 200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。(2) 向(1)的滤液中加入足量的NaOH溶液,加热,标准状况下产生能使湿润红色石蕊试纸变蓝的气体1.12 L。由此可以得出关于原溶液组成的正确结论是
A. 一定存在SO42-、CO32-、NH4+,可能存在Cl-、Na+、K+
B. 一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+
C. c(CO32-)=0.01mol·L-1,c(NH4+)>c(SO42-)
D. 如果上述6种离子都存在,则c(Cl-)>c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)

(1)写出下列物质的化学式:F____________,G________________。
(2)将混合物中两种金属分离开的最简单的方法是___________。
(3)D→E的转化中,加入过量的X可能是_____________________。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______________________________________________;
H→I:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图所示装置探究氯气能否与水发生反应。已知气体a的主要成分是含有少量水蒸气的氯气。请回答下列问题:
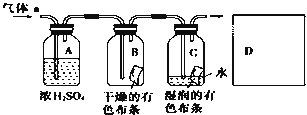
(1)浓硫酸的作用是_____________________________________。
(2)写出实验室制取Cl2的化学方程式_______________________________。
(3)证明氯气和水发生反应的实验现象为___________________________。
(4)该实验设计存在的缺陷是________,为了克服该缺陷,需要补充装置D,其中发生反应的离子方程式为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确解释下列反应原理,并且书写的离子方程式正确的是( )
A.用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+
B.用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O
C.电解MgCl2饱和溶液制取Mg:MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
D.用碳酸钠溶液浸泡锅炉水垢:CaSO4+CO32-=CaCO3+SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1mol·L-1 KNO3溶液:Mg2+、Fe3+、Cl-、![]()
B.无色透明的溶液:Cu2+、![]() 、
、![]() 、
、![]()
C.使pH试纸变红的溶液:K+、Ca2+、Cl-、ClO-
D.水电离出的c(H+)=10-12mol·L-1的溶液:Na+、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 互为同分异构体,下列说法不正确的是
互为同分异构体,下列说法不正确的是
A. z的二氯代物有三种
B. x、y的一氯代物均只有三种
C. x、y、z中只有x的所有原子可能处于同一平面
D. x、y 可使溴的四氯化碳溶液因发生加成反应而褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取冰晶石(![]() )的化学方程式为
)的化学方程式为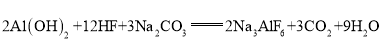 ,反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是( )
,反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是( )
A.简单氢化物的稳定性强弱
B.最高价氧化物对应水化物的碱性或酸性强弱
C.原子达到稳定结构失去或得到电子的多少
D.元素的最高化合价的高低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com